- Таблица: плотности газов, химические формулы газов и молекулярные веса основных распространенных газов — ацетилен, воздух, метан, азот, кислород и многих других — инженерный справочник / технический справочник дпва / таблицы для инженеров (ex dpva-info)
- Нахождение в природе
- Применение кислорода:
- Разложение кислородсодержащих веществ
- Сварка и резка металлов
- Свойства и применение кислорода
- Физические свойства
- Химические свойства
- Химические формулы таблица
Таблица: плотности газов, химические формулы газов и молекулярные веса основных распространенных газов — ацетилен, воздух, метан, азот, кислород и многих других — инженерный справочник / технический справочник дпва / таблицы для инженеров (ex dpva-info)
| Газ | Химическая формула | Молекулярный вес | Плотность | ||
кг/м3 | футов/фут3(lb/ft3) | относительная плотность газа по воздуху | |||
| Азот / Nitrogen | N2 | 28.02 | 1.1651) 1.25062) | 0.07271) 0.0780722) | 0,97 |
| Ацетилен = этин / Acetylene (ethyne) | C2H2 | 26 | 1.0921) 1.1702) | 0.06821) 0.07292) | 0,91 |
| Аммиак / Ammonia | NH3 | 17.031 | 0.7171) 0.7692) | 0.04481) 0.04802) | 0,60 |
| Аргон / Argon | Ar | 39.948 | 1.6611) 1.78372) | 0.10371) 0.1113532) | 1,38 |
| Бензол / Benzene | C6H6 | 78.11 | 3.486 | 0.20643 | 2,90 |
| Биогаз, генерируемый метантенком; метан, генерируемый метантенком / Digester Gas (Sewage or Biogas) | 0.062 | ||||
| Бутан / Butane | C4H10 | 58.1 | 2.4891) 2.52) | 0.15541) 0.1562) | 2,07 |
| Бутилен = Бутен / Butylene (Butene) | C4H8 | 56.11 | 2.504 | 0.1482) | 2,03 |
| Веселящий газ, закись азота / Nitrous Oxide | N2O | 44.013 | 1.9801) | 0.114 | 1,65 |
| Водород / Hydrogen | H2 | 2.016 | 0.08992) | 0.00562) | 0,08 |
| Водяной пар / Water Vapor, steam | H2O | 18.016 | 0.804 | 0.048 | 0,67 |
| Водяной битуминозный газ= голубой водяной газ жирный / Water gas (bituminous) | 0.054 | ||||
| Водяной карбюрированный газ = голубой водяной газ / Carbureted Water Gas | 0.048 | ||||
| Воздух / Air | 29 | 1.2051) 1.2932) | 0.07521) 0.08062) | 1 | |
| Газ | Химическая формула | Молекулярный вес | Плотность | ||
кг/м3 | футов/фут3(lb/ft3) | ||||
| Гелий / Helium | He | 4.02 | 0.16641) 0.17852) | 0.010391) 0.0111432) | 0,014 |
| Гексан / Hexane | 86.17 | ||||
| Двукосиь азота / Nitric oxide | NO | 30.0 | 1.2491) | 0.07801) | 1,04 |
| Двуокись азота = перекись азота / Nitrogen Dioxide | NO2 | 46.006 | |||
| Доменный газ = колошниковый газ / Blast furnace gas | 1.2502) | 0.07802) | 0,97 | ||
| Дисульфид углерода = двусернистый углерод = сернистый углерод = сероуглерод / Carbon disulphide | 76.13 | ||||
| Криптон / Krypton | 3.742) | 2,90 | |||
| Коксовальный газ = коксовый газ / Coke Oven Gas | 0.0342) | ||||
| Метан / Methane | CH4 | 16.043 | 0.6681) 0.7172) | 0.04171) 0.04472) | 0,56 |
| Метиловый спирт / Methyl Alcohol | 32.04 | ||||
| Пригодный газ = натуральный газ / Natural gas | 19.5 | 0.7 — 0.92) | 0.044 — 0.0562) | 0,55-0,70 | |
| Продукты сгорания = смесь продуктов полного сгорания в виде CO2, Н2О, SO2 и золы неполного сгорания в виде СО, Н2, и др., а также азота и кислорода / Combustion products | 1.112) | 0.0692) | 0,86 | ||
| Изопентан / Iso-Pentane | 72.15 | ||||
| Газ | Химическая формула | Молекулярный вес | Плотность | ||
кг/м3 | футов/фут3(lb/ft3) | ||||
| Кислород / Oxygen | O2 | 32 | 1.3311) 1.42902) | 0.08311) 0.0892102) | 1,11 |
| Ксенон / Xenon | 5.862) | 4,54 | |||
| Метилбензол = толуол / Toluene | C7H8 | 92.141 | 4.111 | 0.2435 | 3,42 |
| Неон / Neon | Ne | 20.179 | 0.89992) | 0.0561792) | 0,70 |
| Н-гептан / N-Heptane | 100.20 | ||||
| Н-октан / N-Octane | 114.22 | ||||
| Н-пентан / N-Pentane | 72.15 | ||||
| Озон / Ozone | O3 | 48.0 | 2.142) | 0.125 | 1,78 |
| Оксид серы (II)= диоксид серы = двуокись серы = сернистый ангидрид = сернистый газ / Sulfur Dioxide | SO2 | 64.06 | 2.2791) 2.9262) | 0.17031) 0.18282) | 1,90 |
| Оксид серы (III)= триоксид серы = серный ангидрид = серный газ / Sulfur Trioxide | SO3 | 80.062 | |||
| Оксид серы (I)= моноксид серы / Sulfuric Oxide | SO | 48.063 | |||
| Пропан / Propane | C3H8 | 44.09 | 1.8821) | 0.11751) | 1,57 |
| Пропен = пропилен / Propene (propylene) | C3H6 | 42.1 | 1.7481) | 0.10911) | 1,45 |
| Перокид азота / Nitrous Trioxide | NO3 | 62.005 | |||
| Светильный газ угольный газ (горючий газ, состоящий из 20-30% метана и 50% водорода получаемый из каменного угля в процессе его полукоксования и частичного термического крекинга / Coal gas | 0.5802) | 0,45 | |||
| Сера / Sulfur | S | 32.06 | 0.135 | ||
| Соляная кислота = хлористый водород / Hydrochloric Acid = Hydrogen Chloride | HCl | 36.5 | 1.5281) | 0.09541) | 1,27 |
| Сероводород = сернистый водород / Hydrogen Sulfide | H2S | 34.076 | 1.4341) | 0.08951) | 1,19 |
| Угарный газ, моноксид углерода / Carbon monoxide | CO | 28.01 | 1.1651) 1.2502) | 0.07271) 0.07802) | 0,97 |
| Углекислый газ = двуокись углерода, диоксид углерода / Carbon dioxide | CO2 | 44.01 | 1.8421) 1.9772) | 0.11501) 0.12342) | 1,53 |
| Газ | Химическая формула | Молекулярный вес | Плотность | ||
кг/м3 | футов/фут3(lb/ft3) | ||||
| Хладагент R-11 | 137.37 | ||||
| Хладагент R-12 | 120.92 | ||||
| Хладагент R-22 | 86.48 | ||||
| Хладагент R40 = хлористый метил / Methyl Chloride | 50.49 | ||||
| Хладагент R-114 | 170.93 | ||||
| Хладагент R-123 | 152.93 | ||||
| Хладагент R-134a | 102.03 | ||||
| Холодильный агент R160 =хлористый этил / Ethyl Chloride | 64.52 | ||||
| Хлор / Chlorine | Cl2 | 70.906 | 2.9941) | 0.18691) | 2,49 |
| Циклогексан / Cyclohexane | 84.16 | ||||
| Этан / Ethane | C2H6 | 30.07 | 1.2641) | 0.07891) | 1,05 |
| Этиловый спирт = этанол / Ethyl Alcohol | 46.07 | ||||
| Этилен / Ethylene | C2H4 | 28.03 | 1.2602) | 0.07862) | 0,98 |
1)NTP — Нормальная температура и давление (Normal Temperature and Pressure) — 20oC (293.15 K, 68oF) при 1 атм ( 101.325 кН/м2, 101.325 кПа, 14.7 psia, 0 psig, 30 in Hg, 760 мм.рт.ст)
2)STP — Стандартная температура и давление (Standard Temperature and Pressure) — 0oC (273.15 K, 32oF) при 1 атм (101.325 кН/м2, 101.325 кПа, 14.7 psia, 0 psig, 30 in Hg, 760 torr=мм.рт.ст)
Нахождение в природе

Накопление O
2
в
атмосфере
Земли. Зелёный график — нижняя оценка уровня кислорода, красный — верхняя оценка.
1
. (3,85—2,45 млрд лет назад) — O
2
не производился
2
. (2,45—1,85 млрд лет назад) — O
2
производился, но поглощался океаном и породами морского дна
3
. (1,85—0,85 млрд лет назад) — O
2
выходит из океана, но расходуется при окислении горных пород на суше и при образовании озонового слоя
4
. (0,85—0,54 млрд лет назад) — все горные породы на суше окислены, начинается накопление O
2
в атмосфере
5
. (0,54 млрд лет назад — по настоящее время) — современный период, содержание O
2
в атмосфере стабилизировалось
Кислород — самый распространённый в земной коре элемент, на его долю (в составе различных соединений, главным образом силикатов) приходится около 47 % массы твёрдой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе).
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе (около 1015 тонн[7]). Однако до появления первых фотосинтезирующих микробов в архее 3,5 млрд лет назад в атмосфере его практически не было.
Свободный кислород в больших количествах начал появляться в палеопротерозое (3—2,3 млрд лет назад) в результате глобального изменения состава атмосферы (кислородной катастрофы). Первый миллиард лет практически весь кислород поглощался растворённым в океанах железом и формировал залежи джеспилита.
Наличие большого количества растворённого и свободного кислорода в океанах и атмосфере привело к вымиранию большинства анаэробных организмов. Тем не менее, клеточное дыхание с помощью кислорода позволило аэробным организмам производить гораздо больше АТФ, чем анаэробным, сделав их доминирующими[10].
С начала кембрия 540 млн лет назад содержание кислорода колебалось от 15 % до 30 % по объёму[11]. К концу каменноугольного периода (около 300 миллионов лет назад) его уровень достиг максимума в 35 % по объёму, который, возможно, способствовал большому размеру насекомых и земноводных в это время[12].
Основная часть кислорода на Земле выделяется фитопланктоном Мирового океана. Около 60 % кислорода от используемого живыми существами расходуется на процессы гниения и разложения, 80 % кислорода, производимого лесами, уходит на гниение и разложение растительности лесов[13].
Деятельность человека очень мало влияет на количество свободного кислорода в атмосфере[14][нет в источнике].
Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет около 25 %, по массовой доле — около 65 %[6].
В 2022 году датские учёные доказали, что свободный кислород входил в состав атмосферы уже 3,8 млрд лет назад[16].
Применение кислорода:
Таблица химических элементов Д.И. Менделеева
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева
Разложение кислородсодержащих веществ
Небольшие количества кислорода можно получать нагреванием перманганата калия KMnO4:
- 2KMnO4→tK2MnO4 MnO2 O2↑{displaystyle {ce {2KMnO4 ->[t] K2MnO4 MnO2 O2 ^}}}
Используют также реакцию каталитического разложения пероксида водорода H2O2 в присутствии оксида марганца(IV):
- 2H2O2→MnO22H2O O2↑{displaystyle {ce {2H2O2 ->[MnO2] 2H2O O2 ^}}}
Кислород можно получить каталитическим разложением хлората калия (бертолетовой соли) KClO3:
- 2KClO3⟶2KCl 3O2↑{displaystyle {ce {2KClO3 -> 2KCl 3O2 ^}}}
Разложение оксида ртути(II) (при t = 100 °C) было первым методом синтеза кислорода:
- 2HgO→100°C2Hg O2↑{displaystyle {ce {2HgO ->[100{°}C] 2Hg O2 ^}}}
Сварка и резка металлов
Кислород в баллонах голубого цвета широко используется для газопламенной резки и сварки металлов.
В качестве окислителя для ракетного топлива применяется жидкий кислород, пероксид водорода, азотная кислота и другие богатые кислородом соединения.
Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива (удельный импульс смеси водород — озон превышает удельный импульс для пары водород-фтор и водород-фторид кислорода).
Медицинский кислород хранится в металлических газовых баллонах высокого давления голубого цвета различной ёмкости от 1,2 до 10,0 литров под давлением до 15 МПа (150 атм) и используется для обогащения дыхательных газовых смесей в наркозной аппаратуре, при нарушении дыхания, для купирования приступа бронхиальной астмы, устранения гипоксии любого генеза, при декомпрессионной болезни, для лечения патологии желудочно-кишечного тракта в виде кислородных коктейлей.
Крупные медицинские учреждения могут использовать не сжатый кислород в баллонах, а сжиженный в сосуде Дьюара большой ёмкости. Для индивидуального применения медицинским кислородом из баллонов заполняют специальные прорезиненные ёмкости — кислородные подушки.
Для подачи кислорода или кислородо-воздушной смеси одновременно одному или двум пострадавшим в полевых условиях или в условиях стационара применяются кислородные ингаляторы различных моделей и модификаций. Достоинством кислородного ингалятора является наличие конденсатора-увлажнителя газовой смеси, использующего влагу выдыхаемого воздуха.
Для расчёта оставшегося в баллоне количества кислорода в литрах обычно величину давления в баллоне в атмосферах (по манометруредуктора) умножают на величину ёмкости баллона в литрах. Например, в баллоне вместимостью 2 литра манометр показывает давление кислорода 100 атм.
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавкиE948[26], как пропеллент и упаковочный газ.
В химической промышленности кислород используют как реактив-окислитель в многочисленных синтезах, например, окисления углеводородов в кислородсодержащие соединения (спирты, альдегиды, кислоты), диоксид серы в триоксид серы, аммиака в оксиды азота в производстве азотной кислоты.
В тепличном хозяйстве для изготовления кислородных коктейлей, для прибавки в весе у животных, для обогащения кислородом водной среды в рыбоводстве.
Свойства и применение кислорода
Рассмотрите картинки и поясните свои соображения. Какова причина длительного пребывания водолазов под водой? Где ещё используется кислородный баллон?
Физические свойства:
Кислород — это бесцветный газ без запаха и вкуса, относительно мало растворим в воде (при температуре 20°С в 100 объёмах воды растворяется 3,1 объёма кислорода). Кислород немного тяжелее воздуха, при температуре — 183 °С сжижается, а при понижении температуры до — 218,8 °С — затвердевает.
Химические свойства:
В обычных условиях кислород в чистом виде и в составе воздуха химически неактивен. Однако при нагревании его активность резко возрастает. Кислород может находиться во взаимодействии с большинством простых веществ — неметаллами и металлами, а также со сложными веществами.
Взаимодействие кислорода с неметаллами. Если раскалить под действием пламени спиртовки уголек в железной ложке, то он не загорится, а начнет дымиться. Поместим железную ложку с дымящимся угольком в банку с кислородом (для того, чтобы банка не разбилась, дно посыпаем мелким песком). Раскаленный уголек будет гореть без пламени, выделяя тепло. Если нальем в банку известковую воду 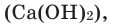
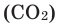
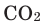
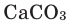
При горении раскаленного угля в условиях нехватки кислорода образуется очень опасный удушающий угарный газ:
Нагреем в железной ложке немножко серы. Сера горит слабым голубоватым пламенем. Опустим ложку в банку с кислородом. Скорость горения серы увеличивается, появляется пламя ярко-голубого цвета. В банке образуется бесцветный газ с резким запахом — серный газ (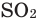
Возьмем немного фосфора в железной ложке и нагреем на огне спиртовки. Фосфор начинает гореть. Если опустить горящий фосфор в банку с кислородом, то горение ускорится и очень скоро банка наполнится белым дымом оксида фосфора (V). Горение фосфора тоже сопровождается выделением теплоты.
Все неметаллы, кроме фтора (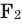
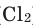
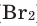
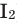
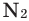
Взаимодействие кислорода с металлами. Кроме ценных (благородных) металлов (Ag, Au, Pt), большинство других металлов находятся в непосредственном взаимодействии с кислородом. Для вступления металлов в реакцию с кислородом, их следует нагреть, после чего реакция протекает самопроизвольно, с выделением света и тепла.
Магний горит в воздухе ярким, ослепительным пламенем. Если опустить ленту горящего магния в сосуд с кислородом, яркость пламени еще больше увеличится. В результате реакции образуется белый порошок оксида магния:
Если, насадив на железную проволоку деревянную щепку, мы зажжем ее и опустим в сосуд с кислородом, то вначале будет гореть кусок дерева, а затем железо. Железо горит без пламени, разбрасывая вокруг искры железной окалины.
Сложные вещества, состоящие из двух элементов, один из которых является кислородом, называются оксидами.
Взаимодействие сложных веществ с кислородом. Как и простые вещества, сложные вещества тоже могут гореть в кислороде и окисляться. Реакции взаимодействия веществ с кислородом являются реакциями окисления. Ряд оксидов, взаимодействуя с кислородом, образуют новые оксиды.
В наших квартирах ежедневно в газовых печах горит природный газ (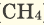
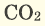
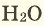
Серные соединения некоторых металлов (сульфиды) при горении в кислороде образуют два оксида.
Применение:
Сварка и резка металлов происходит при участии чистого кислорода. В металлургической и химической промышленности больше всего используется кислород из воздуха. Например, при производстве чугуна и серной кислоты использование кислорода из воздуха позволяет значительно ускорить и повысить производительность производственных процессов.
В медицине чистый кислород применяют для облегчения затрудненного дыхания. В этих целях в больницах используются кислородные подушки и заполненные чистым кислородом стальные баллоны. Летающие на большой высоте летчики, космонавты, работающие под водой водолазы также пользуются небольшими по размеру кислородными баллонами.
Все живые организмы в природе при дыхании употребляют кислород, ежегодно усваивая миллионы тонн атмосферного кислорода. Так, например, было вычислено, что только люди употребляют в течение года свыше 1330 миллиардов кубических метров атмосферного кислорода.
В организме человека и животных происходит медленное окисление глюкозы кислородом (рис. 2).
Физические свойства
При нормальных условиях кислород — это газ без цвета, вкуса и запаха.
1 л его при нормальных условиях имеет массу 1,429 г., то есть немного тяжелее воздуха. Слабо растворяется в воде (4,9 мл/100 г при 0 °C,2,09 мл/100 г при 50 °C) и спирте(2,78 мл/100 г при 25 °C).
Межатомное расстояние — 0,12074 нм. Является парамагнетиком. В жидком виде притягивается магнитом.
При нагревании газообразного кислорода происходит его обратимая диссоциация на атомы, концентрация диссоциированных атомов в смеси при 2000 °C — 0,03 %, при 2600 °C — 1 %, 4000 °C — 59 %, 6000 °C — 99,5 %.
Жидкий кислород кипит под давлением 101,325 кПа при температуре −182,98 °C и представляет собой бледно-голубую жидкость. Критическая температура кислорода 154,58 К (-118,57 °C), критическое давление 4,882 МПа[17].
Твёрдый кислород (температура плавления −218,35 °C) — синие кристаллы.
Известны 6 кристаллических фаз, из которых три существуют при давлении в 1 атм.:
- α-О2 — существует при температуре ниже 23,65 K; ярко-синие кристаллы относятся к моноклинной сингонии, параметры ячейкиa=5,403 Å,b=3,429 Å,c=5,086 Å;β=132,53°[18].β-O2 — существует в интервале температур от 23,65 до 43,65 K; бледно-синие кристаллы (при повышении давления цвет переходит в розовый) имеют ромбоэдрическую решётку, параметры ячейки a=4,21 Å,α=46,25°[18].γ-O2 — существует при температурах от 43,65 до 54,21 K; бледно-синие кристаллы имеют кубическую симметрию, период решётки a=6,83 Å[18].
Ещё три фазы существуют при высоких давлениях:
Химические свойства
Сильный окислитель, самый активный неметалл после фтора, образует бинарные соединения (оксиды) со всеми элементами, кроме гелия, неона, аргона, фтора (с фтором кислород образует фторид кислорода, так как фтор более электроотрицателен, чем кислород).
- 4Li O2⟶2Li2O{displaystyle {ce {4Li O2 -> 2Li2O}}}
- 2Sr O2⟶2SrO{displaystyle {ce {2Sr O2 -> 2SrO}}}
Окисляет соединения, которые содержат элементы с не максимальной степенью окисления:
- 2NO O2⟶2NO2↑{displaystyle {ce {2NO O2 -> 2NO2 ^}}}
Окисляет большинство органических соединений в реакциях горения:
- 2C6H6 15O2⟶12CO2 6H2O{displaystyle {ce {2C6H6 15O2 -> 12CO2 6H2O}}}
- CH3CH2OH 3O2⟶2CO2 3H2O{displaystyle {ce {CH3CH2OH 3O2 -> 2CO2 3H2O}}}
При определённых условиях можно провести мягкое окисление органического соединения:
- CH3CH2OH O2⟶CH3COOH H2O{displaystyle {ce {CH3CH2OH O2 -> CH3COOH H2O}}}
Кислород реагирует непосредственно (при нормальных условиях, при нагревании и/или в присутствии катализаторов) со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета.
Косвенным путём получены оксиды золота и тяжёлых инертных газов (Xe, Rn). Во всех двухэлементных соединениях кислорода с другими элементами кислород играет роль окислителя, кроме соединений со фтором (см. ниже #Фториды кислорода).
Кислород образует пероксиды со степенью окисления атома кислорода, формально равной −1.
- 2Na O2⟶Na2O2{displaystyle {ce {2Na O2 -> Na2O2}}}
- 2BaO O2⟶2BaO2{displaystyle {ce {2BaO O2 -> 2BaO2}}}
- H2 O2⟶H2O2{displaystyle {ce {H2 O2 -> H2O2}}}
- Na2O2 O2⟶2NaO2{displaystyle {ce {Na2O2 O2 -> 2NaO2}}}
- K O2⟶KO2{displaystyle {ce {K O2 -> KO2}}}
- 3KOH 3O3⟶2KO3 KOH⋅H2O 2O2↑{displaystyle {ce {3KOH 3O3 -> 2KO3 KOH * H2O 2O2 ^}}}
- PtF6 O2⟶O2PtF6{displaystyle {ce {PtF6 O2 -> O2PtF6}}}
В этой реакции кислород проявляет восстановительные свойства.
Химические формулы таблица
Все формулы химических соединений на одной странице.
| Название химического соединения | Формула |
| Азид бария | BaN6 |
| Азид кадмия | Cd(N3)2 |
| Азид серебра | AgN3 |
| Азид цезия | CsN3 |
| Азот | N2 |
| Азотистая кислота | HNO2 |
| Азотисто- водородная кислота | HN3 |
| Азотная кислота | HNO3 |
| Азулен | C10H8 |
| Акрилонитрил | H2C(CH)CN |
| Аланин Ala | C3H7NO2 |
| Альбит | N4H4 |
| Алюминат бария | Ba(AlO2)2 |
| Алюминат кобальта(II) | CoAl2O4 |
| Алюминат лития | AlLiO2 |
| Алюминат магния | Mg(AlO2)2 |
| Алюминат натрия | AlNaO2 |
| Алюминат цинка | Zn(AlO2)2 |
| Амид ион | NH2− |
| Амид цезия | CsNH2 |
| Аммиак | NH3 |
| Андалузит | Al2O5Si |
| Антимонид галлия | GaSb |
| Антимонид индия | InSb |
| Антимонид кадмия | CdSb |
| Антимонид кобальта | CoSb |
| Антимонид марганца(II) | Mn3Sb2 |
| Антимонид меди(III) | Cu3Sb |
| Антимонид никеля(II) | Ni3Sb2 |
| Антимонид хрома | CrSb |
| Антимонид хрома(II) | Cr3Sb2 |
| Антимонид цинка | ZnSb |
| Антимонид цинка | Zn3Sb2 |
| Антрацен | C14H10 |
| Аргинин | C6H14N4O2 |
| Арсенат бария | Ba(AsO4)2 |
| Арсенат бора | BAsO4 |
| Арсенат цинка | Zn3(AsO4)2 |
| Арсенид бора | BAs |
| Арсенид галлия | GaAs |
| Арсенид индия | InAs |
| Арсенид иттрия | YAs |
| Арсенид кадмия | Cd3As2 |
| Арсенид кобальта | CoAs |
| Арсенид кобальта(II) | CoAs2 |
| Арсенид магния | Mg3As2 |
| Арсенид марганца(II) | Mn3As2 |
| Арсенид марганца(III) | MnAs |
| Арсенид меди(I) | Cu3As |
| Арсенид никеля(III) | NiAs |
| Арсенид таллия | AsTl |
| Арсенид хрома(II) | Cr3As2 |
| Арсенид цинка | Zn3As2 |
| Арсенит бария | Ba(AsO3)2 |
| Арсенит цинка | Zn(AsO2)2 |
| Арсин | AsH3 |
| Аскорбиновая кислота | HC6H7O6 |
| Аспарагин | C4H8N2O3 |
| Аспарагиновая кислота Asp | C4H7NO4 |
| Аспартам | C14H18N2O5 |
| Аспирин | C9H8O4 |
| Ацетальдегид | CH3CHO |
| Ацетамид | CH3CONH2 |
| Ацетат | CH3COO− |
| Ацетат | C2H3O2− |
| Ацетат бария | Ba(C2H3O2)2 |
| Ацетат бериллия | Be(C2H3O2)2 |
| Ацетат висмута (III) | Bi(C2H3O2)3 |
| Ацетат галлия | Ga(C2H3O2)3 |
| Ацетат кадмия | Cd(C2H3O2)2 |
| Ацетат кальция | Ca(C2H3O2)2 |
| Ацетат кобальта(II) | Co(C2H3O2)2 |
| Ацетат ртути(II) | Hg(C2H3O2)2 |
| Ацетат свинца — тригидрат | Pb(CH3COO)2 · 3H2O |
| Ацетат серебра | AgC2H3O2 |
| Ацетат цезия | CsC2H3O2 |
| Ацетилацетонат бериллия | Be(C5H7O2)2 |
| Ацетилен | C2H2 |
| Ацетилен | HCCH или C2H2 |
| Ацетиленид серебра | Ag2C2 |
| Ацетил- салициловая кислота | C9H8O4 |
| Ацетил- салициловая кислота | HC9H7O4 |
| Ацетилхлорид | CH3COCl |
| Ацетоаминофен | C8H9NO2 |
| Ацетоацетат этила | C6H10O3 |
| Ацетон | CH3COCH3 |
| Ацетон | (CH3)2CO |
| Бадделеит | ZrO2 |
| Барит | |
| Бензальдегид | C6H5CHO |
| Бензилацетат | CH3COOCH2C6H5 |
| Бензиловый спирт | C6H5CH2OH |
| Бензоат | C6H5COO− |
| Бензоат натрия | NaC6H5COO |
| Бензоилхлорид | C6H5COCl |
| Бензойная кислота | C6H5COOH |
| Бензол | C6H6 |
| Бензофенон | C13H10O |
| Бертолетова соль (хлорат калия) | KClO3 |
| Бифенил | C12H10 |
| Боразол | B3N3H6 |
| Борат алюминия | AlBO2 |
| Борат висмута(III) | BiBO3 |
| Борат цезия | CsBO2 |
| Боргидрид бериллия | Be(BH4)2 |
| Борид бериллия | BeB2 |
| Борид иттрия | YB6 |
| Борид кальция | CaB6 |
| Борид кальция | CaB6 |
| Борид кобальта | Co2B |
| Борид кобальта(II) | CoB |
| Борид церия | CeB6 |
| Борид циркония | ZrB2 |
| Борная кислота | B(OH)3 |
| Бром | Br2 |
| Бромат | BrO3− |
| Бромат лития | LiBrO3 |
| Бромат серебра | AgBrO3 |
| Бромат цезия | CsBrO3 |
| Бромдииодид индия(III) | InBrI2 |
| Бромид аммония | NH4Br |
| Бромид бария | BaBr2 |
| Бромид бериллия | BeBr2 |
| Бромид бора | BBr3 |
| Бромид ванадия(II) | VBr2 |
| Бромид ванадия(III) | VBr3 |
| Бромид висмута(III) | BiBr3 |
| Бромид вольфрама(II) | WBr2 |
| Бромид вольфрама(III) | WBr3 |
| Бромид вольфрама(IV) | WBr4 |
| Бромид вольфрама(V) | WBr5 |
| Бромид вольфрама(VI) | WBr6 |
| Бромид галлия | GaBr3 |
| Бромид гафния(IV) | HfBr4 |
| Бромид германия | GeBr4 |
| Бромид золота(I) | AuBr |
| Бромид золота(III) | AuBr3 |
| Бромид индия(I) | InBr |
| Бромид индия(III) | InBr3 |
| Бромид иода(I) | IBr |
| Бромид иода(III) | IBr3 |
| Бромид иттербия(II) | YbBr2 |
| Бромид иттербия(III) | YbBr3 |
| Бромид иттрия | YBr3 |
| Бромид кадмия | CdBr2 |
| Бромид кальция | CaBr2 |
| Бромид кобальта(II) | CoBr2 |
| Бромид лития | LiBr |
| Бромид марганца(II) | MnBr2 |
| Бромид меди(I) | CuBr |
| Бромид меди(II) | CuBr2 |
| Бромид молибдена(II) | MoBr2 |
| Бромид молибдена(III) | MoBr3 |
| Бромид натрия | NaBr |
| Бромид никеля(II) | NiBr2 |
| Бромид ниобия(V) | NbBr5 |
| Бромид ртути(I) | Hg2Br2 |
| Бромид ртути(I) | HgBr |
| Бромид ртути(II) | HgBr2 |
| Бромид серебра(I) | AgBr |
| Бромид тантала (III) | TaBr3 |
| Бромид тантала (V) | TaBr5 |
| Бромид хрома(II) | CrBr2 |
| Бромид хрома(III) | CrBr3 |
| Бромид цезия | CsBr |
| Бромид церия(III) | CeBr3 |
| Бромид цинка | ZnBr2 |
| Бромид циркония | ZrBr4 |
| Бромоводород | HBr |
| Бромэтан | CH3CH2Br |
| Бромэтан | C2H5Br |
| Бутан | C4H10 |
| Бутанол-1 | CH3CH2CH2 CH2OH |
| Бутиловый спирт | C4H9OH |
| Валин | C5H11NO2 |
| Винилацетат | CH3COOCHCH2 |
| Винилхлорид | C2H3Cl |
| Винная кислота | H2C4H4O6 |
| Висмутид магния | Mg3Bi2 |
| Висмутид марганца(III) | MnBi |
| Витамин B1 | HC12H17ON4SCl2 |
| Витерит | |
| Вода | H2O |
| Водород | H2 |
| Волластонит | CaSiO3 |
| Вольфрамат бария | BaWO4 |
| Вольфрамат ион | WO42− |
| Вольфрамат кадмия | CdWO4 |
| Вольфрамат кальция | CaWO4 |
| Вольфрамат кобальта(II) | CoWO4 |
| Вольфрамат магния | MgWO4 |
| Вольфрамат меди(II) | CuWO4 |
| Вольфрамат ртути(II) | HgWO4 |
| Вольфрамат цезия | Cs2WO4 |
| Галенит | PbS |
| Галит | NaCl |
| Гашёная известь | Ca(OH)2 |
| Гексаборид бария | BaB6 |
| Гексабромид диалюминия | Al2Br6 |
| Гексагидрат бромата меди (II) | Cu(BrO3)2 · 6H2O |
| Гексагидрат хлората меди (II) | Cu(ClO3)2 · 6H2O |
| Гексадекан | C16H34 |
| Гексаиодид диалюминия | Al2I6 |
| Гексан | C6H14 |
| Гекса- оксидифторид | O6F2 |
| Гекса- тиоциано- платинат (IV) аммония | (NH4)2[Pt(SCN)6] |
| Гексафторид диалюминия | Al2F6 |
| Гекса- фтороалюминат калия | AlF6K3 |
| Гекса- фтороалюминат лития | AlF6Li3 |
| Гекса- фтороалюминат натрия(криолит) | AlF6Na3 |
| Гекса- фторосиликат бария | BaSiF6 |
| Гекса- хлороалюминат калия | AlCl6K3 |
| Гекса- хлороалюминат натрия | AlCl6Na3 |
| Гекса- хлороплатинат (IV) аммония | (NH4)2[PtCl6] |
| Гекса- цианоферрат (III) кобальта(II) | Co3(Fe(CN)6)2 |
| Гептадекан | C17H36 |
| Гептан | C7H16 |
| Гидразин | H2NNH2 |
| Гидразин | N2H4 |
| Гидрат сульфата кальция | CaSO4 · 0.5H2O |
| Гидрид кальция | CaH2 |
| Гидрид натрия | NaH |
| Гидрид-фторид аргона | ArFH |
| Гидрид-хлорид аргона | ArClH |
| Гидрокарбонат | HCO3− |
| Гидрокарбонат натрия | NaHCO3 |
| Гидроксид алюминия | Al(OH)3 |
| Гидроксид бария | Ba(OH)2 |
| Гидроксид бериллия | Be(OH)2 |
| Гидроксид галлия | Ga(OH)3 |
| Гидроксид золота(III) | Au(OH)3 |
| Гидроксид индия(III) | In(OH)3 |
| Гидроксид кадмия | Cd(OH)2 |
| Гидроксид кальция | Ca(OH)2 |
| Гидроксид кобальта(II) | Co(OH)2 |
| Гидроксид кобальта(III) | Co(OH)3 |
| Гидроксид магния | Mg(OH)2 |
| Гидроксид марганца(II) | Mn(OH)2 |
| Гидроксид меди(II) | Cu(OH)2 |
| Гидроксид натрия | NaOH |
| Гидроксид неодима | Nd(OH)3 |
| Гидроксид никеля(II) | Ni(OH)2 |
| Гидроксид цезия | CsOH |
| Гидроксид цинка | Zn(OH)2 |
| Гидроксид циркония | Zr(OH)4 |
| Гидроксил | OH− |
| Гидроксиламин | NH2OH |
| Гидроксоний | H3O |
| Гидросульфат | HSO4− |
| Гидросульфат лития | LiHSO4 |
| Гидросульфид аммония | NH4HS |
| Гидросульфит | HSO3− |
| Гидрофосфат | HPO42− |
| Гидрофосфат цезия | Cs2HPO4 |
| Гидрохинон | C6H6O2 |
| Гиллеспит | BaFeSi4O10 |
| Гипофосфит кальция | Ca(H2PO2)2 |
| Гипохлорит кальция | Ca(OCl)2 |
| Гистидин | C6H9N3O2 |
| Глиоксилат бутила | C6H10O3 |
| Глицин | H2NCH2COOH |
| Глицин Gly | C2H5NO2 |
| Глутамин | C5H10N2O3 |
| Глутаминовая кислота | C5H9NO4 |
| Глюкоза | C6H12O6 |
| Дезоксирибоза | C5H10O4 |
| Декан | C10H22 |
| Диборан | B2H6 |
| Дибромид серебра | Ag3Br2 |
| Дибромиодид индия(III) | InBr2I |
| Дигенит | Cu9S5 |
| Дигидрат бромата бария | Ba(BrO3)2·2H2O |
| Дигидрат бромата ртути(II) | Hg(BrO3)2 · 2H2O |
| Дигидрат селенита меди(II) | CuSeO3 · 2H2O |
| Дигидро- арсенат аммония | (NH4)H2AsO4 |
| Дигидро- фосфат | H2PO4− |
| Дииодид галлия | GaI2 |
| Диметил- гидразин | (CH3)2NNH2 |
| Диметиловый эфир | CH3OCH3 |
| Диметил- оксалат | (CH3)2C2O4 |
| Диметил- сульфид | CH3SCH3 |
| Диметил сульфоксид DMSO | C2H6OS |
| Диметил сульфонио- пропионат DMSP | (CH3)2S CH2CH2 COO− |
| Диоксид железа | FeO2 |
| Диоксид кремния | SiO2 |
| Диоксид мышьяка | AsO2 |
| Диоксид углерода | CO2 |
| Диоксид хлора | ClO2 |
| Диоксид циркония | ZrO2 |
| Диоксид- дибромид вольфрама(VI) | WO2Br2 |
| Диоксид- дииодид вольфрама(VI) | WO2I2 |
| Диоксид-дихлорид вольфрама(VI) | WO2Cl2 |
| Диоксид- фторид ксенона | XeO2F2 |
| Дисерная кислота | H2S2O7 |
| Дисиликат бария | BaSi2O5 |
| Дисульфид кобальта | CoS2 |
| Дителлурид алюминия | AlTe2 |
| Ди- трет- бутилпероксид DTBP | (CH3)3 COOC(CH3)3 |
| Дифосфид димышьяка | As2P2 |
| Дифтор- дихлорметан фреон-12 | CCl2F2 |
| Дифторид алюминия | AlF2 |
| Дифторид дикислорода, диоксидифторид | O2F2 |
| Дифторид кислорода | OF2 |
| Дифторид озона, триоксидифторид | O3F2 |
| Дифторид серебра | AgF2 |
| Дифторид- хлорид алюминия | AlClF2 |
| Дифтороксид алюминия | AlF2O |
| Дихлорид галлия | GaCl2 |
| Дихлорид серебра(II) | Ag2Cl2 |
| Дихлорметан | CH2Cl2 |
| Дихлоро- гексаоксид | Cl2O6 |
| Дихлорэтилен | C2H4Cl2 |
| Дихромат лития | Li2Cr2O7 |
| Дихромат серебра(I) | Ag2Cr2O7 |
| Дихромат цезия | Cs2Cr2O7 |
| Дицианоаурат (I) натрия | NaAu(CN)2 |
| Диэтиламин | (C2H5)2NH |
| Диэтиловый эфир | C4H10O |
| Диэтиловый эфир этоксиэтан | CH3CH2 OCH2CH3 |
| Додекан | C12H26 |
| Известняк | CaCO3 |
| Изоамилацетат | CH3 COO(CH2)2 CH(CH3)2 |
| Изолейцин | C6H13NO2 |
| Изопропиловый спирт пропанол-2 изопропанол | (CH3)2CHOH |
| Иод | I2 |
| Иодат | IO3− |
| Иодат кадмия | Cd(IO3)2 |
| Иодат кальция | Ca(IO3)2 |
| Иодат кобальта (II) | Co(IO3)2 |
| Иодат лития | LiIO3 |
| Иодат меди (I) | CuIO3 |
| Иодат меди (II) | Cu(IO3)2 |
| Иодат ртути (II) | Hg(IO3)2 |
| Иодат серебра | AgIO3 |
| Иодат цинка | Zn(IO3)2 |
| Иодид бария | BaI2 |
| Иодид бериллия | BeI2 |
| Иодид бора | BI3 |
| Иодид висмута (III) | BiI3 |
| Иодид вольфрама (II) | WI2 |
| Иодид вольфрама (IV) | WI4 |
| Иодид галлия | GaI3 |
| Иодид германия (IV) | GeI4 |
| Иодид золота (I) | AuI |
| Иодид золота (III) | AuI3 |
| Иодид индия (I) | InI |
| Иодид индия (II) | InI2 |
| Иодид индия (III) | In(IO3)3 |
| Иодид индия (III) | InI3 |
| Иодид иттербия (II) | YbI2 |
| Иодид иттербия (III) | YbI3 |
| Иодид кадмия | CdI2 |
| Иодид кальция | CaI2 |
| Иодид кобальта(II) | CoI2 |
| Иодид магния | MgI2 |
| Иодид марганца (II) | MnI2 |
| Иодид меди(I) | CuI |
| Иодид мышьяка (III) | AsI3 |
| Иодид натрия | NaI |
| Иодид неодима (III) | NdI2 |
| Иодид никеля (II) | NiI2 |
| Иодид ниобия(V) | NbI5 |
| Иодид ртути (I) | Hg2I2 |
| Иодид ртути (II) | HgI2 |
| Иодид серебра (I) | AgI |
| Иодид тантана (V) | TaI5 |
| Иодид хрома (II) | CrI2 |
| Иодид хрома (III) | CrI3 |
| Иодид цезия | CsI |
| Иодид церия(II) | CeI2 |
| Иодид церия (III) | CeI3 |
| Иодид цинка | ZnI2 |
| Иодид циркония | ZrI4 |
| Иодметан метилиодид | CH3I |
| Иодноватая кислота | HIO3 |
| Иодоводород | HI |
| Ион аммония | NH4 |
| Ион озонида | O3− |
| Ион пероксида | O22− |
| Ион супероксида | O2− |
| Кадмиевая обманка | CdS |
| Кадмоселит | CdSe |
| Кальцит | CaCO3 |
| Каменная соль | NaCl |
| Камфора | C10H16O |
| Каприлат цинка | Zn(C8H15O2)2 |
| Карбамат аммония | NH4CO2NH2 |
| Карбид алюминия | Al4C3 |
| Карбид бария | BaC4 |
| Карбид бериллия | Be2C |
| Карбид бора | B4C |
| Карбид вольфрама | W2C |
| Карбид иттрия | YC2 |
| Карбид кальция | CaC2 |
| Карбид кремния | SiC |
| Карбид хрома(II) | Cr3C2 |
| Карбид церия | CeC |
| Карбид церия(III) | Ce2C3 |
| Карбид циркония | ZrC |
| Карбонат | CO32− |
| Карбонат бария | BaCO3 |
| Карбонат висмутила | (BiO)2CO3 |
| Карбонат кадмия | CdCO3 |
| Карбонат кальция | CaCO3 |
| Карбонат магния | MgCO3 |
| Карбонат марганца (II) | MnCO3 |
| Карбонат натрия | Na2CO3 |
| Карбонат серебра(I) | Ag2CO3 |
| Карбонат цезия | Cs2CO3 |
| Карбонат цинка | ZnCO3 |
| Карбонил вольфрама (VI) | W(CO)6 |
| Кварц | SiO2 |
| Кеатит | Li(AlSi2O6) |
| Кетен | CH2CO |
| Киноварь | HgS |
| Кислород | O2 |
| Ковеллин | CuS |
| Кремниевая кислота | H2SiO3 |
| Криолит | Na3AlF6 |
| Кубан | C8H8 |
| Кубанит | CuFe2S3 |
| Лейцин | C6H13NO2 |
| Лизин | C6H14N2O2 |
| Лимонная кислота | C6H8O7 |
| Линолевая кислота | C18H32O2 |
| Магнетит | FeO4 |
| Малахит | Cu2CO3(OH)2 |
| Малонат | C3H3O4− |
| Мальтоза | C12H22O11 |
| Манганат бария | BaMnO4 |
| Манганит | MnOOH |
| Медный купорос | [Cu(H2O)4] SO4 · H2O |
| Метаарсенит натрия | NaAsO2 |
| Метаванадат висмута (III) | Bi(VO3)5 |
| Метаванадат кальция | Ca(VO3)2 |
| Метаванадат магния | Mg(VO3)2 |
| Метаванадат меди(II) | Cu(VO3)2 |
| Метаванадат натрия | NaVO3 |
| Метаванадат никеля(II) | Ni(VO3)2 |
| Метаванадат цинка | Zn(VO3)2 |
| Метан природный газ | CH4 |
| Метаниобат бария | BaNb2O6 |
| Метаниобат кальция | Ca(NbO3)2 |
| Метаниобат лития | Li2NbO3 |
| Метаниобат натрия | NaNbO3 |
| Метаниобат цезия | CsNbO3 |
| Метаниобат цинка | Zn(NbO3)2 |
| Метановая кислота | HCOOH |
| Метанол | CH3OH |
| Метасиликат бария | BaSiO3 |
| Метасиликат кадмия | CdSiO3 |
| Метасиликат кальция | CaSiO3 |
| Метасиликат лития | Li2SiO3 |
| Метасиликат магния | MgSiO3 |
| Метасиликат меди(II) | CuSiO3 |
| Метасиликат цезия | Cs2SiO3 |
| Метатанталат кадмия | Cd(TaO3)2 |
| Метатанталат натрия | NaTaO3 |
| Метатанталат цинка | Zn(TaO3)2 |
| Метатитанат лития | Li2TiO3 |
| Метатитанат магния | MgTiO3 |
| Метатитанат натрия | Na2TiO3 |
| Метатитанат никеля(II) | NiTiO3 |
| Метатитанат цезия | CsTaO3 |
| Метатитанат цинка | ZnTiO3 |
| Метафосфат бария | Ba(PO3)2 |
| Метацирконат кадмия | CdZrO3 |
| Метацирконат лития | Li2ZrO3 |
| Метацирконат марганца(II) | MnZrO3 |
| Метацирконат натрия | Na2ZrO3 |
| Метацирконат цинка | ZnZrO3 |
| Метилмеркаптан | CH3SH |
| Метионин | C5H11NO2S |
| Молибдат бария | BaMoO4 |
| Молибдат висмута (III) | Bi2(MoO4)3 |
| Молибдат кадмия | CdMoO4 |
| Молибдат кальция | CaMoO4 |
| Молибдат кобальта(II) | CoMoO4 |
| Молибдат магния | MgMoO4 |
| Молибдат меди(II) | CuMoO4 |
| Молибдат серебра | Ag2MoO4 |
| Молибдат цезия | Cs2MoO4 |
| Молочная кислота | HC3H5O3 |
| Монобромид алюминия | AlBr |
| Моногидрат бензоата ртути (II) | Hg(C7H5O2)2 · H2O |
| Моногидрат бромата бария | Ba(BrO3)2 · H2O |
| Моногидрат нитрата ртути (II) | Hg(NO3)2 · H2O |
| Моногидрат сульфата индия (III) | In2(SO4)3 · H2O |
| Моноиодид алюминия | AlI |
| Монооксид алюминия | AlO |
| Монооксид мышьяка | AsO |
| Монооксид углерода угарный газ | CO |
| Монотеллурид алюминия | AlTe |
| Монофторид алюминия | AlF |
| Монохлорид алюминия | AlCl |
| Мочевина | NH2CONH2 |
| Мочевина | (NH2)2CO |
| Мрамор | CaCO3 |
| Муллит | Al6O13Si2 |
| Муравьиная кислота | HCOOH |
| Мышьяковая кислота | H3AsO4 |
| Натрия гипохлорит | NaOCl |
| Нафталин | C10H8 |
| Негашёная известь | CaO |
| Никотиновая кислота | C5H4NCOOH |
| Ниобат бария | Ba(NbO3)2 |
| Ниобат дибария- натрия | Ba2Na(NbO3)5 |
| Ниобат кадмия | Cd2Nb2O7 |
| Ниобат меди (II) | Cu(NbO3)2 |
| Нитрат | NO3− |
| Нитрат алюминия | Al(NO3)3 |
| Нитрат аммония | NH4NO3 |
| Нитрат аммония-церия(IV) | NH4Ce(NO3)5 |
| Нитрат бария | Ba(NO3)2 |
| Нитрат гуанидиния | C(NH2)3NO3 |
| Нитрат кадмия | Cd(NO3)2 |
| Нитрат кальция | Ca(NO3)2 |
| Нитрат кобальта (II) | Co(NO3)2 |
| Нитрат кобальта (III) | Co(NO3)3 |
| Нитрат лития | LiNO3 |
| Нитрат магния | Mg(NO3)2 |
| Нитрат марганца (II) | Mn(NO3)2 |
| Нитрат меди (II) | Cu(NO3)2 |
| Нитрат натрия | NaNO3 |
| Нитрат серебра(I) | AgNO3 |
| Нитрат хрома(III) | Cr(NO3)3 |
| Нитрат цезия | CsNO3 |
| Нитрат цинка | Zn(NO3)2 |
| Нитрид алюминия | AlN |
| Нитрид аммония | (NH4)3N |
| Нитрид бария | Ba3N2 |
| Нитрид бериллия | Be3N2 |
| Нитрид бора | BN |
| Нитрид галлия | GaN |
| Нитрид кальция | Ca3N2 |
| Нитрид церия | CeN |
| Нитрид цинка | Zn3N2 |
| Нитрид циркония | ZrN |
| Нитрит | NO2− |
| Нитрит бария | Ba(NO2)2 |
| Нитрит кальция | Ca(NO2)2 |
| Нитрит цинка | Zn(NO2)2 |
| Нитроглицерин | C3H5(NO3)3 |
| Нонадекан | C19H40 |
| Нонан | C9H20 |
| Одид германия(II) | GeI2 |
| Озон | O3 |
| Окись алюминия | AlO2 |
| Оксалат | C2O42− |
| Оксалат бария | BaC2O4 |
| Оксалат кадмия | CdC2O4 |
| Оксалат кальция | CaC2O4 |
| Оксалат кобальта (II) | CoC2O4 |
| Оксалат магния | MgC2O4 |
| Оксалат меди (II) | CuC2O4 |
| Оксалат натрия | Na2C2O4 |
| Оксалат серебра | Ag2C2O4 |
| Оксалат цезия | Cs2C2O4 |
| Оксид азота (I) | N2O |
| Оксид азота (II) | NO |
| Оксид азота (III) | N2O3 |
| Оксид азота (IV) | NO2 |
| Оксид азота (IV) | N2O4 |
| Оксид азота (V) | N2O5 |
| Оксид алюминия | Al2O3 |
| Оксид алюминия (I) | Al2O |
| Оксид алюминия (II) | Al2O2 |
| Оксид алюминия-кремния | AlOSi |
| Оксид алюминия- магния | Al2MgO4 |
| Оксид бария | BaO |
| Оксид бериллия- алюминия | Al2BeO4 |
| Оксид бериллия- алюминия | Al6BeO10 |
| Оксид берилллия бромеллит | BeO |
| Оксид бора | B2O3 |
| Оксид ванадия (III) | V2O3 |
| Оксид висмута (III) | Bi2O3 |
| Оксид вольфрама(IV) | WO2 |
| Оксид вольфрама (VI) | WO3 |
| Оксид галлия | Ga2O3 |
| Оксид германия (II) | GeO |
| Оксид германия (IV) | GeO2 |
| Оксид дейтерия | D2O |
| Оксид железа (III) никеля(II) | NiFe2O4 |
| Оксид золота (III) | Au2O3 |
| Оксид индия (III) | In2O3 |
| Оксид иттербия (III) | Yb2O3 |
| Оксид иттрия | Y2O3 |
| Оксид кадмия | CdO |
| Оксид кальция | CaO |
| Оксид кобальта(II) | CoO |
| Оксид кобальта (II) — алюминия | Al2CoO4 |
| Оксид магния | MgO |
| Оксид марганца (II) | MnO |
| Оксид марганца (III) | Mn2O3 |
| Оксид марганца (IV) | MnO2 |
| Оксид меди (II) | CuO |
| Оксид меди (II) — железа (II) | CuFe2O4 |
| Оксид молибдена (IV) | MoO2 |
| Оксид мышьяка (III) | As2O3 |
| Оксид мышьяка (V) | As2O5 |
| Оксид неодима (III) | Nd2O3 |
| Оксид никеля (II) | NiO |
| Оксид ниобия (III) | Nb2O3 |
| Оксид ртути (II) | HgO |
| Оксид серебра (I) | AgO |
| Оксид серебра (I) | Ag2O |
| Оксид титана (IV) | TiO2 |
| Оксид трития | T2O |
| Оксид урана- бария | BaU2O7 |
| Оксид хлора (III) | Cl2O3 |
| Оксид хлора (VI) | Cl2O6 |
| Оксид хлора (VII) | Cl2O7 |
| Оксид хрома (III) | Cr2O3 |
| Оксид хрома(IV) | CrO2 |
| Оксид хрома(VI) | CrO3 |
| Оксид цезия | Cs2O |
| Оксид церия (III) | Ce2O3 |
| Оксид церия (IV) | CeO2 |
| Оксид цинка | ZnO |
| Оксид-борид золота | AuBO |
| Оксид- тетрафторид ксенона | XeOF4 |
| Оксисульфат ванадия | VSO5 |
| Оксоборид алюминия | AlBO |
| Оксобромид мышьяка (III) | AsBrO |
| Оксоиодид висмута (III) | BiOI |
| Оксофторид алюминия | AlFO |
| Оксохлорид алюминия | AlClO |
| Оксохлорид висмута (III) | BiOCl |
| Оксохлорид мышьяка (III) | AsClO |
| Оксохлорид мышьяка(V) | AsCl3O |
| Октагидрат оксохлорида гафния (IV) | HfOCl2 · 8H2O |
| Октадекагидрат сульфата галлия | Ga2(SO4)3 · 18H2O |
| Октадекан | C18H38 |
| Октан | C8H18 |
| Ортоарсенат галлия | GaAsO4 |
| Ортоарсенат ртути (II) | Hg3(AsO4)2 |
| Ортобензо- хинон | C6H4O2 |
| Ортованадат бария | Ba3(VO4)2 |
| Ортованадат кальция | Ca3(VO4)2 |
| Ортованадат магния | Mg3(VO4)2 |
| Ортованадат натрия | Na3VO4 |
| Ортованадат хрома (III) | CrVO4 |
| Ортованадат цезия | Cs3VO4 |
| Ортовольфрамат висмута (III) | Bi2(WO4)3 |
| Ортовольфрамат лития | Li2WO4 |
| Ортовольфрамат никеля (II) | NiWO4 |
| Ортомолибдат лития | Li2MoO4 |
| Ортомолибдат марганца (II) | MnMoO4 |
| Ортомолибдат никеля(II) | NiMoO4 |
| Ортомолибдат цинка | ZnMoO4 |
| Ортосиликат кобальта(II) | Co2SiO4 |
| Ортосиликат лития | Li2SiO4 |
| Ортосиликат магния | Mg2SiO4 |
| Ортосиликат никеля(II) | Ni2SiO4 |
| Ортосиликат цинка | Zn2SiO4 |
| Ортосиликат циркония | ZrSiO4 |
| Ортофосфат бария | Ba3(PO4)2 |
| Ортофосфат бора | BPO4 |
| Ортофосфат висмута(III) | BiPO4 |
| Ортофосфат галлия | GaPO4 |
| Ортофосфат калия | К3РО4 |
| Ортофосфат меди (II) | Cu3(PO4)2 |
| Ортофосфат никеля(II) | Ni3(PO4)2 |
| Ортофосфат серебра | Ag3PO4 |
| Ортофосфат цезия | Cs3PO4 |
| Основной ацетат гафния(IV) | HfOH(C2H3O2)3 |
| Пантолактон | C6H10O3 |
| Парабензо- хинон | C6H4O2 |
| Пентагидрат нитрата висмута (III) | Bi(NO3)3·5H2O |
| Пентагидрат селената меди(II) | CuSeO4 · 5H2O |
| Пентадекан | C15H32 |
| Пентан | C5H12 |
| Пентаокси- дифторид | O5F2 |
| Пентафтор- бензоат | NaC6F5COO |
| Пентафтор- бензойная кислота | C6F5COOH |
| Пентафторид хлора | ClF5 |
| Пентоксид тетрамышьяка | As4O5 |
| Перекись водорода | H2O2 |
| Перксенат бария | Ba2XeO6 |
| Перксенат ион | XeO64− |
| Перксеноновая кислота | H4XeO6 |
| Перманганат бария | Ba(MnO4)2 |
| Перманганат серебра | AgMnO4 |
| Перовскит | CaTiO3 |
| Пероксид бария | BaO2 |
| Пероксид ванадия | V2O5 |
| Пероксид кальция | CaO2 |
| Пероксид натрия | Na2O2 |
| Пероксид цинка | ZnO2 |
| Пероксоди- серная кислота | H2S2O8 |
| Перхлорат аммония | NH4ClO4 |
| Перхлорат бария | Ba(ClO4)2 |
| Перхлорат кальция | Ca(ClO4)2 |
| Перхлорат кобальта(II) | Co(ClO4)2 |
| Перхлорат серебра | AgClO4 |
| Перхлорат хлора | ClOClO3 |
| Перхлорат цезия | CsClO4 |
| Пиридин | C5H5N |
| Пиридиний | HC5H5N |
| Пированадат бария | Ba2V2O7 |
| Пированадат натрия | Na4V2O7 |
| Пированадат- ион | V2O74− |
| Пирокатехин | C6H6O2 |
| Пирофосфат бария | Ba2P2O7 |
| Пирофосфат магния | Mg2P2O7 |
| Пирофосфат цинка | Zn2P2O7 |
| Плавиковая кислота | HF |
| Полутяжёлая вода | HDO |
| Пролин | C5H9NO2 |
| Пропан | C3H8 |
| Пропан | H3CCH2CH3 |
| Пропанамид | CH3CH2CONH2 |
| Пропанол-1 | CH3CH2CH2OH |
| Пропанол-1 пропанол-2 | C3H8O |
| Пропен | CH3CHCH2 |
| Пропиловый пируват | C6H10O3 |
| Пропин | CH3CCH |
| Пропионовая кислота | CH3CH2COOH |
| Резорцин | C6H6O2 |
| Рутил | TiO2 |
| Сахароза | C12H22O11 |
| Селенат бария | BaSeO4 |
| Селенат золота (III) | Au2(SeO4)3 |
| Селенат кальция | CaSeO4 |
| Селенат лития | Li2SeO4 |
| Селенат магния | MgSeO4 |
| Селенат натрия | Na2SeO4 |
| Селенат серебра | Ag2SeO4 |
| Селенат цезия | CsSeO4 |
| Селенид алюминия(I) | Al2Se |
| Селенид бария | BaSe |
| Селенид висмута (III) | Bi2Se3 |
| Селенид висмута (III) | Bi2Se3 |
| Селенид вольфрама (IV) | WSe2 |
| Селенид золота (III) | Au2Se3 |
| Селенид индия (III) | In2Se3 |
| Селенид кадмия | CdSe |
| Селенид кальция | CaSe |
| Селенид кобальта(II) | CoSe |
| Селенид магния | MgSe |
| Селенид меди(I) | Cu2Se |
| Селенид меди (II) | CuSe |
| Селенид мышьяка (I) | As2Se |
| Селенид мышьяка (III) | As2Se3 |
| Селенид мышьяка (V) | As2Se5 |
| Селенид никеля (II) | NiSe |
| Селенид ртути (II) | HgSe |
| Селенид хрома (III) | Cr2Se3 |
| Селенид цинка | ZnSe |
| Селенит бария | BaSeO3 |
| Селенит кадмия | CdSeO3 |
| Селенит кальция | CaSeO3 |
| Селенит кобальта (II) | CoSeO3 |
| Селенит лития | Li2SeO3 |
| Селенит магния | MgSeO3 |
| Селенит натрия | Na2SeO3 |
| Селенит ртути (II) | HgSeO3 |
| Селенит серебра | Ag2SeO3 |
| Селенит цинка | ZnSeO3 |
| Селеновая кислота | H2SeO4 |
| Серин | C3H7NO3 |
| Серная кислота | H2SO4 |
| Сернистая кислота | H2SO3 |
| Сероводород | H2S |
| Сероуглерод | CS2 |
| Силан | SiH4 |
| Силикат алюминия | Al2O5Si |
| Силикат алюминия | Al2O5Si |
| Силикат алюминия | Al2O7Si2 |
| Силицид бария | BaSi2 |
| Силицид хрома (II) | Cr3Si2 |
| Силицид церия | CeSi2 |
| Силицид циркония | ZrSi2 |
| Соляная кислота | HCl |
| Станнат бария | BaSn3 |
| Станнат кобальта (II) | Co2SnO4 |
| Станнат цинка | ZnSnO3 |
| Стеариновая кислота | CH3 (CH2)16COOH |
| Стеариновая кислота | C18H36O2 |
| Субфторид серебра | Ag2F |
| Сульфанилат натрия | NaNH2C6H4SO3 |
| Сульфаниловая кислота | NH2C6H4SO3H |
| Сульфат аммония | (NH4)2SO4 |
| Сульфат бария | BaSO4 |
| Сульфат бериллия | BeSO4 |
| Сульфат гафния (IV) | Hf(SO4)2 |
| Сульфат кадмия | CdSO4 |
| Сульфат кальция | CaSO4 |
| Сульфат кобальта (II) | Co2SO4 |
| Сульфат лития | Li2SO4 |
| Сульфат магния | MgSO4 |
| Сульфат меди(II) | CuSO4 |
| Сульфат натрия | Na2SO4 |
| Сульфат никеля | NiSO4 |
| Сульфат свинца (II) | PbSO4 |
| Сульфат серебра | Ag2SO4 |
| Сульфат хрома (III) | Cr2(SO4)3 |
| Сульфат цезия | Cs2SO4 |
| Сульфат церия (IV) | Ce(SO4)2 |
| Сульфат цинка | ZnSO4 |
| Сульфид алюминия | Al2S3 |
| Сульфид алюминия | Al2S3 |
| Сульфид алюминия (I) | Al2S |
| Сульфид бария | BaS |
| Сульфид бериллия | BeS |
| Сульфид бора | B2S3 |
| Сульфид висмута (III) | Bi2S3 |
| Сульфид вольфрама(IV) | WS2 |
| Сульфид вольфрама(VI) | WS3 |
| Сульфид галлия | Ga2S3 |
| Сульфид железа (II) | FeS |
| Сульфид железа-меди | CuFeS2 |
| Сульфид железа- меди | CuFe2S3 |
| Сульфид золота (I) | Au2S |
| Сульфид золота (III) | Au2S3 |
| Сульфид индия (II) | InS |
| Сульфид индия (III) | In2S3 |
| Сульфид иттербия (III) | Yb2S3 |
| Сульфид иттрия | Y2S3 |
| Сульфид кадмия | CdS |
| Сульфид кальция | CaS |
| Сульфид кобальта(II) | CoS |
| Сульфид кобальта (II) | Co2S3 |
| Сульфид магния | MgS |
| Сульфид марганца(II) | MnS |
| Сульфид меди | Cu9S5 |
| Сульфид меди (I) | Cu2S |
| Сульфид меди (II) | CuS |
| Сульфид молибдена (IV) | MoS2 |
| Сульфид мышьяка (V) | As2S5 |
| Сульфид натрия | Na2S |
| Сульфид никеля | NiS2 |
| Сульфид никеля (II) | NiS |
| Сульфид ртути (II) | HgS |
| Сульфид свинца | PbS |
| Сульфид серебра (I) | Ag2S |
| Сульфид хрома (III) | Cr2S3 |
| Сульфид цезия | Cs2S |
| Сульфид церия (II) | CeS |
| Сульфид церия (III) | Ce2S3 |
| Сульфид цинка | ZnS |
| Сульфид циркония | ZrS2 |
| Сульфид- арсенид никеля | NiAsS |
| Сульфин | H2CSO |
| Сульфит бария | BaSO3 |
| Сульфит кадмия | CdSO3 |
| Сульфит цезия | Cs2SO3 |
| Супероксид цезия | CsO2 |
| Сфалерит | ZnS |
| Танталат лития | LiTaO3 |
| Теллурат кадмия | CdTeO4 |
| Теллурат кальция | CaTeO4 |
| Теллурат лития | Li2TeO4 |
| Теллурат натрия | Na2TeO4 |
| Теллурат хрома (III) | Cr2(TeO4)3 |
| Теллурат цезия | Cs2TeO4 |
| Теллурат цинка | ZnTeO4 |
| Теллурид алюминия (I) | Al2Te |
| Теллурид висмута (III) | Bi2Te3 |
| Теллурид вольфрама (IV) | WTe2 |
| Теллурид галлия | Ga2Te3 |
| Теллурид галлия (II) | GaTe |
| Теллурид золота | AuTe |
| Теллурид индия (II) | InTe |
| Теллурид индия (III) | In2Te3 |
| Теллурид кадмия | CdTe |
| Теллурид кальция | CaTe |
| Теллурид кобальта (II) | CoTe |
| Теллурид марганца (II) | MnTe |
| Теллурид меди (I) | Cu2Te |
| Теллурид меди (II) | CuTe |
| Теллурид ртути (II) | HgTe |
| Теллурид серебра (I) | Ag2Te |
| Теллурид хрома (III) | Cr2Te3 |
| Теллурид цинка | ZnTe |
| Теллуристая кислота | H2TeO3 |
| Теллурит бария | BaTeO3 |
| Теллурит кальция | CaTeO3 |
| Теллурит лития | Li2TeO3 |
| Теллурит меди(II) | CuTeO3 |
| Теллурит натрия | Na2TeO3 |
| Теллурит ртути (II) | HgTeO3 |
| Теллурит цинка | ZnTeO3 |
| Теллуровая кислота | H6TeO6 |
| Теллуровисмутит | |
| Тетра- бромооксид вольфрама(VI) | WOBr4 |
| Тетра- гемигидрат нитрата индия (III) | In(NO3)3·4,5H2O |
| Тетра- гидрат нитрата кальция | Ca(NO3)2 · 4H2O |
| Тетра- гидрат перхлората ртути(I) | HgClO4 · 4H2O |
| Тетра- гидрат хлорида индия(III) | InCl3·4H2O |
| Тетра- гидрофуран | C4H8O |
| Тетрадекан | C14H30 |
| Тетраиодид димышьяка | As2I4 |
| Тетра- иодомеркурат бария | BaHgI4 |
| Тетра- карбонил никеля | Ni(CO)4 |
| Тетра- нитроборат (III) натрия | Na[B(NO3)4] |
| Тетра- оксид ксенона | XeO4 |
| Тетра- оксид тримышьяка | As3O4 |
| Тетра- оксидифторид | O4F2 |
| Тетра- сульфид димышьяка | As2S4 |
| Тетра- сульфид тетрамышьяка | As4S4 |
| Тетра- фенилгерман | (C6H5)4Ge |
| Тетра- фтороалюминат калия | AlF4K |
| Тетра- фтороалюминат лития | AlF4Li |
| Тетра- фторэтилен | C2F4 |
| Тетрахлорид углерода | CCl4 |
| Тетрахлорид циркония | ZrCl4 |
| Тетра- хлорметан | |
| Тетра- хлороалюминат калия | AlCl4K |
| Тетра- хлороалюминат натрия | AlCl4Na |
| Тетра- хлороалюминат рубидия | AlCl4Rb |
| Тетра- хлороалюминат цезия | AlCl4Cs |
| Тетра- хлорооксид вольфрама (VI) | WOCl4 |
| Тиамина гидрохлорид | HC12H17ON4SCl2 |
| Тиомолибдат натрия | Na2MoS4 |
| Тиосульфат бария | BaS2O3 |
| Тиосульфат натрия | Na2S2O3 |
| Тиоцианат аммоний-ртуть (II) | (NH4)2Hg(SCN)4 |
| Тиоцианат бария | Ba(SCN)2 |
| Тиоцианат железа | Fe(CNS)3 |
| Тиоцианат калия | KCNS |
| Тиоцианат меди (I) | CuSCN |
| Тиоцианат ртути (II) | Hg(SCN)2 |
| Тиоцианат серебра | AgSNC |
| Тиоцианат цезия | CsSCN |
| Тиоцианат цинка | Zn(SCN)2 |
| Тирозин | C9H11NO3 |
| Титанат бария | BaTiO3 |
| Титанат кадмия | CdTiO3 |
| Титанат кальция | CaTiO3 |
| Титанат кобальта(II) | CoTiO3 |
| Титанат меди(II) | CuTiO3 |
| Титанат стронция | SrTiO3 |
| Титанат цезия | Cs2TiO3 |
| Титанит кобальта(II) | Co2TiO4 |
| Титановая кислота | H2TiO3 |
| Толуол | C7H8 |
| Треонин | C4H9NO3 |
| Трет- бутиловый спирт | (CH3)3COH |
| Трет- бутилхлорид | (CH3)3CCl |
| Трибромид алюминия | AlBr3 |
| Трибромид мышьяка | AsBr3 |
| Трибромид серебра(III) | Ag3Br3 |
| Трибромид цезия | CsBr3 |
| Трибромооксид вольфрама(V) | WOBr3 |
| Тригидрат нитрата меди (II) | Cu(NO3)2 · 3H2O |
| Тригидрат перхлората ртути (II) | Hg(ClO4)2 · 3H2O |
| Тригидрат теллурата бария | BaTeO4·3H2O |
| Тридекан | C13H28 |
| Трииодид | I3− |
| Трииодид азота | NI3 |
| Трииодид алюминия | AlI3 |
| Трииодид серебра (III) | Ag3I3 |
| Трииодид цезия | CsI3 |
| Трикарбонато- кобальтат (III) натрия | Na3[Co(CO3)3] |
| Триоксид ксенона | XeO3 |
| Триоксид тетрамышьяка | As4O3 |
| Триоксофторид хлора | ClO3F |
| Триптофан | C11H12N2O2 |
| Трисульфид тетрамышьяка | As4S3 |
| Трифосфид мышьяка | AsP3 |
| Трифторид алюминия | AlF3 |
| Трифторид бора | BF3 |
| Трифторид хлора | ClF3 |
| Трихлорид алюминия | AlCl3 |
| Трихлорид мышьяка | AsCl3 |
| Трихлорид серебра (III) | Ag3Cl3 |
| Трихлорид серебра- меди | AgCl3Cu2 |
| Трихлорооксид вольфрама (V) | WOCl3 |
| Угольная кислота | H2CO3 |
| Уксусная кислота | C2H4O2 |
| Уксусная кислота этановая кислота | CH3COOH |
| Ундекан | C11H24 |
| Фенилаланин | C9H11NO2 |
| Фенол | C6H5OH |
| Флюорит | CaF2 |
| Формальдегид | CH2O |
| Формальдегид | H2CO |
| Формамид | HCONH2 |
| Формат марганца (II) | Mn(CHO2)2 |
| Формат натрия | NaHCOO |
| Формиат | CHO2− |
| Формиат | HCOO− |
| Формиат аммония | HCOONH4 |
| Формиат бария | Ba(CHO2)2 |
| Формиат бериллия | Be(CHO2)2 |
| Формиат кальция | Ca(CHO2)2 |
| Фосген | COCl2 |
| Фосфат индия (III) | InPO4 |
| Фосфат кадмия | Cd3(PO4)2 |
| Фосфат лантана (III) | LaPO4 |
| Фосфат хрома(III) | CrPO4 |
| Фосфат цинка | Zn3(PO4)2 |
| Фосфат циркония | Zr3(PO4)4 |
| Фосфид алюминия | AlP |
| Фосфид алюминия- галлия- индия | AlGaInP |
| Фосфид бора | BP |
| Фосфид индия | InP |
| Фосфид иттрия | YP |
| Фосфид кадмия | Cd3P2 |
| Фосфид кальция | Ca3P2 |
| Фосфид магния | Mg3P2 |
| Фосфид марганца (II) | Mn3P2 |
| Фосфид меди (I) | Cu3P |
| Фосфид мышьяка (III) | AsP |
| Фосфид мышьяка (III) | As3P |
| Фосфид цинка | Zn3P2 |
| Фосфид циркония | ZrP2 |
| Фосфорная кислота | H3PO4 |
| Фруктоза | C6H12O6 |
| Фталевая кислота | H2C8H4O4 |
| Фторид бария | BaF2 |
| Фторид бериллия | BeF2 |
| Фторид бора | B2F4 |
| Фторид висмута (III) | BiF3 |
| Фторид вольфрама (IV) | WF4 |
| Фторид вольфрама(V) | WF5 |
| Фторид вольфрама (VI) | WF6 |
| Фторид гафния (IV) | HfF4 |
| Фторид золота (III) | AuF3 |
| Фторид иттербия (II) | YbF2 |
| Фторид иттербия (III) | YbF3 |
| Фторид иттрия | YF3 |
| Фторид кадмия | CdF2 |
| Фторид калия | KF |
| Фторид кальция | CaF2 |
| Фторид кобальта (II) | CoF2 |
| Фторид кобальта (III) | CoF3 |
| Фторид ксенона (I) | XeF |
| Фторид ксенона (II) | XeF2 |
| Фторид ксенона (IV) | XeF4 |
| Фторид ксенона (VI) | XeF6 |
| Фторид лития | LiF |
| Фторид магния | MgF2 |
| Фторид марганца (II) | MnF2 |
| Фторид мышьяка (III) | AsF3 |
| Фторид мышьяка (V) | AsF5 |
| Фторид серебра (I) | AgF |
| Фторид урана (IV) | UF4 |
| Фторид урана (VI) | UF6 |
| Фторид хлора | ClF |
| Фторид хрома (II) | CrF2 |
| Фторид хрома (III) | CrF3 |
| Фторид хрома (IV) | CrF4 |
| Фторид хрома (V) | CrF5 |
| Фторид хрома (VI) | CrF6 |
| Фторид цезия | CsF |
| Фторид церия (III) | CeF3 |
| Фторид церия (IV) | CeF4 |
| Фторид цинка | ZnF2 |
| Фторид циркония | ZrF4 |
| Фторид- дихлорид алюминия | AlCl2F |
| Фторид- тетрахлорид мышьяка | AsCl4F |
| Фторид- хлорид алюминия | AlClF |
| Фторид- хлорид аргона | ArClF |
| Фторноватистая кислота | HOF |
| Фтороводород | HF |
| Фтортрихлор- метан фреон-11 | CFCl3 |
| Фульминат серебра | AgONC |
| Халькозит | Cu2S |
| Халькопирит | CuFeS2 |
| Хинин | C20H24O2N2 |
| Хинон | C6H4O2 |
| Хиолит | Al3F14Na5 |
| Хлор | Cl2 |
| Хлорат кальция | Ca(ClO3)2 |
| Хлорат магния | Mg(ClO3)2 |
| Хлорат серебра | AgClO3 |
| Хлорат цезия | CsClO3 |
| Хлорат цинка | Zn(ClO3)2 |
| Хлорид алюминия- калия | Al2Cl9K3 |
| Хлорид аммония | NH4Cl |
| Хлорид бария | BaCl2 |
| Хлорид бериллия | BeCl2 |
| Хлорид бора | BCl3 |
| Хлорид бора | B2Cl4 |
| Хлорид брома | BrCl |
| Хлорид ванадия (II) | VCl2 |
| Хлорид ванадия (III) | VCl3 |
| Хлорид висмута (III) | BiCl3 |
| Хлорид вольфрама (II) | WCl2 |
| Хлорид вольфрама (III) | WCl3 |
| Хлорид вольфрама (IV) | WCl4 |
| Хлорид вольфрама (V) | WCl5 |
| Хлорид вольфрама (VI) | WCl6 |
| Хлорид галлия | GaCl3 |
| Хлорид железа (II) | FeCl2 |
| Хлорид золота (I) | AuCl |
| Хлорид золота (III) | AuCl3 |
| Хлорид индия (I) | InCl |
| Хлорид индия (II) | InCl2 |
| Хлорид индия (III) | InCl3 |
| Хлорид иода (I) | ICl |
| Хлорид иода (III) | ICl3 |
| Хлорид иттербия (II) | YbCl2 |
| Хлорид иттербия (III) | YbCl3 |
| Хлорид иттрия | YCl3 |
| Хлорид кадмия | CdCl2 |
| Хлорид калия | KCl |
| Хлорид калия | KCl |
| Хлорид кальция | CaCl2 |
| Хлорид кобальта (II) | CoCl2 |
| Хлорид лантана (III) | LaCl3 |
| Хлорид магния | MgCl2 |
| Хлорид марганца (II) | MnCl2 |
| Хлорид меди(I) | CuCl |
| Хлорид меди (II) | CuCl2 |
| Хлорид молибдена (II) | MoCl2 |
| Хлорид молибдена (III) | MoCl3 |
| Хлорид молибдена (V) | MoCl5 |
| Хлорид натрия | NaCl |
| Хлорид неодима (II) | NdCl2 |
| Хлорид никеля (II) | NiCl2 |
| Хлорид ниобия (III) | NbCl3 |
| Хлорид ниобия (V) | NbCl5 |
| Хлорид нитрила | NO2Cl |
| Хлорид ртути (I) | Hg2Cl2 |
| Хлорид ртути (II) | HgCl2 |
| Хлорид серебра (I) | AgCl |
| Хлорид тантала (V) | TaCl5 |
| Хлорид хрома (II) | CrCl2 |
| Хлорид хрома (III) | CrCl3 |
| Хлорид хрома (IV) | CrCl4 |
| Хлорид цезия | CsCl |
| Хлорид церия (III) | CeCl3 |
| Хлорид цинка | ZnCl2 |
| Хлористая кислота | HClO2 |
| Хлористый алюминий | AlCl2 |
| Хлорметан метилхлорид | CH3Cl |
| Хлорная кислота | HClO4 |
| Хлорноватая кислота | HClO3 |
| Хлорноватистая кислота | HClO |
| Хлороводород | HCl |
| Хлороформ трихлорметан трихлорид метила | CHCl3 |
| Хлоруксусная кислота | CH2ClCOOH |
| Хромат аммония | (NH4)2CrO4 |
| Хромат бария | BaCrO4 |
| Хромат бария- калия | BaK2(CrO4)2 |
| Хромат кадмия | CdCrO4 |
| Хромат кобальта (II) | CoCrO4 |
| Хромат лития | Li2CrO4 |
| Хромат магния | MgCrO4 |
| Хромат цезия | Cs2CrO4 |
| Хромат (V) бария | Ba3(CrO4)2 |
| Хромат (VI) серебра (I) | Ag2CrO4 |
| Хромилхлорид | CrO2Cl2 |
| Хромит кобальта (II) | CoCr2O4 |
| Хромит цинка | ZnCr2O4 |
| Хромовая кислота | H2CrO4 |
| Цвиттер- ион | H3N CH2COO− |
| Церианит | CeO3 |
| Цианамид кальция | CaCN2 |
| Цианат | CNO− |
| Цианид | CN− |
| Цианид бария | Ba(CN)2 |
| Цианид золота (I) | AuCN |
| Цианид кадмия | Cd(CN)2 |
| Цианид калия | KCN |
| Цианид кальция | Ca(CN)2 |
| Цианид кобальта (II) | Co(CN)2 |
| Цианид кобальта (III) | Co(C2H3O2)3 |
| Цианид лития | LiCN |
| Цианид натрия | NaCN |
| Цианид серебра | AgCN |
| Цианид цезия | CsCN |
| Цианид цинка | Zn(CN)2 |
| Циановодород | HCN |
| Циануровая кислота | C3N3(OH)3 |
| Циануровый триазид | C3N12 |
| Циклобутан | C4H8 |
| Циклогексан | C6H12 |
| Цикло- пентадиенил- анион | C5H5− |
| Циклопентан | C5H10 |
| Циклопропан пропилен | C3H6 |
| Цинкат натрия | Na2ZnO2 |
| Циркон | ZrSiO4 |
| Цирконат бария | BaZrO3 |
| Цирконат- ион | ZrO32− |
| Цистеин Cys | C3H7NO2S |
| Цитрат | C6H5O73− |
| Цитрат висмута (III) | BiC6H5O7 |
| Цихлоро- тетраоксид | ClOClO3 |
| Частично тритированная вода | HTO |
| Щавелевая кислота | HOOCCOOH |
| Эйкозан | C20H42 |
| Эсколаит | Cr2O3 |
| Этан | C2H6 |
| Этанол | CH3CH2OH |
| Этанол этиловый спирт | C2H5OH |
| Этиламин | C2H5NH2 |
| Этилат | C2H5O− |
| Этилат лития | LiC2H5O |
| Этилен | C2H4 |
| Этиленгликоль | CH2OHCH2OH |
| Этилендиамин | NH2CH2CH2NH2 |
| Эфедрин | C10H15ON |
| Дисилицид циркония | ZrSi2 |
| Перхлорат калия | KClO4 |
| 1,1,2 — трифтор- трихлорэтан, Фреон — 113 | CFCl2CF2Cl |
| 1,3 — бутадиен | CH2CHCHCH2 |
| 2- броммасляная кислота 4- броммасляная кислота | C4H7BrO2 |
| 2- бутен | CH3CHCHCH3 |
| 2- гермауксусная кислота | GeH3COOH |
| 2- гидрокси- пропилакрилат | C6H10O3 |
| 2- метилпропан | C4H10 |
| 4- ацетилмасляная кислота | C6H10O3 |
Таблица всех химических формул различных соединений (вода, кислород, водород, спирт, кислота и прочие), применяемых в химических и физических процессах.


![{displaystyle {ce {2KMnO4 ->[t] K2MnO4 MnO2 O2 ^}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fa985cedcb06a74333be1dbf055f4b95e5b416e4)
![{displaystyle {ce {2H2O2 ->[MnO2] 2H2O O2 ^}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/39356fdea2f393003bf49298522c43c2aa66e358)

![{displaystyle {ce {2HgO ->[100{°}C] 2Hg O2 ^}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8ed83305529bb4aea427f4cd72a0f92c5fe51aef)












