- Почему связь между классами веществ считается генетической
- Все тесты
- Кислоты и их свойства
- Нахождение в природе
- Оксиды
- Онлайн урок: кислород по предмету химия 8 класс |
- Особенности протекания реакций в растворе
- Природный газ
- Родственные связи между металлами и неметаллами
- Соли и их свойства
- Состав растворов
- Теория электролитической диссоциации
- Химические свойства
Почему связь между классами веществ считается генетической
Чтобы разобраться в этом вопросе. Вспомним состав классов веществ, с которыми Вы познакомились на предыдущих занятиях.
Обратите внимание, что соли содержат в себе частицы как оснований (атомы металла), так и кислот (кислотных остатков). Если соль рассматривать как «венец» превращений, то давайте, попытаемся прийти к истокам. Всё начинается с простого, точнее металла и неметалла, как простых веществ.
Попробуем построить генетический ряд металлов, переходя от одного класса к другому.
Возьмём, к примеру, металлы кальций и медь, подставив их в цепочку уравнений.
Обратите внимание, что данные металлы отличаются своей реакционной способностью.
Получается, эта генетическая связь соединений присуща только для активных металлов, оксиды которых, реагируя с водой, дают продукт в виде щёлочи.
Для металлов, которые отличаются малой активностью, переход от вещества, находящегося в простом состоянии, к соли, происходит путём превращений.
Поскольку основные оксиды реагируют с металлами (более активными, чем металлы, которые входят в состав оксида), то эту схему можно сократить.
Аналогичным способом можно составить генетический ряд неметаллов, начиная от неметалла заканчивая солью или неметаллом.
Подставим в цепочку уравнений фосфор и кремний.
А возможны иные пути решения данных цепочек уравнений. Способы получения кислотных оксидов реализуются путём взаимодействия простых веществ с кислородом. А вот не с каждого оксида можно получить ему соответствующую кислоту, путём прибавления воды. Поскольку кремниевая кислота нерастворима в воде, то необходимо получить сначала соль, а потом уже и кислоту.
В данном решении предлагается добыть соль Na3PO4, взаимодействием основания и кислоты. Однако можно использовать и другие варианты, которые также будут верны.
Если объединить генетические ряды металлов и неметаллов, получим дружную семью неорганических соединений, где каждое вещество связано неразрывной нитью с другими классами. Таблица 1.
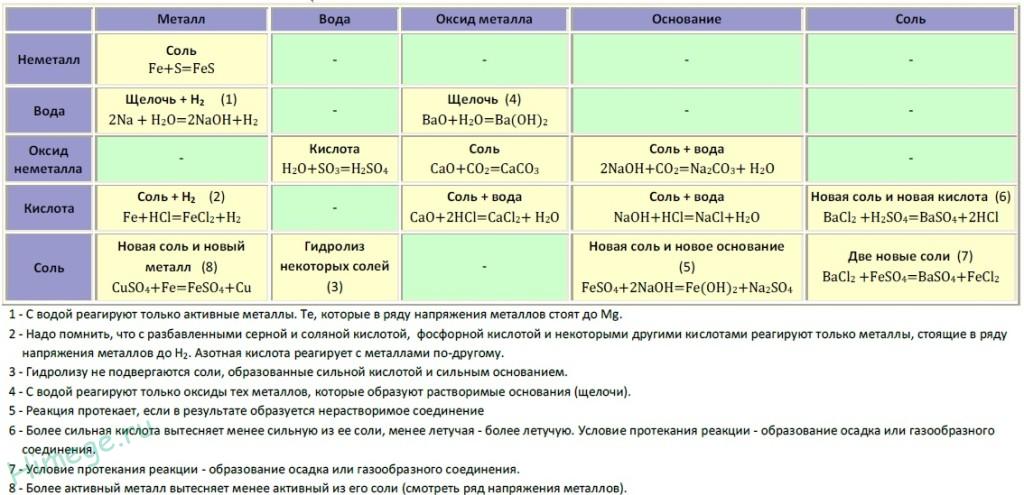
Источник
Данная таблица отображает, как реагируют между собой вещества и какие продукты возможны, вследствие реакции.
Промоделируем на примере: В вашем распоряжении имеются следующие вещества: оксид серы (VI), гидроксид бария, соляная кислота, карбонат кальция и железо. Ваша задача спрогнозировать, между какими соединениями возможна реакция и, записать, соответствующие уравнения реакций.
Подтвердив свои прогнозы молекулярно-ионными уравнениями в сокращённом и полном виде.
Все тесты
- Тест на темуАнализ стихотворения «Не с теми я, кто бросил землю» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Перемена» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Стихи о Петербурге» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Стихи к Блоку» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «Клеветникам России» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Завещание» Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «Стихи о Москве» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «Молитва» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «И. И. Пущину!» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «День и ночь» Ф. Тютчева5 вопросов
- Тест на темуАнализ стихотворения «Весна в лесу» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Журавли» Р. Гамзатова5 вопросов
- Тест на темуАнализ стихотворения «Люблю» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения «Когда на меня навалилась беда» К. Кулиева5 вопросов
- Тест на темуАнализ стихотворения «Гамлет» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Русь» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Ночь» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения К. Симонова «Ты помнишь, Алёша, дороги Смоленщины…»5 вопросов
- Тест на темуАнализ стихотворения Жуковского «Приход весны»5 вопросов
- Тест на темуАнализ стихотворения Анны Ахматовой «Сероглазый король»5 вопросов
- Тест на темуАнализ стихотворения «Июль – макушка лета…»5 вопросов
- Тест на темуАнализ стихотворения «Мелколесье. Степь и дали…» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Не позволяй душе лениться» Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «На дне моей жизни» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Нивы сжаты, рощи голы…» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Бабушкины сказки» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Снежок» Н. Некрасова1 вопрос
- Тест на темуАнализ стихотворения «По вечерам» Н. Рубцова5 вопросов
- Тест на темуАнализ стихотворения «Вчерашний день, часу в шестом…» Н. Некрасова5 вопросов
- Тест на темуАнализ стихотворения «Цветы последние милей…» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Я знаю, никакой моей вины…» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Я не ищу гармонии в природе»Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «Разбуди меня завтра рано» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Снега потемнеют синие» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Осень» Н. Карамзина5 вопросов
- Тест на темуАнализ стихотворения «Молитва» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Вечер» А. Фета5 вопросов
- Тест на темуАнализ стихотворения «Не жалею, не зову, не плачу» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Тучи» М. Лермонтова5 вопросов
- Тест на темуАнализ стихотворения «Книга» Г. Тукая5 вопросов
- Тест на темуАнализ стихотворения «Необычайное приключение, бывшее с Владимиром Маяковским летом на даче» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения «Деревня» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Летний вечер» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Я убит подо Ржевом» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Элегия» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Зимнее утро» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Троица» И. Бунина5 вопросов
- Тест на темуАнализ стихотворения «Бабушке» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «О весна без конца и краю» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Море» В. Жуковского5 вопросов
Кислоты и их свойства
Если посмотреть на состав этого класса соединений, то абсолютно во всех содержаться ионы водорода.
Следует заметить, что уравнение диссоциации кислот похожи, но отличие будет по кислотному остатку.Рассмотрим на примерах следующих многоосновных кислот –сернойН2SО4 и фосфорной Н3РО4.Характерной особенностью диссоциации многоосновных кислот – это ступенчатая диссоциация. Это означает, что ионы водорода будут отрываться не сразу все (2 или 3), а по одному.
Следствием этого является способность многоосновных кислот образовывать кислые соли.
Рассмотрим химические свойства кислот, за которые отвечают ионы Н .
Каким образом можно доказать, что неизвестное вещество относится к кислотам. Для этих целей создали индикаторы, которые как настоящие сыщики, ищут ионы Н или ОН- (в основаниях). Найдя их, они моментально меняют свою окраску. Кислая среда обусловлена наличием Н .
В реакциях обмена на их место могут стать только ионы металла, поэтому кислоты реагируют со следующими веществами.
Следственно, при реакции кислот с основными оксидами образуется соль и вода.
Атомы металла входят в состав оснований, в результате реакции нейтрализации, аналогично, как и основными оксидами, продуктом реакции является соль (может быть и кислая, и средняя) и вода.
Исходя из этого, кислая соль образуется, если «не хватает» атомов металла, чтобы обменять их на атомы водорода.
Взаимодействие кислот с солями возможно только в случае, когда соль образована слабой или летучей кислотой, а также в продукте будет газ или осадок.

Источник
Особенно хочется отметить взаимодействие металлов с кислотами, поскольку это будет реакция замещения со сменой степени окисления. Не все металлы способны реагировать с кислотами, а только те, что стоят в ряду напряжения до водорода и способны его вытеснить.
Действие концентрированных серной и азотной кислот на металлы отличается от их растворов, при этом происходит образование не водорода, а воды и других продуктов. Детально со свойствами азотной кислоты Вы познакомитесь чуть позже, однако сейчас необходимо запомнить, что при реакции с раствором этой кислоты водород не выделяется.
Нахождение в природе

Накопление O
2
в атмосфере Земли. Зелёный график — нижняя оценка уровня кислорода, красный — верхняя оценка.
1
. (3,85—2,45 млрд лет назад) — O
2
не производился
2
. (2,45—1,85 млрд лет назад) O
2
производился, но поглощался океаном и породами морского дна
3
. (1,85—0,85 млрд лет назад) O
2
выходит из океана, но расходуется при окислении горных пород на суше и при образовании озонового слоя
4
. (0,85—0,54 млрд лет назад) все горные породы на суше окислены, начинается накопление O
2
в атмосфере
5
. (0,54 млрд лет назад — по настоящее время) современный период, содержание O
2
в атмосфере стабилизировалось
Кислород — самый распространённый в земной коре элемент, на его долю (в составе различных соединений, главным образом силикатов) приходится около 47 % массы твёрдой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе). Более 1500 соединений земной коры в своём составе содержат кислород.
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе (около 1015 тонн). Однако до появления первых фотосинтезирующих микробов в архее 3,5 млрд лет назад, в атмосфере его практически не было. Свободный кислород в больших количествах начал появляться в палеопротерозое (3—2,3 млрд лет назад) в результате глобального изменения состава атмосферы (кислородной катастрофы).
Наличие большого количества растворённого и свободного кислорода в океанах и атмосфере привело к вымиранию большинства анаэробных организмов. Тем не менее, клеточное дыхание с помощью кислорода позволило аэробным организмам производить гораздо больше АТФ, чем анаэробным, сделав их доминирующими.
С начала кембрия 540 млн лет назад содержание кислорода колебалось от 15 % до 30 % по объёму. К концу каменноугольного периода (около 300 миллионов лет назад) его уровень достиг максимума в 35 % по объёму, который, возможно, способствовал большому размеру насекомых и земноводных в это время.
Основная часть кислорода на Земле выделяется фитопланктоном Мирового океана. Около 60 % кислорода от используемого живыми существами расходуется на процессы гниения и разложения, 80 % кислорода, производимого лесами, уходит на гниение и разложение растительности лесов.
Деятельность человека очень мало влияет на количество свободного кислорода в атмосфере. При нынешних темпах фотосинтеза понадобится около 2000 лет, чтобы восстановить весь кислород в атмосфере.
Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет около 25 %, по массовой доле — около 65 %.
В 2022 году датские учёные доказали, что свободный кислород входил в состав атмосферы уже 3,8 млрд лет назад.
Оксиды
В состав оксидов ВСЕГДА входит ТОЛЬКО два элемента, один из которых будет кислород. В этом классе соединений срабатывает правило, третий элемент лишний, он не запасной, его просто не должно быть. Второе правило, степень окисления кислорода равна -2. Из выше сказанного, определение оксидов будет звучать в следующем виде.
Оксиды в природе нас окружают повсюду, честно говоря, сложно представить нашу планету без двух веществ – это вода Н2О и песок SiO2.
Вы можете задаться вопросом, а что бывают другие бинарные соединения с кислородом, которые не будут относиться к оксидам.
Поранившись, Вы обрабатываете рану перекисью водорода Н2О2. Или для примера соединение с фтором OF2. Данные вещества вписываются в определение, так как состоят из 2 элементов и присутствует кислород. Но давайте определим степени окисления элементов.
Данные соединения не относятся к оксидам, так как степень окисления кислорода не равна -2.
Кислород, реагируя с простыми, а также сложными веществами образует оксиды. При составлении уравнения реакции, важно помнить, что элементу О свойственна валентность II (степень окисления -2), а также не забываем о коэффициентах. Если не помните, какую высшую валентность имеет элемент, советуем Вам воспользоваться периодической системой, где можете найти формулу высшего оксида.
Рассмотрим на примере следующих веществ кальций Са, мышьяк As и алюминий Al.
Подобно простым веществам реагируют с кислородом сложные, только в продукте будет два оксида. Помните детский стишок, а синички взяли спички, море синее зажгли, а «зажечь» можно Чёрное море, в котором содержится большое количество сероводорода H2S. Очевидцы землетрясения, которое произошло в 1927 году, утверждают, что море горело.
Чтобы дать название оксиду вспомним падежи, а именно родительный, который отвечает на вопросы: Кого? Чего? Если элемент имеет переменную валентность в скобках её необходимо указать.
Классификация оксидов строится на основе степени окисления элемента, входящего в его состав.
Реакции оксидов с водой определяют их характер. Но как составить уравнение реакции, а тем более определить состав веществ, строение которых Вам ещё не известно. Здесь приходит очень простое правило, необходимо учитывать, что эта реакция относиться к типу соединения, при которой степень окисления элементов не меняется.
Возьмём основный оксид, степень окисления входящего элемента 1, 2(т.е. элемент одно- или двухвалентен). Этими элементами будут металлы. Если к этим веществам прибавить воду, то образуется новый класс соединений – основания, состава Ме(ОН)n, где n равно 1, 2 или 3, что численно отвечает степени окисления металла, гидроксильная группа ОН- имеет заряд –(минус), что отвечает валентности I.При составлении уравнений не забываем о расстановке коэффициентов.
Аналогично реагируют с водой и кислотные оксиды, только продуктом будет кислота, состава НхЭОу. Как и в предыдущем случае, степень окисления не меняется, тип реакции — соединение. Чтобы составить продукт реакции, ставим водород на первое место, затем элемент и кислород.
Особо следует выделить оксиды неметаллов в степени окисления 1 или 2, их относят к несолеобразующим. Это означает, что они не реагируют с водой, и не образуют кислоты либо основания. К ним относят CO, N2O, NO.
Чтобы определить будет ли оксид реагировать с водой или нет, необходимо обратиться в таблицу растворимости. Если полученное вещество растворимо в воде, то реакция происходит.
Золотую середину занимают амфотерные оксиды. Им могут соответствовать как основания, так и кислоты, но с водой они не реагируют. Они образованные металлами в степени окисления 2 или 3, иногда 4. Формулы этих веществ необходимо запомнить.
Онлайн урок: кислород по предмету химия 8 класс |
Кислород – самый распространенный на Земле химический элемент:
земная кора содержит 47% кислорода
мировой океан состоит из кислорода на 85%
Кроме этого, кислород – основной участник обмена веществ в живых организмах – дыхания и фотосинтеза.
В таблице приведены основные сведения о кислороде.
Химический элемент | Простое вещество |
Название «Oxygenium» произошло от двух слов, в переводе «рождающий кислоты» Химический знак – О Атомный номер – 8 Расположение в периодической системе – 2 период, VI группа Типичный неметалл (сильный окислитель) Атомная масса – 16 а. е. м. Валентность – 2 Степени окисления – –2; 0; 1; 2 | Химическая формула – O2 Молекулярная масса – 32 а. е. м. Бесцветный газ без запаха; светло-голубая жидкость; синие кристаллы Температура кипения – –183 °С Температура плавления – –218 °С |
В жидком состоянии кислород имеет голубой цвет, поэтому на всех формулах мы его будем обозначать голубым!

Изучением кислорода занимались несколько учёных примерно в одно и то же время.
Официально первооткрывателем кислорода считается англичанин Джозеф Пристли (1774 год).
Однако установлен факт, что в свое время Леонардо да Винчи изучал химию кислорода, не подозревая тогда, что он является элементом.
Название «кислород» в русский язык ввёл Михаил Ломоносов, который также ввёл в употребление термин «кислота», который в те времена обозначал оксид – соединение элемента с кислородом.
Поэтому истинное значение названия «кислород» переводится как «рождающий оксиды». Некоторое время в России кислород называли «кислотвор».
Химический элемент кислород образует два простых вещества: кислород (O2) и озон (O3).
Кислород активно участвует в обмене веществ, именно ему обязана наша планета возникновением на ней жизни.
Атмосфера содержит 21 % кислорода.
Считается, что несколько сотен миллионов лет назад концентрация кислорода в атмосфере была почти в 2 раза выше – около 40%.
Количество кислорода в воздухе ниже 8% является угрозой для жизни человека.
В отличие от кислорода, озон даже в газообразном состоянии имеет голубой цвет, в жидком – насыщенный фиолетовый, в твёрдом – почти чёрный.
Озон (O3) образуется из кислорода при воздействии ионизирующих излучений: радиации или жестких ультрафиолетовых лучей (это свойство кислорода было открыто в 1899 году учеными Пьером и Марией Кюри).
Он образуется в атмосфере под воздействием разрядов молнии, а также при работе бытовой техники, например, лазерных принтеров.
При этом вы можете чувствовать характерный запах – это и есть запах озона.
Слово «озон» с греческого языка так и переводится: «пахну».
Озон также способен в некоторой степени задерживать ультрафиолетовые лучи. Это его свойство является одним из факторов существования жизни на Земле.
Кислород и озон являются парамагнетиками – это значит, что они притягиваются к магниту.
Это заметно при проведении опытов с жидкими кислородом и озоном.
Особенности протекания реакций в растворе
Химические реакции, в отличие от физических, характеризуются образованием новых веществ. Судить об их получении, мы можем, наблюдая изменение окраски, либо выделение газа или осадка.
Вспомним, что происходит с веществом, когда оно попадает в воду. Оно распадается на ионы. Тем не менее, этот процесс характерен не для всех веществ, а только для сильных электролитов, к которым относятся растворимые соли и кислоты, а также щёлочи.
Также необходимо вспомнить, какие реакции относятся к типу обмена.
Судить произошла реакция или нет, мы можем, если будет выполняться хотя бы одно из условий.
Условия протекания реакций между ионами сложных веществ.
Рассмотрим подробно каждое условие и составим алгоритм написания уравнений.
Выпадение осадка является подтверждением того, мы визуально видим, что реакция произошла. Составим уравнение между щёлочью – гидроксидом калия и солью – сульфатом меди (II). Запишем молекулярное уравнение.
Выполняя данный опыт, Вы могли бы наблюдать образование осадка голубого цвета.
Чтобы понять, какое вещество выпало в осадок, воспользуемся таблицей растворимости, а также составим полное ионно-молекулярное уравнение, которое отображает все частицы, находящиеся в растворе, с учётом коэффициентов.
Таким образом, KOH, K2SO4 и CuSO4 – это сильные электролиты, которые запишем в ионном виде. Cu(OH)2 – нерастворимое вещество, будет в молекулярном виде со стрелкой ↓. Также обращаем внимание, что перед щёлочью КОН находится коэффициент 2. Значит, образуется по два моля ионов К и ОН−.
При написании уравнений реакций, не забываем о законе сохранения вещества. Поэтому количество атомов, а также ионов, до реакции и после должны быть равны.
Следует отметить, что в полном ионно-молекулярном уравнении, слева и справа, имеются одинаковые частицы, их можно сократить.
Эти ионы при взаимодействии не образуют вещества, поэтому находятся в растворе в свободном виде как K и SO4−2.
Сокращённая реакция ионного обмена отображает суть химического процесса, а именно, между какими частицами происходит реакция.
Следственно, Cu(OH)2 будет осадком в растворе состоящем из ионов SO42−и К .
Вторым из условий является выделение газа. Эту реакцию Вы наблюдаете, когда гасите соду кислотой, не важно, какой уксусной, лимонной, яблочной, или же при добавлении к ней кефира, результат будет один и тот же, образование пузырьков углекислого газа.
Возникает закономерный вопрос, в уравнении отсутствует газ, однако раствор «шипит». Чтобы разобраться в этой проблеме, следует вспомнить, что угольная кислота относится к слабым электролитам и происходит выделение углекислого газа, а также образование молекулы воды. Поэтому полное молекулярно-ионное уравнение приобретает вид.
После сокращение одинаковых частиц левой и правой части, получаем сокращённое ионное уравнение.
Именно по причине наличия ионов водорода, сода «шипит» во всех кислотах.
И к третьему условию относится образование слабого электролита, зачастую это молекула воды, однако могут получаться и другие вещества. Ярким примером является реакция нейтрализации.
Почему этот тип реакции носит такое название? Рассмотрим на примере взаимодействия оснований КОН и Cu(OH)2 с раствором соляной кислоты.
В каждом случае происходит образование воды. В случае нерастворимых оснований, реакция идёт с образованием растворимой соли.
Уравнение реакции нейтрализации показывает, как два противоположных по свойствам класса неорганических соединений, отдавая по своей частице (Н и ОН-), образуют нейтральное вещество Н2О.
Природный газ
Основным компонентом этого природного ресурса является метан. В незначительном количестве содержит этан, пропан, бутан, а также азот, углекислый газ и сероводород. Без углеводородов не было бы и природного газа. Его залежи образовываются в донных отложениях при анаэробном разложении останков животного и растительного происхождения.
Газ имеет превосходство перед нефтью по эффективности использования, простоте добычи и экономичности. Добыча заключается в бурении скважин на всей площади месторождения. Поскольку газ в чистом виде в природе встречается крайне редко, для отделения его от примесей породы или других химических соединений рядом с местом добычи разворачиваются перерабатывающие комплексы.
Значительно экономить на транспортировке позволяет то, что сырье не требует такой очистки, как нефть, для перегонки по газопроводу. На химических заводах газ подвергается вторичной переработке, которая по принципу воздействия на природное сырье подразделяется на следующие виды:
- физико-энергетическая переработка;
- термохимическая;
- химико-каталитическая.
Первый метод предполагает сильное нагревание или охлаждение газа, за счет чего происходит его сжатие и разделение на компоненты. Обычно именно этот способ используется на местах газодобычи.
Суть второй технологии заключается в образовании непредельных углеводородов под воздействием высоких температур и давления.
Третий способ заключается в трансформации метана в синтезированный газ и последующая его переработка. Для этого применяют паровую конверсию. Этот вариант — самый быстрый и экономичный, так как высокая скорость протекания химической реакции избавляет от использования дополнительных катализаторов.
В основном продукты переработки природного газа используют как топливо.
Из прочих составляющих также получают смолы, формальдегиды, аммиак, различные кислоты, которые находят дальнейшее применение в химической, оборонной, пищевой промышленности, в текстильном производстве и многих других отраслях.
Родственные связи между металлами и неметаллами
Кислород является типичным представителем неметаллов. Он является достаточно сильным окислителем, перед которым может устоять только фтор. Получение основных оксидов происходит путём взаимодействия кислорода и металлов. Однако не все металлы охотно с ним реагируют.
Щелочные реагируют бурно, именно поэтому их хранение осуществляется под слоем керосина. Необходимо заметить, что щелочные металлы не образуют оксиды во время взаимодействия с О2. Их чрезвычайная активность позволяет получать только для их характерные продукты, это будут пероксиды и надпероксиды (за исключением лития, продукт Li2O).
А вот, чтобы менее активные металлы – железо или медь прореагировали, необходимо нагревание.
Получение кислотных оксидов происходит аналогично взаимодействием неметаллов с О2.
Металлы и неметаллы в химии рассматриваются как противоположности, которые, как заряды (положительные и отрицательные) имеют свойства притягиваться. Рассмотрим на примере металла кальций и неметалла углерод.
Соль СаСО3 имеет истоки от простых веществ Са и С, промежуточным звеном являются оксиды этих веществ, для которых свойственно реагировать между собой.
Вспомним с Вами один с основных постулатов химии, а именно, закон постоянства состава вещества.

Источник
Представим, что мы с Вами химики-первооткрыватели и нам предстоит сложная задача получить азотную кислоту, которая имеет важную роль в химической промышленности. Получение кислот возможно несколькими способами. Обращаясь к таблице 1, делаем вывод, что нам доступно несколько способов, а именно.
Взаимодействие кислот с солями приведёт нас к желаемому результату, однако не забывайте, что в продукте должны увидеть газ, осадок либо окрашивание.
Способы получения средних солей доказательно показывают связь между веществами. Снова выручалочкой нам послужит таблица 1. Наша задача получить вещество, без которого, полагаем, Вы не представляете своё существование, это соль NaCl. Используя данные, видим, что доступно для её получения 4 способа (Вы ищете, где продуктом является соль и применяете данные на свой пример).
Рассмотрим подробно каждый с них.
Способы получения солей отличаются, причиной этому является то, какую именно соль мы хотим получить, кислородсодержащей,сильной или слабой кислоты. К примеру, получение Na2SO4 будет отличаться от предыдущего примера с NaCl. Количество способов будет больше, так как это соль кислородсодержащей кислоты.
Здесь следуют отметить особенность щелочных, а также щелочно-земельных металлов, для которых свойственно взаимодействие с водой. По сути, идёт два параллельных процесса.
Полученная щёлочь реагирует с кислотой.
Способы получения солей аммония несколько отличаются, от солей металлов, тем, что аммиак непосредственно реагирует с кислотами (смотри урок химическая связь) с образованием донорно-акцепторных связей.
Гидроксид аммония имеет способность взаимодействовать с кислотами, с образованием необходимого продукта, не иначе как солей аммония.
Наверняка некоторые из Вас пугал вид заданий, который был цепочек уравнений. Обобщая всё выше сказанное, рассмотрим несколько примеров.
Пример 1.
Чтобы справится с данной задачей, проанализируем условие. Первое, что необходимо выделить – это количество уравнений (смотрим по стрелочкам, их 5). Второе определим исходное вещество – цинк, металл средней силы. Чтобы получить с него соль (не забываем о таблице 1), можно использовать 3 способа:
Выбор за Вами, одного из трёх уравнений. Переходим к следующей части цепочки ZnCl2 → Zn(OH)2. Здесь решением будет один вариант, это прибавление щёлочи.
Zn(OH)2 относится к нерастворимым основанием, поэтому при нагревании распадаются.
И наконец, итоговый продукт, металл. Его необходимо выделить из соли. Для этого необходимо взять металл, сила которого будет больше. Если эту информацию забыли, то освежить эти данные сможете с помощью урока Соли и их свойства.
Решение цепочек химических уравнений на первый взгляд кажется не посильной задачей, но если внимательно изучить свойства веществ, то они кажутся не такими уж и сложными.
Соли и их свойства
Этот класс веществ состоит из частичек кислоты – кислотного остатка и основания – катионов металла (либо иона аммония NH4 ). Диссоциация солей всегда идёт в одну стадию.
Если посмотреть на состав соли, то смело можно предположить, что их растворы будут нейтральными. Поскольку нет ионов, которые отвечают за реакцию среды. Однако на деле совсем не так. Лакмус в водном растворе солей может иметь как красную, так и синюю окраску, а также не изменять её.
Объяснением этого явления служит их взаимодействие с водой, которое имеет название гидролиз солей. Возьмём, к примеру, три пробирки, в которых содержатся растворы NaCl, ZnCl2 и Na2CO3. И в каждую добавим лакмус. Результаты эксперимента отображены на рисунке.
Запишем суть реакции соли с водой (молекулу Н2О распишем как НОН), с помощью ионно-молекулярных уравнений.
Сокращённое уравнение хорошо иллюстрирует, почему происходит изменение окраски индикатора. Теперь давайте разберёмся, какие соли подвергаются гидролизу.
Именно наличием ионов Н в растворе соли ZnCl2, а также группы ОН- в солевом растворе карбоната натрия, объясняется изменение окраски индикатора.

Источник
Рассмотрим взаимодействие металлов с солями. Чтобы понять принцип их взаимодействия, вспомним ряд активностей металлов.
Данный вид взаимодействия Вы можете наблюдать, выполнив дома опыт (не забываем о разрешении родителей). Вам понадобится раствор медного купороса и скрепка, либо гвоздь.
На поверхности гвоздя выделилась медь в чистом виде. Это окислительно-восстановительная реакция.
Более сильный металл, вытесняет слабый с раствора его соли. Если промоделировать обратную реакцию, а именно положить медную проволоку в раствор соли железа, то не будет никакого взаимодействия. «Силы» у меди не хватит, потеснить железо.
Взаимодействие солей между собой возможно только, если реагенты растворимы, а в продукте будет осадок.
Свойства солей, кислот и оснований, рассмотренных выше, можно объединить в схематическом виде.

Источник
Состав растворов

Источник
Чтобы приготовить сладкий напиток, необходимо взять сахар (растворимое вещество) и воду, которая будет играть роль растворителя. Масса раствора состоит из входящих в неё компонентов.
Растворённое вещество в данном случае сахар, поскольку его количество малое по отношению к воде.
Чтобы выразить, какую часть занимает растворённое вещество, введём понятие массовая концентрация или массовая доля.
Вернёмся к примеру с сахаром, массовая концентрация вещества будет составлять:
Чем выше масса растворённого вещества, тем более концентрированный раствор.
И снова вспомним наш сладкий раствор, допустим, вы утром ещё не очень проснулись, и вместо одной ложечки сахара, положили две. Как выйти из ситуации? Правильно, добавить воды. При этом доля растворённого вещества (сахара) уменьшается и образуется разбавленный раствор.
Разберёмся ещё с одним понятием – растворимость.

Источник
Обратите внимание, что указывается растворимость при определённой температуре. Возьмём два стакана объёмом 100 мл, в одном горячая, а во втором холодная вода. В оба добавим 3 столовых ложки сахара. Как вы думаете, где лучше и быстрее растворится сахар? Конечно там, где температура воды выше.
Существует зависимость между растворимостью и природой вещества.

Источник
Растворимость сахара при температуре 20 °C составляет 2000 г на 1л, раствор с такими данными будет насыщенным. При меньшем содержании растворённого вещества – ненасыщенным, большем – пересыщенным.

Источник
Химия не только удивительная наука, но она ещё и экспериментальная. С разрешения взрослых, Вы можете выполнить эксперимент. Вырастить замечательный «сад». Чтобы выполнить данный опыт, необходимо приготовить насыщенный раствор медного купороса или другой соли.
А как Вы думаете, может концентрированный раствор вещества быть ненасыщенным. Математические расчёты помогут дать ответ. Допустим, что растворили 200 г сахара в 100 г воды при температуре 20°C. Необходимо определить массовую концентрацию.
Как показывают расчёты, этот раствор будет концентрированным, однако является ненасыщенным.
Насыщенность и концентрация – это разные понятия.
Рассмотрим на примере сахара и гипса (CaSO4∙2H2O).
Поскольку большинство химических процессов происходит между растворами, важно знать, какое количество вещества там содержится. Содержание растворённого вещества можно выразить в массовых долях, а также с помощью ещё одного вида, которая носит название молярная концентрация.
Если массовая доля растворённого вещества показывает содержание вещества в растворе (%), то молярная концентрация указывает, сколько моль содержится в 1 литре раствора.
Промоделируем лабораторную ситуацию. Разбавленный раствор щёлочи был приготовлен путём растворения 10 г гидроксида натрия в 500 мл воды. Наша с Вами задача, определить массовую и молярную концентрации.
Теория электролитической диссоциации
Вернёмся к раствору, который состоит из хлорида натрия и воды. Если взять отдельно два этих вещества и каждое проверить на электропроводность, то результат будет отрицательный – они не проводят ток. Однако смесь этих веществ – раствор,будет электропроводный, т.е. являться электролитом.
Как Вам известно, с курса физики, электрический ток – это поток заряженных частиц. Однако, откуда они берутся? При растворении образуются ионы, которые и будут причиной электропроводности.
Т.е. диссоциацию хлорида натрия можно записать в следующем виде:
NaCl -> Na Cl-
Рассмотрим, как происходит диссоциация веществ с ионным типом связи. Данный тип локализуется в солях и основаниях.
Рассмотрим NaOH, Ba(OH)2, Fe(OH)3. Из них NaOHи Ва(ОН)2 относятся к щелочам (растворимые) основания и Fe(OH)3, который является нерастворимым. Если соединениене способно раствориться в воде, то такой раствор не будет проводить электрический ток. Молекула воды не может разрушить кристаллическую решётку, поэтому ионы не образуются и эти вещества неэлектролиты.
Раствор гидроксида натрия и гидроксида бария считаются электролитами, так как они диссоциируют на ионы. Следует обратить внимание, чтобы записать уравнение диссоциации оснований, запишем металл (указав его степень окисления) и гидроксильную группу, которая всегда имеет заряд минус 1. Число гидроксильных групп указываем коэффициентом.
Соли в воде распадаются на ионы металла и кислотного остатка. Как и в случае с основаниями, записываем: металл плюс кислотный остаток. Предварительно смотрим в таблицу растворимости, где можем уточнить заряд кислотного остатка и металла, а также проверить растворимость вещества.
Рассмотрим, как происходит диссоциация кислот, на примере соляной кислоты.
Для этого соединения характерна ковалентная полярная связь. Водород имеет положительный заряд, хлор – отрицательный.
Обычно в уравнении диссоциации записывают просто ион водорода Н , а не ион гидроксония Н3О .
Также следует обратить внимание, что молекула изначально нейтральное вещество. При написании уравнения, необходимо смотреть, чтобы количество положительных и отрицательных зарядов было равно.
Диссоциация электролитов имеет количественную характеристику.
Степень диссоциации зависит от следующих параметров:
Сила электролита определяется числом молекул, которые продиссоциировали. Чем выше это число, тем сильнее будет электролит.
Соответственно, электролитом является вещество с ионным или ковалентным типом связи. Его сила будет зависеть от природы вещества.
Обобщим всё выше сказанное, попробуем вывести положения теории электролитической диссоциации. Первый пункт можно записать в следующем виде.
Если же к электролитам относятся растворимые соли, кислоты и основания, рассмотрим, на какие частицы они будут диссоциировать.
Второй пункт даст ответ на вопрос, что является причиной диссоциации.
Если же через растворы электролитов пропустить электрический ток, то ионы принимают упорядоченное движение. Третий постулат звучит так.

Источник
Каждое вещество индивидуально, имеет определённый качественный и количественный состав, а также отличается строением. Именно по этой причине молекулы веществ в водном растворе могут распадаться полностью на ионы или частично. Выделим 4 пункт.
Поскольку в растворах слабых электролитов одновременно происходит два процесса распад молекул на ионы и их взаимодействие, то в уравнении принято ставить не знак равно или →, а две стрелки .
Каким образом мы можем прогнозировать силу электролитов. Если в случае солей и оснований достаточно посмотреть в таблицу растворимости, растворимые вещества это сильные электролиты, то в случае кислородсодержащих кислот этого будет недостаточно. К примеру, угольная кислота Н2СО3 по данным таблицы растворимости, относится к растворимым веществам, однако она считается слабым электролитом.
Из этого следует, что серная кислота – это сильный электролит, сернистая кислота относится к слабым электролитам.
Химические свойства
Сильный окислитель, самый активный неметалл после фтора, образует бинарные соединения (оксиды) со всеми элементами, кроме гелия, неона, аргона. Наиболее распространённая степень окисления −2. Как правило, реакция окисления протекает с выделением тепла и ускоряется при повышении температуры (см. Горение). Пример реакций, протекающих при комнатной температуре:
- 4Li O2 → 2Li2O
- 2Sr O2 → 2SrO
Окисляет соединения, которые содержат элементы с не максимальной степенью окисления:
- 2NO O2 → 2NO2↑
Окисляет большинство органических соединений в реакциях горения:
- 2C6H6 15O2 → 12CO2 6H2O
- CH3CH2OH 3O2 → 2CO2 3H2O
При определённых условиях можно провести мягкое окисление органического соединения:
- CH3CH2OH O2 → CH3COOH H2O
Кислород реагирует непосредственно (при нормальных условиях, при нагревании и/или в присутствии катализаторов) со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета.
Кислород образует пероксиды со степенью окисления атома кислорода, формально равной −1.
- 2Na O2 → Na2O2
- 2BaO O2 → 2BaO2
- H2 O2 → H2O2
- Na2O2 O2 → 2NaO2
- K O2 → KO2
- 3KOH 3O3 → 2KO3 KOH ∗ H2O 2O2↑
- PtF6 O2 → O2PtF6
В этой реакции, кислород проявляет восстановительные свойства.

