- Библиотеки и музеи
- Вид катализа
- Другие имена
- Другие свойства
- Каталитическое окисление этилена
- Каталитическое окисление этилена кислородом
- Медицинские приложения
- Молекулярный вес
- Огонь
- Плотность
- Производство
- Промышленное применение
- Растворимость
- Сельское хозяйство и пищевая промышленность
- Состав
- Температура самовоспламенения
- Точка возгорания
- Физическое состояние
- Химизм процесса
- Этиленоксид • большая российская энциклопедия — электронная версия
Библиотеки и музеи
В этих местах оксид этилена используется для борьбы с вредителями, такими как грибы и насекомые. Однако это использование не так распространено и используется, когда другие альтернативы не эффективны.
Вид катализа
Окисление этилена в присутствии серебра, которое играет роль катализатора, относится к гетерогенному катализу.
Другие имена
— Оксирано.
— Эпоксиэтан.
Другие свойства
— Если он подвергается нагреванию или загрязнению, он может экзотермически полимеризоваться (выделяя большое количество тепла). Если внутри контейнера происходит полимеризация, он может сильно разорваться.
— Может реагировать с окислителями.
— Он чрезвычайно токсичен, канцероген и является хорошим генератором мутаций в клетках бактерий и млекопитающих.
Каталитическое окисление этилена

Для проведения реакции прямого окисления этилена было предложено большое число высокоактивных катализаторов. Почти все они содержат в качестве основного компонента серебро . Применяемые катализаторы можно разделить на две основные группы:
· сплошные серебряные катализаторы;
· активное серебро на носителе (трегерные катализаторы).
Катализаторы первой группы представляют собой металлическое серебро, которое обычно гранулируют и гранулы обрабатывают кислотами, что увеличивает поверхность катализатора и повышает его активность. Если катализатор предназначается для проведения процесса окисления этилена в псевдоожиженном слое, металлическое серебро измельчают до порошкообразного состоя-ния и формуют в виде таблеток или шариков.
Предложены также сплавные скелетные катализаторы; серебро сплавляют с кальцием, который извлекается затем уксусной кислотой. Недостатком сплошных скелетных катализаторов является их высокая стоимость из-за большого расхода серебра.
Трегерные катализаторы готовят нанесением активного серебра на носитель (окись алюминия, карборунд, силикагель, пемза). Для приготовления трегерного катализатора чаще всего пропитывают носитель растворами некоторых соединений серебра (например, водным раствором нитрата серебра) с последующим восстановле-нием до металлического серебра.
В настоящее время в промышленности используются только серебряные катализаторы, но в последние годы появились сообще-ния об окислении этилена в окись этилена в присутствии солей или окисей других металлов. Из них особого внимания заслуживает процесс получения окиси этилена в паровой фазе на катализато-ре, представляющем собой смесь и . Окисление эти-лена производилось кислородом при разрежении в интервале температур 400 — 600°С с 90 — 100 %-ным выходом окиси этилена.
В жидкой фазе окисление этилена протекает в среде дибутилфталата в присутствии окиси ртути. При этом образуется окись этилена, хотя и в меньшем количестве, чем в присутствии катализаторов, содержащих серебро. Окисление этилена в этих условиях осуществляется за счет восстановления окислов металлов.
Большое влияние на выход окиси этилена оказывает соотноше-ние вводимых в процесс воздуха и этилена. Максимальный выход получается при соотношении воздух : этилен от 7:1 до 8:1, что соответствует содержанию в газовой смеси 12 об. % этилена и 88 об. % воздуха. Однако такие смеси взрывоопасны и по-этому приходится проводить процесс в менее выгодных условиях — при концентрации этилена ниже нижнего предела взрываемости, который составляет 2,75 об. % этилена в смеси с возду-хом.
При получении окиси этилена можно использовать в качестве окислителя технический кислород. В этом случае желательно при-менять концентрированный этилен (98 %-ный и выше). В присут-ствии парафиновых углеводородов выход окиси этилена понижает-ся; при наличии в газе гомологов этилена в процессе окисление развиваются высокие температуры и затрудняется отвод выделяю-щегося тепла. Присутствие ацетилена в исходной газовой смеси недопустимо, так как с серебром он образует взрывчатый ацетеленид серебра. Если исходный этилен содержит ацетилен, то его удаляют путем промывки газа селективными растворителями (ацетоном, диметилформамидом) или гидрируют до этилена на никелевом катализаторе.
От соединений серы исходный газ очищают обычным методом — промывкой щелочью и водой.
При пропускании смеси этилена и воздуха над катализатором при 200 — 300єС одновременно протекают две реакции:

Обычно до окиси этилена окисляется не больше 55 — 60% эти-лена, а 40 — 45% его полностью сгорает до CО2 и Н2О.
В промышленных установках прямого окисления используются контактные аппараты с неподвижным или с псевдоожиженным слоем катализатора.
Реактор с неподвижным слоем катализатора, работающий под давлением до 21 атм., представляет собой кожухо-трубный аппарат, трубки которого заполнены зерненным катализатором. Так как окис-лы железа каталитически ускоряют реакцию полного окисления этилена, трубки изготавливают из хромоникелевых аустенитных сталей или из обычных углеродистых сталей и серебрят изнутри. Благодаря малому се-чению трубок реагирующие газы проходят по ним с большой ско-ростью. Таким образом, достигается повышенная теплоотдача от газа к стенкам трубок и сравнительно равномерное охлаждение контактной массы. Интенсивный отвод реакционного тепла в этом процессе весьма важен, так как при температуре свыше 300°С мо-жет происходить полное окисление этилена.
Окись этилена извлекают из контактных газов в скрубберах, орошаемых водой, затем отгоняют из водного раствора, осушают и конденсируют. Транспортируют окись этилена в жидком виде в стальных баллонах. Если целевым продуктом производства яв-ляется этиленгликоль, контактные газы промывают горячим 1%-ным раствором серной кислоты, в результате чего окись этилена гидратируется до этиленгликоля .
Изучен и разработан процесс получения окиси этилена катали-тическим окислением этилена в псевдоожиженном слое катализа-тора. Благодаря высокому коэффициенту теплоотдачи в псев-доожиженном слое катализатора (значительно большему, чем в аппаратах с неподвижным слоем катализатора) при окислении тре-буется меньшая поверхность теплообмена, а следовательно, и меньшие габариты реакционных аппаратов.

Рис. 2.2. Схема производства окиси этилена прямым окислением этилена в псевдоожиженном слое катализатора.
1) реактор первой ступени; 2, 6) холодильники; 3) абсорбер первой ступени; 4) компрессор; 5) реактор второй ступени; 7) абсорбер второй ступени; 8) теплообменник; 9) отпарная колонна; 10, 12) дефлегматоры; 11) ректификационная колонна; 13) кипятильник; 14) разделительная колонна.
В нижней части реакционного аппарата помещены трубы, охла-ждаемые высокотемпературным теплоносителем, циркулирующим в межтрубном пространстве. Над трубами расположены охлаждаю-щие элементы, а еще выше фильтры из пористой окиси алюми-ния. Равномерное распределение псевдоожиженного катализаторапо трубам реактора достигается благодаря тому, что аппарат за-полняют катализатором до уровня, значительно превышающего вы-соту труб (над трубной решеткой создается слой катализатора. Равномерность подачи этилена во все трубы автоматически регули-руется специальными приборами.
Для данного процесса требуется прочный катализатор, не тре-бующий регенерации или реактивации в течение длительного вре-мени и не подвергающийся заметному истиранию.
Процесс проводят под давлением в две ступени. Смесь этилена и воздуха нагнетается в контактный реактор 1 первой ступени, где до 50% этилена превращается в окись этилена. Продукты реакции охлаждаются в холодильнике 2, после чего в абсорбере 3 первой ступени из них извлекается окись этилена.
Часть непрореагировавших газов возвращают в реактор 1, а остальной газ подают в реактор 5 второй ступени. Общая степень превращения этилена во второй ступени окисления составляет 70%.
Из контактных газов после второй ступени окисления окись эти-лена извлекают водой в абсорбере 7 второй ступени. Из абсорбе-ров 3 и 7 водный раствор окиси этилена через теплообменник 8 направляют в отпарную колонну 9. Отгоняемая из этой ко-лонны паро-газовая смесь поступает через дефлегматор 10 на раз-деление в ректификационную колонну 11. Окончательная очистка окиси этилена от CO2 производится в колонне 14. Получаемый по этому способу продукт представляет собой 99,5%-ную окись этилена.
При прямом окислении расход этилена несколько выше, чем при хлоргидринном методе. Однако этот недостаток вполне окупается другими достоинствами метода прямого окисления, который следует считать весьма перспективным.
Каталитическое окисление этилена кислородом
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Медицинские приложения
Он используется в качестве стерилизующего агента для медицинского оборудования, такого как хирургические инструменты, иглы и инъекторы для подкожных инъекций или протезы.
Он также используется для стерилизации гемодиализных аппаратов, лабораторного оборудования, стоматологических инструментов, ветеринарных инструментов, термометров, хирургической одежды или оборудования для оказания первой помощи, среди прочего.

Несмотря на то, что существуют различные методы стерилизации медицинского оборудования, в некоторых случаях использование оксида этилена не может быть заменено никакими средствами.
Это касается стерилизации некоторых материалов, чувствительных к теплу и излучению, а также некоторых инструментов и устройств, требующих стерилизации на месте использования в больницах.
Молекулярный вес
44,05 г / моль.
Огонь
— При воздействии пламени или тепла существует опасность взрыва. При нагревании образуются опасные пары.
— Пар образует с воздухом взрывоопасные смеси в широком диапазоне концентраций.
— Избегайте работы с оборудованием, которое содержит металлы, такие как медь, серебро, ртуть, магний, алюминий или оксиды железа, а также избегайте таких агентов, как аммиак, окислители, органические кислоты или основания и другие. Все эти материалы могут ускорять полимеризацию и / или взрыв.
Плотность
Его плотность ниже, чем у воды, 0,882 при 10 ºC. В свою очередь, его пары тяжелее воздуха.
Производство
В промышленных масштабах его получают окислением этилена кислородом (O2) с воздуха. Скорость этой реакции увеличивается в присутствии металлического серебра (Ag) и воздействия температуры. Реакция показана ниже:
Ag, 250ºC
2 С2ЧАС4 O2 —-> 2C2ЧАС4ИЛИ
Этилен Этиленоксид
Промышленное применение
Он используется в качестве промежуточного звена в производстве других химикатов, которые, в свою очередь, используются при производстве полиэфирных волокон для одежды, обивки, ковров и подушек.
Оксид этилена производит этиленгликоль, который используется в антифризах автомобильных двигателей. Этиленгликоль также используется в производстве стекловолоконных и пластиковых упаковочных пленок.
Другие химические вещества, производимые из окиси этилена, включают неионные поверхностно-активные вещества, используемые в моющих средствах и рецептурах посуды.
Растворимость
Он растворим в воде, бензоле, ацетоне, этаноле и эфире. Смешивается с четыреххлористым углеродом.
Сельское хозяйство и пищевая промышленность
Он использовался как пестицид, фунгицид, фумигант, гербицид, инсектицид, родентицид и другие варианты. Значительно снижает популяцию бактерий и грибков в специях.
Однако из соображений безопасности и защиты окружающей среды использование окиси этилена для фумигации пищевых продуктов было запрещено в Европейском Союзе и в Соединенных Штатах.
Состав
Его молекулярная формула C2ЧАС4О. Он принадлежит к группе эпоксидов, являясь наиболее простыми и важными из них. Он имеет форму трехчленного кольца.
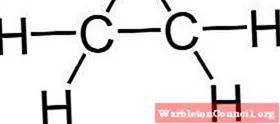
Из-за своей треугольной кольцевой структуры оксид этилена очень реакционноспособен, что связано с легкостью, с которой кольцо открывается. В среднем валентные углы составляют 60º, что ослабляет ваши связи. Молекула менее стабильна, чем у линейного эфира, и имеет тенденцию легко реагировать с другими химическими соединениями.
Температура самовоспламенения
428,9 ° С.
Точка возгорания
Менее 0ºF (-17,8ºC).
Физическое состояние
При комнатной температуре и атмосферном давлении это газ. При температуре ниже 10,6 ºC и при атмосферном давлении это жидкость. Ниже -111 ° C он твердый.
Химизм процесса
В настоящее время, в промышленности для синтеза оксида этилена наиболее широко применяется серебряный катализатор.
Реакция
CH2=CH2 1/2 O2 > C2H4O, (1)
сопровождается полным окислением этилена
CH2=CH2 3O2 > 2CO2 2H2O , (2)
При более высоких температурах проявляется реакция полного окисления окиси этилена
C2H4O 1/2 O2 > 2 CO2 2 H2O. (3)
Механизм окисления этилена до оксида этилена на серебряном контакте заключается в следующем. Серебро способно адсорбировать на своей поверхности кислород в сравнительно больших количествах. При этом адсорбция происходит без диссоциации или с диссоциацией молекулы, причем требуемые электроны поставляет металл и переводит адсорбированный кислород в состояние ион-радикала:
Ag O2 > Ag — O — ЇO? (4)
Ag — O — ЇO? Ag > 2 AgЇO? (5)
Сходный тип хемосорбции кислорода наблюдается на оксидных и солевых катализаторах, где сорбция происходит по иону переходного металла. Этилен сорбируется на окисленной поверхности катализатора вначале по ион-радикалу кислорода, а затем, взаимодействуя с ним, образует продукты окисления:
AgO ЇO? CH2=CH2 > AgOOCH2 — CH2? > AgЇO? C2H4O (6)
Продукты полного окисления образуются из этилена и ион-радикала:
6 AgЇO? CH2=CH2 > 2 CO2 2 H2O 6 Ag (7)
2 Ag O2 > 2 AgЇO? (8)
Для подавления реакции полного окисления этилена предложено добавлять в реакционную массу небольшие количества паров хлороводорода, дихлорэтана или диоксида углерода, которые несколько понижают каталитическую активность ион-радикала AgЇO? и тем самым, уменьшают образование CO2 и H2O.
Этиленоксид • большая российская энциклопедия — электронная версия
ЭТИЛЕНОКСИ́Д (оксиран, 1,2-эпоксиэтан), простейший представитель эпоксидов:
Бесцветный газ с характерным эфирным запахом; tкип 10,7 °C; хорошо растворяется в воде, спирте, эфире, углеводородах; горюч, смеси с воздухом (3–80% по объёму Э.) взрывоопасны. При нагревании до 300 °C устойчив, св. 400 °C в смеси с N2 изомеризуется в ацетальдегид или образует этилен (при избытке Э.); при окислении О2 в водном растворе AgNO3 образуется гликолевая кислота, при гидрировании над Ni – этанол. Для Э. характерны реакции с размыканием цикла, что используют для гидроксиэтилирования органич. соединений. Гидратация Э. в присутствии катализаторов приводит к этиленгликолю. При взаимодействии Э. с галогеноводородами образуются галогенгидрины; со спиртами при нагревании – целлозольвы, карбитолы или эфиры полигликолей. Э. легко реагирует с HCN в присутствии щелочей, образуя этиленциангидрин, при дегидратации которого получают акрилонитрил. Реакции Э. с органич. кислотами или их ангидридами приводят к моно- и диэфирам этиленгликоля; с альдегидами и кетонами – к циклич. ацетатам или кеталям. Э. взаимодействует с ароматич. углеводородами по реакции Фриделя – Крафтса. Циклоолигомеризацией Э. получают краун-эфиры. При димеризации Э. образуется 1,4-диоксан. Э. легко полимеризуется, с пропиленоксидом и полиэтилентерефталатом образует блоксополимеры.
Получают прямым окислением этилена кислородом (катализатор Ag; осн. метод), дегидрохлорированием этиленхлоргидрина, эпоксидированием этилена. Э. – один из важнейших продуктов основного органического синтеза. Применяется в произ-ве этиленгликоля, галогенгидринов, этаноламинов, диоксана, фенилэтанола, полиэтиленгликолей, неионогенных ПАВ, полиуретанов и др., как бактерицидное средство. Высокотоксичен, обладает канцерогенным и мутагенным действием.
