- Газовые законы. газовые смеси. задача 70 — задачи по химии
- Задача #13861: определите плотность смеси газов, состоящей из 8 г (условие) — студизба
- Задачи по физике
- Найти плотность ρ газовой смеси водорода и кислорода, если их массовые доли w1 и w2 равны соответственно 1/9 и 8/9. давление p смеси равно 100
- Относительная плотность по… задачи
- Относительная плотность вещества – отношение плотности вещества Б к плотности вещества А
- Примеры решенных задач по физике — контрольная 8(молекулярная физика, равновесное излучение, ядерные реакции)
- Срядняя плотность по водороду газовой смеси состоит из водорода и кислорода равна14,5.вычислите сколько объемных процентов водорода и кислорода содержится в смеси? —
Газовые законы. газовые смеси. задача 70 — задачи по химии
Средняя плотность по водороду газовой смеси состоящей из водорода и кислорода 12,5. Вычислите сколько процентов водорода и кислорода (по объему) содержит смесь.
Задача #13861: определите плотность смеси газов, состоящей из 8 г (условие) — студизба
Задачи по физике
Общий
вид уравнения колебаний:
(1)
Скорость
колебаний:
(2)
Максимальная
скорость:
(3)
В момент
когда скорость точки максимальна,
ее кинетическая энергия равна полной
энергии:
(4)
Ускорение
точки:
(5)
Максимальное
ускорение точки:
(6)
Ускорение
максимально, когда максимальна
сила, действующая на точку:
(7)
Делим
(4) на (7), получаем амплитуду колебаний:
(8)
Круговая
частота колебаний:
(9)
Подставляем
(8) и (9) в (1), получаем уравнение движения:
(м)
Ответ: .
Найти плотность ρ газовой смеси водорода и кислорода, если их массовые доли w1 и w2 равны соответственно 1/9 и 8/9. давление p смеси равно 100
готовое задание, попробуте поиск по другим похожим ключевым фразам из ее условия
| Решение задач → Задачи по физике с решениями Найти плотность ρ газовой смеси водорода и кислорода, если их массовые доли w1 и w2 равны соответственно 1/9 и 8/9. Давление p смеси равно 100 кПа, температура T=300 К.
|
Относительная плотность по… задачи
24-Фев-2022 | комментариев 26 | Лолита Окольнова
В ЕГЭ иногда встречаются задачи (часть С последнее задание), где в условии дана относительнаяплотность вещества по… водороду, кислороду, воздуху, азоту и т.д.
Например:
Относительная плотность вещества – отношение плотности вещества Б к плотности вещества А
Относительная плотность — величина безразмерная
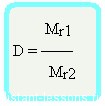
Формула достаточно простая, и из нее вытекает другая формула —
Формула молярной массы вещества
Mr1 = D•Mr2
и т.д.
В условии задачи может быть полная формулировка — «относительная плотность (паров)…», а может быть просто «плотность вещества по…»
Давайте решим нашу задачу:
Дана плотность паров вещества по воздуху, значит, нам подходит формула молярной массы вещества —
Mr (вещества)=Mr(воздуха)•D=29 гмоль • D
Mr(вещества)=29 гмоль • 1.448 = 42 гмоль
Нам дан углеводород — СхHy, значит, мы можем найти Mr(Cx и Mr(Hy). Обратите внимание, именно молярные массы, т.к.у нас несколько атомов углерода и водорода.
Для этого надо молярную массу вещества умножить на процентное содержание элемента:
Mr(Cx)=Mr(вещества)•ω
Mr(Cx)= 42 гмоль · 0.8571=36 гмоль
x=Mr(Cx)Ar(C)=36 гмоль ÷ 12 гмоль =3.
Точно так же находим все данные для водорода:
Mr(Hy)=Mr(вещества)•ω
Mr(Hy)= 42 гмоль · 0.1429=6 гмоль
x=Mr(Hy)Ar(H)=6 гмоль ÷ 1 гмоль =6.
Искомое вещество — C3H6 — пропен.
Еще раз повторим определение —
Относительная плотность газа – это сравнение молярной или относительной молекулярной массы одного газа с аналогичным показателем другого газа.
Дана относительная плотность по аргону.
Mr (вещества)=Ar(Ar)•D
Mr (CxHy)=40 гмоль ·1.05=42 гмоль
Запишем уравнение горения:
СхHy O2 = xCO2 y2H2O
Найдем количество углекислого газа и воды:
n(CO2)=V22,4 лмоль = 33.622.4=1.5
n(H2O)=mMr=2718=1.5
Соотношение х : y2 как 1.5 : 1.5, т.е. y=2x, что соответствует общей формуле алкенов: CnH2n
Выражаем в общем виде молярную массу: Mr=Mr(C) Mr(H)
12n 2n=42
n=3
Наше вещество — C3H6 — пропен
Примеры решенных задач по физике — контрольная 8(молекулярная физика, равновесное излучение, ядерные реакции)
Ниже приведены условия и решения задач. Закачка решений в формате doc начнется автоматически через 10 секунд.
Задача 407.
Найти плотность ![]() газовой смеси, состоящей по массе из одной части водорода и восьми частей кислорода при давлении
газовой смеси, состоящей по массе из одной части водорода и восьми частей кислорода при давлении ![]() газовой смеси, состоящей по массе из одной части водорода и восьми частей кислорода при давлении
газовой смеси, состоящей по массе из одной части водорода и восьми частей кислорода при давлении и температуре
![]()
Дано : ![]()
![]()
![]()
![]()
Найти g.
Решение. Пусть ![]() и
и ![]() и
и — масса водорода и кислорода,
![]() и
и ![]() и
и — их парциальные давления,
![]() объём смеси газов. Согласно уравнению Менделеева – Клапейрона для водорода имеем
объём смеси газов. Согласно уравнению Менделеева – Клапейрона для водорода имеем
![]() ( 1 )
( 1 )
а для кислорода
![]() ( 2 )
( 2 )
где ![]() — молярная масса водорода,
— молярная масса водорода,![]() — молярная масса водорода,
— молярная масса водорода, — молярная масса кислорода,
![]() — универсальная газовая постоянная. Сложим левые и правые части уравнений (1) и (2), учитывая, что
— универсальная газовая постоянная. Сложим левые и правые части уравнений (1) и (2), учитывая, что ![]() — универсальная газовая постоянная. Сложим левые и правые части уравнений (1) и (2), учитывая, что
— универсальная газовая постоянная. Сложим левые и правые части уравнений (1) и (2), учитывая, что — давление смеси газов:
![]()
![]()
откуда объём ![]()
![]()
Масса смеси ![]() поэтому её плотность
поэтому её плотность
![]() ( 3 )
( 3 )
Пусть масса одной части составляет ![]() Тогда масса
Тогда масса ![]() Тогда масса
Тогда масса частей водорода
![]() а масса
а масса ![]() а масса
а масса частей кислорода
![]() Подставляем значения
Подставляем значения
![]() и
и ![]() и
и в формулу (3):
![]()
![]()
Проверка размерности:
![]()
Подставляем данные:
![]()
Ответ: ![]()
Задача 417.
Найти среднее число столкновений в 1 секунду молекул углекислого газа при температуре ![]() если длина свободного пробега при этих условиях равна
если длина свободного пробега при этих условиях равна
![]()
Дано: ![]()
![]()
Найти ![]()
Решение. Среднее число столкновения в единицу времени рассчитывается по формуле
![]() ( 4 )
( 4 )
где ![]() — средняя арифметическая скорость молекул,
— средняя арифметическая скорость молекул, ![]() — средняя арифметическая скорость молекул,
— средняя арифметическая скорость молекул, — средняя длина свободного пробега. В свою очередь скорость
![]() находится по формуле
находится по формуле
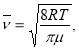 ( 5 )
( 5 )
где ![]() — молярная масса углекислого газа
— молярная масса углекислого газа ![]() — молярная масса углекислого газа
— молярная масса углекислого газа
Подставляем (5) в (4)
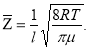
Проверка размерности:
![]()
Подставляем данные:
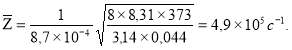
Ответ:![]()
Задача 427.
В баллоне объёмом ![]() литров находится гелий под давлением
литров находится гелий под давлением ![]() литров находится гелий под давлением
литров находится гелий под давлением и при температуре
![]() после того, как из баллона было взято
после того, как из баллона было взято ![]() после того, как из баллона было взято
после того, как из баллона было взято гелия, температура в баллоне понизилась до
![]() Определить давление
Определить давление ![]() Определить давление
Определить давление гелия, оставшегося в баллоне,и изменение внутренней энергии газа.
Дано:![]()
![]()
Найти ![]()
Решение. Пусть ![]() — начальная масса гелия. Запишем уравнение Менделеева – Клапейрона
— начальная масса гелия. Запишем уравнение Менделеева – Клапейрона
![]() ( 6 )
( 6 )
где ![]() — молярная масса гелия. После изъятия из баллона гелия массой
— молярная масса гелия. После изъятия из баллона гелия массой ![]() — молярная масса гелия. После изъятия из баллона гелия массой
— молярная масса гелия. После изъятия из баллона гелия массой его масса становится равной
![]() и уравнение Менделеева – Клапейрона принимает вид
и уравнение Менделеева – Клапейрона принимает вид
![]()
![]()
( 7 )
Из (6) находим массу ![]()
![]()
и подставляем её в (7)
![]()
![]()
откуда давление ![]()
![]() ( 8 )
( 8 )
Начальная внутренняя энергия гелия
![]()
а его конечная внутренняя энергия
![]()
где ![]() — число степеней свободы молекулы. Изменение внутренней энергии.
— число степеней свободы молекулы. Изменение внутренней энергии.
![]() ( 9 )
( 9 )
Подставляем начальную массу ![]() в формулу (9)
в формулу (9)
![]()
![]() ( 10 )
( 10 )
Проверка размерности:
![]()
![]()
![]()
Подставляем данные в формулы (8) и (10), учитывая, что гелий – одноатомный газ, поэтому имеются только три поступательные степени свободы ![]()
![]()
![]()
Отрицательный знак ![]() указывает на то, что внутренняя энергия гелия уменьшается.
указывает на то, что внутренняя энергия гелия уменьшается.
Ответ: ![]()
![]()
Задача 437.
Азот массой ![]()
![]()
адиабатически расширили в
![]()
а затем изобарно сжали до первоначального объёма. Определить изменение энтропии DS газа в ходе указанных процессов.
Дано: ![]()
![]()
![]()
Найти ![]()
Решение. Процессы, в которых участвует газ, изображены на рис.1 на
![]() — диаграмме.
— диаграмме.
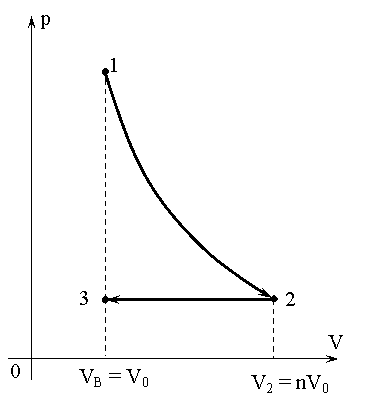
Процесс 1-2 представляет собой адиабатическое расширение, а процесс 2-3 – изобарное сжатие. Изменение энтропии в этих процессах
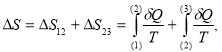 ( 11 )
( 11 )
где ![]() — подводимое к газу количество теплоты. При адиабатическом процессе газ теплоизолирован и
— подводимое к газу количество теплоты. При адиабатическом процессе газ теплоизолирован и ![]() — подводимое к газу количество теплоты. При адиабатическом процессе газ теплоизолирован и
— подводимое к газу количество теплоты. При адиабатическом процессе газ теплоизолирован и Поэтому в данном процессе энтропия не изменяется:
![]() При изобарном процессе при изменении температуры на малое значение
При изобарном процессе при изменении температуры на малое значение
![]()
![]()
![]()
( 12 )
где ![]() — молярная теплоёмкость при постоянном давлении. Подставляем (12) в (11), получаем
— молярная теплоёмкость при постоянном давлении. Подставляем (12) в (11), получаем
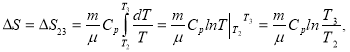 ( 13 )
( 13 )
где ![]() температура газа в состояниях 2 и 3. При изобарном процессе
температура газа в состояниях 2 и 3. При изобарном процессе
![]()
поэтому
![]() ( 14 )
( 14 )
( см.рис.1). Молярная теплоёмкость при постоянном давлении
![]() ( 15 )
( 15 )
При этом число степеней свободы для двухатомной молекулы азота ![]() Подставляя (14) и (15) в ( 13), окончательно получаем
Подставляя (14) и (15) в ( 13), окончательно получаем
![]()
Проверка размерности:
![]()
Подставляем данные:
![]()
Видно, что энтропия при переходе газа из состояния 1 в состояние 3 уменьшается.
Ответ: ![]()
Задача 447.
За 5 мин. излучается энергия ![]() Площадь окошка
Площадь окошка ![]() Площадь окошка
Площадь окошка Принимая, что окошко излучает как абсолютно чёрное тело, определить температуру печи.
Дано: ![]()
![]()
![]()
Найти ![]()
Решение. Излучаемая энергия равна
![]() ( 16 )
( 16 )
где ![]() энергетическая светимость,
энергетическая светимость, ![]() энергетическая светимость,
энергетическая светимость, — площадь излучателя,
![]() промежуток времени. Согласно закону Стефана – Больцмана энергетическая светимость абсолютно черного тела
промежуток времени. Согласно закону Стефана – Больцмана энергетическая светимость абсолютно черного тела
![]() ( 17 )
( 17 )
где ![]() — постоянная Стефана- Больцмана,
— постоянная Стефана- Больцмана, ![]() — постоянная Стефана- Больцмана,
— постоянная Стефана- Больцмана, — температура. Подставляем (17)в (16)
![]()
![]()
откуда находим температуру ![]()
![]()
Проверка размерности:
![]()
Подставляем данные:
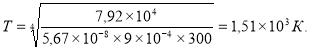
Ответ: ![]()
Задача 457.
В одном акте деления ядра урана ![]() освобождается энергия
освобождается энергия ![]() освобождается энергия
освобождается энергия Определить: 1) энергию, выделяющуюся при распаде всех ядер этого изотопа урана массой
![]() 2) массу каменного угля с удельной теплотой сгорания
2) массу каменного угля с удельной теплотой сгорания
![]() эквивалентную в тепловом отношении
эквивалентную в тепловом отношении ![]() эквивалентную в тепловом отношении
эквивалентную в тепловом отношении урана
![]()
Дано: ![]()
Найти ![]()
![]()
Решение. Если в одном анте деления выделяется энергия ![]() то при распаде
то при распаде ![]() то при распаде
то при распаде ядер выделяется энергия
![]()
Рассчитаем количество ядер ![]() в уране массой
в уране массой ![]() в уране массой
в уране массой Количество урана
![]() где
где ![]() где
где — молярная масса изотопа
![]() Поэтому
Поэтому
![]()
где ![]() постоянная Авогадро. Таким образом, выделяемая энергия
постоянная Авогадро. Таким образом, выделяемая энергия
![]()
Эквивалентная в тепловом отношении масса каменного угля
![]()
Проверка размерности:
![]()
![]()
Подставляем данные, предварительно переведя энергию ![]() из
из![]() из
из в
![]()
![]()
![]()
![]()
Ответ: 1) ![]() 2) 2,8 тысячи тонн.
2) 2,8 тысячи тонн.
Срядняя плотность по водороду газовой смеси состоит из водорода и кислорода равна14,5.вычислите сколько объемных процентов водорода и кислорода содержится в смеси? —
обозначим объемную долю водорода за х, тогда получим уравнение
два икс плюс 32(1-х) равно 29, раскрываем скобки и находим х=о,1. Объемная доля водорода 10 процентов, а кислорода 90 процентов