§3.5 элементы с переменной валентностью.
§3.5 Элементы с переменной валентностью.
До сих пор мы не объясняли причину переменной валентности некоторых элементов на основе строения их атомов. Давайте сделаем это на примере элемента 16S (серы).
Действительно, почему сера в одних соединениях двухвалентна, в других — четырехвалентна, а в третьих — шестивалентна? Наконец, откуда именно такие, а не другие значения валентности — II, IV, VI? Теперь мы знаем достаточно для того, чтобы ответить на эти вопросы. Рассмотрим три реакции, в которых сера проявляет разные валентности:
2 H S = H2S (валентность серы II),
2 O S = SO2 (валентность серы IV),
3 O S = SO3 (валентность серы VI).
Сера располагает свои 16 электронов на 1-м, 2-м и 3-м уровнях:
1s2 2s2 2p6 3s2 3p4
Как обычно, нас интересуют только валентные электроны последнего уровня:
…3s2 3p4
В основном (не возбужденном) состоянии сера двухвалентна. В реакции с атомами водорода она образует соединение H2S потому, что у нее на двух p-орбиталях (из трех имеющихся) находится по одному электрону, и остается место для спаривания еще с двумя «чужими» электронами водородных атомов.
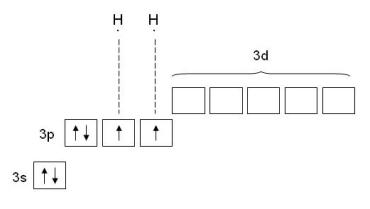
Однако, в отличие от атомов водорода или кислорода, у которых валентные электроны находятся на 1-м и 2-м уровнях (где нет d-подуровней), валентная оболочка серы имеет пустой 3d-подуровень. Этот 3d-подуровень находится достаточно близко по энергии к внешнему 3p-подуровню атома серы. При поглощении даже небольшой порции энергии один из 3p-электронов может переходить на 3d-подуровень (рис. 3-5). Затрата энергии при этом с лихвой покрывается выигрышем при образовании дополнительных ковалентных связей.
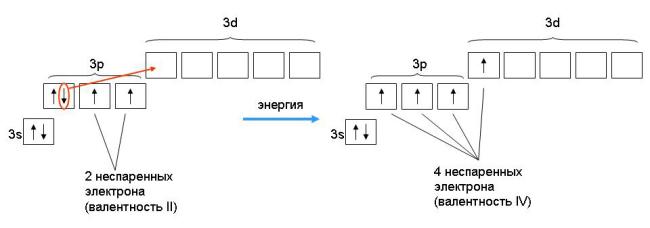
Рис. 3-5. Переход атома серы из основного состояния с валентностью II в первое возбужденное состояние с валентностью IV.
Таким образом, на внешнем уровне возбужденного атома серы оказывается уже 4 неспаренных электрона. Эти 4 электрона могут быть предоставлены двум атомам кислорода для образования молекулы SO2.
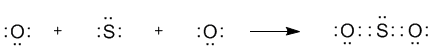
Дальнейшее возбуждение атома серы (которое требует уже гораздо больше энергии) ведет к переходу одного из 3s-электронов на 3d-уровень (рис. 3-6). В результате атом серы получает шесть неспаренных электронов, которые предоставляются уже трем атомам кислорода для образования молекулы SO3.
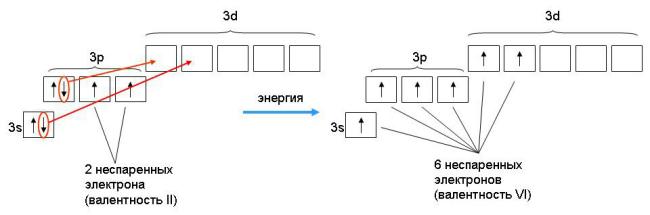
Рис. 3-6. Переход атома серы во второе возбужденное состояние с валентностью VI.
Возникает вопрос: соблюдается ли правило октета в молекулах SO2 и SO3? На первый взгляд, у атома серы оказывается избыток (10 и 12) электронов и такие молекулы не должны быть стабильными. В чем же дело?
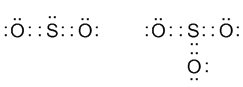
Объяснение заключается в большой разнице электроотрицательностей серы (X = 2,58) и кислорода (X = 3,44) — у кислорода она значительно выше. Можно предположить, что в молекуле SO2 кислород оттягивает с внешней оболочки атома серы именно столько электронов, сколько нужно для того, чтобы сделать ее похожей на октетную оболочку. Это можно показать даже с помощью структурных формул:
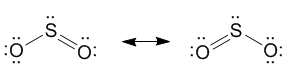
В каждой из таких «крайних» структур одна «лишняя» электронная пара всегда целиком сдвинута к одному из атомов кислорода. Реальная молекула, как полагают, является чем-то средним между этими двумя крайними структурами. Аналогичная ситуация в молекуле SO3, но ее строение описывается уже не двумя, а тремя крайними структурами (заметьте, что все они октетные):
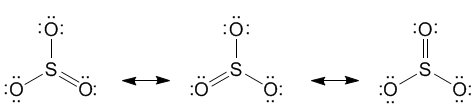
Почему же не существует таких соединений, как H4S и H6S, где сера тоже проявляет валентность (IV) и (VI)? Вероятно, в этом случае правило октета для серы действительно оказалось бы нарушенным, поскольку водород недостаточно электроотрицателен, чтобы оттянуть «лишние» электроны с внешней оболочки атома серы. Поэтому такие соединения до сих пор не получены. Эти вещества должны быть чрезвычайно неустойчивы. Зато изначально «октетная» молекула сероводорода H2S вполне устойчива. Таким образом, сера может проявлять валентность IV и VI только в соединениях с более электроотрицательными элементами, чем она сама. Действительно, не существуют соединений K6S, Ca2S, и других подобных веществ, но вполне устойчив, например, газообразный фторид серы SF6.
Электроотрицательность дает ответ и еще на один вопрос: почему в орбитальных диаграммах на рис. 3-5 и 3-6 мы не рисуем 4s-подуровень, который по энергии тоже близок к 3p- и 3d-подуровням? Из главы 2 мы знаем, что 4s-подуровень в большинстве атомов заполняется электронами даже раньше 3d-подуровня — сразу следом за 3p-подуровнем. Почему же его нет на орбитальных диаграммах?
Вероятно, 4s-подуровень можно включать в орбитальные диаграммы, но это ровным счетом ничего не изменит, потому что при соединении серы с кислородом этот подуровень всего лишь будет выполнять роль «электрического провода», по которому электроны перетекают от атома серы к более электроотрицательным атомам кислорода или фтора.
К счастью, молекулярные орбитали в соединениях серы (IV) и (VI) не полностью повторяют электронные оболочки инертных газов, а всего лишь подобны им. Вспомним, что до сих пор не удается вовлечь неон и аргон в химические реакции. Если бы вещества SO2, SO3, SF4, SF6 оказались такими же устойчивыми, как инертные газы, мы бы просто не смогли получать из них другие полезные соединения, с которыми познакомимся позже.
** В этом параграфе вам встретились не совсем обычные «крайние» структуры оксидов серы SO2 и SO3. Например, в наборе крайних структур для SO2 у атома четырехвалентной серы только 3 валентных штриха, и в каждой из формул есть какой-то странный «одновалентный» кислород. Чтобы устранить эти противоречия, можно атому серы в «крайних» структурах приписать положительный заряд, а «одновалентным» атомам кислорода — отрицательные заряды. Кстати, это будет соответствовать реальному распределению зарядов в молекуле SO2, если помнить при этом, что заряды здесь на самом деле не полные, а частичные.

Соседство зарядов » » и «-» на соседних атомах в данном случае заменяет недостающую простую связь между серой и кислородом. Важно понимать, что каждая из этих структур не существует в отдельности. Это как бы «чертеж» молекулы. Представьте чертеж какого-нибудь знакомого предмета — например, собачьей будки. Его можно начертить в трех проекциях: вид спереди, вид сбоку, вид сверху. Согласитесь, что нельзя изготовить для собаки один только «вид сверху» и заставить ее там жить.
Точно так же нельзя синтезировать каждую из крайних структур в отдельности. Они потому и называются крайними, что электроны в них смещены в крайние из возможных положений. В реальной молекуле такая ситуация никогда не реализуется полностью и она представляет собой нечто среднее между двумя или несколькими крайними структурами. Другое их название — резонансные структуры. Они находят широкое применение в органической химии для описания строения таких соединений, как бензол и его производные. Например, вот так можно показать, что существуют не два разных 1,2-дихлорбензола, а только один, молекула которого представляет собой нечто среднее между двумя крайними структурами, соединенными обоюдоострыми стрелками (атомы водорода в кольце здесь не показаны):
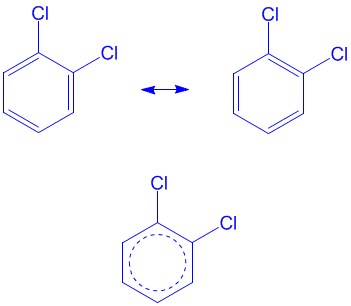
Такие обоюдоострые стрелки — это ни в коем случае не химическое равновесие между реальными молекулами, а знак перемещения электронов в гипотетические «крайние» положения одной молекулы.
Задачи.
3.16. Изобразите структурные формулы хлорида фосфора (III) и хлорида фосфора (V).
Объясните переменную валентность фосфора с точки зрения строения его атома. Будут ли, по вашему мнению, устойчивы соединения фосфора (III) и фосфора (V) с водородом?
** 3.17. (ФМШ). Изобразите структурные формулы следующих соединений хлора: HClO4, HClO3, HClO2, HClO (в этой молекуле нет связи H-Cl), HCl, Cl2. Объясните валентность хлора в этих соединениях с помощью орбитальных диаграмм. Может ли фтор образовывать подобные соединения? Ответ обоснуйте.
_________________
Сравнить строение атомов кислорода и серы; физические свойства кислорода и серы — знания.org
В атомах серы имеется 6 валентных электоронов, от сюда: она может быть шестивалентной. У серы больше радиус, чем у кислорода.
У кислорода: незаполненная электронная оболочка, на которой не хватает 2-ух электронов.
Физические св-ва Серы:В отличие от кислорода, образующего 2 аллотропные формы, сера образует большее число аллотропных модификаций, отличающихся всеми св-вами. Образует 2 аллотропные модификации: ромбическую и моноклинную. Способна сера образовывать цепи. Все аллотропные модификации со временем переходят в ромбическую форму.
Ромбическая модификация серы: цвет: лимонно-желтый, плотность: 2,07 г/см^3 , темп. пл : 112,8, нерасторима, плохие проводники тепла и электричества. Моноклинная- цвет: медово-желтый, плотность :1,96, темп. пл. : 119,0 , нерастворима, плохие проводнкии тепла и электричества.
У кислорода: при нормальных условиях кислород-газ без цвета и запаха, немного тяжелее воздуха, слабо растворяется в воде и спирте, при нагревании происходит диссоциация его на атомы.
Существует жидкий кислород — это бледно-голубая жидкость и твердый кислород — синие кристаллы
Тема 2. химическая связь и строение молекул.
Читайте также:
|
ЗАДАНИЕ НА КОНТРОЛЬНУЮ РАБОТУ
Общие методические указания
В процессе изучения курса химии студент должен выполнить одну контрольную работу. Решение задач и ответы на теоретические вопросы должны быть коротко, но четко обоснованы. При решении задач нужно приводить весь ход решения и математические преобразования.
Контрольная работа должна быть аккуратно оформлена, написана четко и ясно и иметь поля для замечаний рецензента.
Номера и условия задач необходимо переписывать в том порядке, в каком они указаны в задании. В начале работы следует указать учебный шифр студента, номер варианта и полный список номеров задач этого варианта.
В конце работы следует дать список использованной литературы с указанием года издания.
Работа должна иметь подпись студента и дату.
Если контрольная работа не зачтена, ее следует выполнить повторно в соответствии с указаниями рецензента и представить вместе с незачтенной работой. Исправления следует выполнять в конце работы, после рецензии, а не в тексте.
Контрольная работа, выполненная не по своему варианту, преподавателем не рецензируется и не засчитывается как сданная.
Каждый студент выполняет вариант контрольных заданий, обозначенный двумя последними цифрами номера студенческого билета (6594, две последние цифры 94, им соответствует вариант контрольного задания 94).
Контрольная работа выполняется в тетради в клетку на 18 листов.
Варианты контрольных заданий
| Номер варианта | Номера задач, относящихся к данному варианту | |||||||
| 01 35 69 | ||||||||
| 02 36 70 | ||||||||
| 03 37 71 | ||||||||
| 04 38 72 | ||||||||
| 05 39 73 | ||||||||
| 06 40 74 | ||||||||
| 07 41 75 | ||||||||
| 08 42 76 | ||||||||
| 09 43 77 | ||||||||
| 10 44 78 | ||||||||
| 11 45 79 | ||||||||
| 12 46 80 | ||||||||
| 13 47 81 | ||||||||
| 14 48 82 | ||||||||
| 15 49 83 | ||||||||
| 16 50 84 | ||||||||
| 17 51 85 | ||||||||
| 18 52 86 | ||||||||
| 19 53 87 | ||||||||
| 20 54 88 | ||||||||
| 21 55 89 | ||||||||
| 22 56 90 | ||||||||
| 23 57 91 | ||||||||
| 24 58 92 | ||||||||
| 25 59 93 | ||||||||
| 26 60 94 | ||||||||
| 27 61 95 | ||||||||
| 28 62 96 | ||||||||
| 29 63 97 | ||||||||
| 30 64 98 | ||||||||
| 31 65 99 | ||||||||
| 32 66 00 | ||||||||
| 33 67 | ||||||||
| 34 68 |
Раздел №1. Строение вещества.
Тема 1. СТРОЕНИЕ АТОМА.
Тема 2. ХИМИЧЕСКАЯ СВЯЗЬ И СТРОЕНИЕ МОЛЕКУЛ.
Пример 1.Описать свойства атома индия и его положение в периодической системе элементов.
Решение.Так как Z=49, заряд ядра атома Jn и общее количество электронов равны 49. Зная, что свойства атома определяет структура его валентных электронов, начнем с ее построения. Индий находится в 5 периоде III А группы, отсюда его валентные электроны имеют следующую структуру: 5s25p1.
Наличие трех электронов на внешнем уровне и большой радиус атома (n = 5) предполагают достаточную легкость отдачи электронов (небольшую энергию ионизации) и как следствие – металлические свойства и достаточно высокую химическую активность.
Пример 2.Какую валентность, обусловленную неспаренными электронами (спин-валентность), может проявлять фосфор в нормальном и возбужденном* состояниях?
Решение.Распределение электронов внешнего энергетического уровня фосфора …3s23p3 (учитывая правило Хунда, 3s23pх 3pу 3pZ ) по квантовым ячейкам имеет вид: 15Р 3s23pх1 3pу1 3pZ13d0
Атомы фосфора имеют свободные d – орбитали, поэтому возможен переход одного 3s – электрона в 3d – состояние:
15Р* 3s13pх1 3pу1 3pZ13d1
Отсюда валентность (спин-валентность) фосфора в нормальном состоянии равна трем, а в возбужденном – пяти.
Пример 3.Укажите тип связей в молекулах F2, KCl, HCl. Приведите электронные модели их строения.
| или перекрыванием одноэлектронных р-р-орбиталей: |
Решение.1. Молекула F2 состоит из двух одинаковых атомов фтора, поэтому ковалентная связь будет неполярной. Так как структура валентных электронов фтора …2s22p5, строение молекулы можно представить:
2. Молекула КСl состоит из двух резко отличающихся по электроотрицательности атомов металла (К) и неметалла (Сl), что определяет ионный тип связи;
К0 – ē → К
Cl0 ē → Cl—
К Cl– → КCl
3. Молекула НСl тоже состоит из двух разных атомов Н и Сl, поэтому в данном случае имеем ковалентную полярную связь,причем общая электронная пара смещена к более электроотрицательному атому хлора:
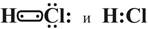
При этом происходит перекрывание s-р – валентных орбиталей водорода и хлора:
s – p
Пример 4.Определите тип кристаллической решетки SiC и сделайте вывод о свойствах данного вещества.
Решение.Валентные электронные структуры кремния и углерода сходны (…3s23p2 и …2s22p2), поэтому в результате перекрывания они образуют ковалентную связь (малополярную). Так как их насыщаемость в соединении высока (четыре связи), вещество является твердым и образует атомную кристаллическую решетку. А это влечет за собой высокую твердость вещества, его тугоплавкость, малую растворимость и диэлектрические свойства.
Контрольные вопросы
1. У какого из элементов – лития, цезия или бериллия – больше энергия ионизации? Сделайте вывод о химических свойствах их атомов, у какого элемента наиболее выражены металлические свойства?
2. Какой из элементов S или Se проявляют более выраженные окислительные свойства? Почему?
3. Почему Cu, Ag, Au – это благородные металлы? Дайте объяснение их свойств на основе электронных структур и справочного материала.
4. Радиусы атомов Si и V равны (r=1,34 Ао), почему же так различны их свойства?
5. Почему Mn и Cl расположены в одной группе периодической системы, но в разных подгруппах? Дайте сравнительную характеристику свойств этих элементов на основе их электронных структур.
6. Какие типы связей проявляются в кристаллах следующих веществ: воды, метана, кремния, хлорида кальция, алюминия, оксида углерода (IV).
7. Почему свойства всех элементов II периода очень сильно отличаются от свойств элементов всех последующих периодов?
8. Пользуясь периодической системой, выясните, какие химические элементы относятся к подгруппе азота. Выпишите их символы и названия. Приведите для каждого элемента электронную конфигурацию валентного слоя атома. Предскажите возможные степени окисления данных элементов.
9. Изобразите с помощью квантовых ячеек строение атомов кислорода и германия. Сделайте вывод об их химических свойствах. Приведите формулы гидроксидов этих элементов в высшей степени окисления.
10. Выделите валентные орбитали атомов кремния и ванадия. Сделайте вывод о химических свойствах этих атомов.
11. У какого из элементов As или Cl электроотрицательность выше? Почему? Сделайте вывод об их химических свойствах.
12. Составьте формулы водородных соединений азота и фосфора. В каком из этих соединений химическая связь более прочная? Какое из этих соединений и почему термически менее устойчиво?
13. Укажите тип химической связи в молекулах N2, NaCl. Приведите схемы перекрывания их электронных облаков.
14. Укажите тип химической связи в молекулах NН3, Н2О. Приведите электронные модели их строения.
15. Какую валентность, обусловленную неспаренными электронами, может проявлять свинец в нормальном и возбужденном состояниях? Сделайте вывод о химических свойствах соединений Pb с разной степенью окисления.
16. Укажите тип кристаллической решетки в кристаллах Н2О, CsF. Сделайте вывод о свойствах этих кристаллов.
17. Почему Н2О – жидкость, а Н2S – газ? Сравните их tкип, tпл.
18. Определите тип связи молекул NaI и CH4. Сделайте вывод об их свойствах (прочность, реакционная способность, агрегатное состояние).
19. У каких кристаллов: Н2О, SiO2, КСl, Li температура плавления наибольшая? Ответ обоснуйте.
20. Какой тип кристаллической решетки характерен для веществ с самой низкой температурой плавления? Ответ обоснуйте. Почему кислород и сера, имея в наружном слое одинаковое число электронов, проявляют разную валентность?
21. Проанализируйте валентные возможности атомов Be и Al в основном и возбужденном состояниях. Приведите формулы высших оксидов рассматриваемых элементов и предскажите их кислотно-основные свойства.
22. Укажите, какие из перечисленных молекул являются полярными, а какие неполярными: СО2, Н2О, SO2, СН4. Ответ мотивируйте.
23. Как изменяются химические свойства соединений марганца и характер связей в них с увеличением степени окисления?
Дата добавления: 2022-02-16; просмотров: 55 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.013 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
Экзотермическая реакция – протекает с выделением тепла (DН0хим.р <.0). Эндотермическая реакция – протекает с поглощением тепла (DН0хим.р >0).
Пример 1. Укажите в каком направлении повышается устойчивость карбонатов MgСО3(к); CaCО3(к); BaCO3(к).
Решение. Устойчивость веществ определяется значениями величин DН0образ (термическая устойчивость) и DG0образ (химическая устойчивость). Чем меньше эти значения, тем вещество более устойчиво. Для ответа сравним величины DН0образ и DG0образ данных карбонатов:
| Наименование карбоната | DН0образ, кДж/моль | DG0образ, кДж/моль |
| MgСО3 | -1096,21 | -1029,3 |
| CaСО3 | -1206 | -1128,8 |
| BaCO3 | -1202 | -1164,8 |
Из сравнения величин DG и DН следует, что устойчивость карбонатов в ряду MgСО3®CaCО3®BaCO3 повышается (термическая устойчивость CaCО3 и BaCO3 почти одинакова, т.к. 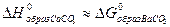
Пример 2. Прямая или обратная реакция будет протекать при стандартных условиях в системе:
СН4(г) СО2(г)Û2СО(г) 2Н2(г)
Решение. Для ответа на вопрос следует вычислить DG0298 прямой реакции (значения DG0298 соответствующих веществ приведены в табл.1 и в Приложении в табл.2). Зная, что DG0298 есть функция состояния и что DG для простых веществ, находящихся в устойчивых при стандартных условиях агрегатных состояниях, равны 0, находим DG0298 процесса по формуле:
DG0х.р.=åDG0образ.пр.-åDG0образ.исх.
DG0х.р.=2(-137,27) 2(0)-(-50,79-394,38)= 170,63 кДж
То, что DG0298>0, указывает на невозможность самопроизвольного протекания прямой реакции при Т=298 К и равенстве давлений взятых газов 1,013×105 Па (760 мм рт.ст.=1 атм).
Таблица 1
| Вещество | Состояние | DG0298, кДж/моль | Вещество | Состояние | DG0298, кДж/моль |
| ВаСО3 | К | -1138,8 | FeO | К | -244,3 |
| СаСО3 | К | -1128,75 | H2O | Ж | -237,19 |
| Fe3O4 | К | -1014,2 | H2O | Г | -228,59 |
| ВеСО3 | К | -944,75 | PbO2 | К | -219,0 |
| СаО | К | -604,2 | CО | Г | -137,27 |
| ВеО | К | -581,61 | CH4 | г | -50,79 |
| ВаО | К | -528,4 | NO2 | г | 51,84 |
| СО2 | Г | -394,38 | NO | г | 86,69 |
| NaCl | К | -384,03 | C2H2 | г | 209,20 |
| ZnO | К | -318,2 |
Пример 3. Вычислите DН0, DS0, DG0Т реакции, протекающей по уравнению
Fe2O3(к) 3C=2Fe 3CO.
Возможна ли реакция восстановления Fe2O3 углеродом при температурах 500 и 1000 К?
Решение. DНх.р. и DSх.р. находим по формулам (DН, S – функции состояния систем):
DН0х.р.=åDН0прод.-åDG0исх.
DS0х.р.=åDS0прод.-åDS0исх.
DН0х.р.=[3(-110,52) 2×0]-[-822,10 3×0]=-331,56 822,10= 490,54 кДж/моль
DS0х.р.=(2×27,2 3×197,91)-(89,96 3×5,69)=541,1 Дж/моль
Энергию Гиббса при соответствующих температурах находим из соотношения
DG0Т=DН0-ТDS0:
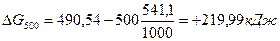
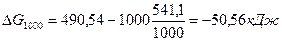
Так как DG500>0, а DG1000<0, то восстановление Fe2O3 углеродом возможно при 1000 К и не возможно при 500 К.
Пример 4.Реакция восстановления Fe2O3 водородом протекает по уравнению
Fe2O3 (к) 3Н2 (г)=2Fe (к) 3Н2О (г), DН= 96,61 кДж. Возможна ли эта реакция при стандартных условиях, если изменение энтропии DS=0,1387 кДж/(моль×К)? При какой температуре начнется восстановление Fe2O3?
Решение. Вычисляем DG0 реакции:
DG0Т=DН0-ТDS0=96,61-298×0,1387= 55,28 кДж.
Так как DG0>0, то реакция при стандартных условиях невозможна; наоборот, при этих условиях идет обратная реакция окисления железа (коррозия). Найдем температуру, при которой DG=0:
DН=ТDS; 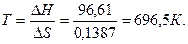
Следовательно, при температуре » 696,5 К, начнется реакция восстановления Fe2O3. Иногда эту температуру называют температурой начала реакции.
Контрольные вопросы.
24. Вычислите DН0, DS0, DG0500 реакции Fe2O3(к) 3Н2=2Fe(к) 3Н2О(г).
25. Реакция протекает по уравнению TiO2(к) 2С(к)=Ti(к) 2СО(г). Вычислите DН0, DS0, DG01000. Возможна ли эта реакция при 1000 К?
26. При какой температуре возможны реакции восстановления:
Fe2O3(к) 3C(граф) = 2Fe(к) 3CO2(г);
Возможна ли эта реакция при стандартных условиях?
27. Напишите термохимическое уравнение реакции взаимодействия газообразных аммиака и хлористого водорода. Сколько теплоты выделится в ходе этой реакции, если было израсходовано 100 л аммиака?
28. При гашении извести СаО водой выделяется 32,5 кДж теплоты. Напишите термохимическое уравнение реакции и определите энтальпию образования оксида кальция.
29. Напишите термохимическое уравнение реакции между CO(г) и водородом, в результате которой образуются CH4(г) и H2O (г). Сколько теплоты выделится при этой реакции, если было получено 67,2 л метана в пересчете на нормальные условия?
30. При сгорании 1 л водорода выделяется 12,76 кДж. Рассчитать энтальпию образования воды. Какая вода получается в результате этого процесса – пар или жидкость?
31. Оцените величины DН и DS реакции Fe2O3 3/2С(к)=3/2СО2(г) 2Fe(к). На их основании определите условия ее протекания.
32. Аллотропные модификации углерода. Теплота сгорания карбина ΔH0298 = 356,1 кДж/моль, а для графита теплота сгорания ΔH0298 = 396,3 кДж/моль. Сравнить термическую устойчивость графита и карбина. Чем объясняется необычное обилие соединений углерода.
33. Вычислите тепловой эффект и напишите термохимическое уравнение реакции горения 1 моль этана C2H6(г), в результате которой образуются пары воды и диоксида углерода. Сколько теплоты выделится при сгорании 1м3 этана в пересчете на н.у.
34. При какой температуре начнется реакция: СН4(г) СО2(г) = 2СО(г) 2Н2(г). Возможна ли она при стандартных условиях.
35. Пользуясь таблицами DG0обр,298 и S0обр,298, определите возможен ли самопроизвольный процесс Al2O3(к) 3SO3(ж)=Al 2 (SO4 )3 (к) при 298 К.
35. Пользуясь таблицами DН0обр,298 вычислите DН0298 реакции Zn(NO3)2(к)=ZnO(к) 2NO2(г) 1/2О2(г).
36. Кристаллический хлорид аммония образуется при взаимодействии газообразных аммиака и хлорида водорода. Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект. Сколько теплоты выделится, если в реакции было израсходовано 10 л аммиака в пересчете на нормальные условия?
37. Реакция горения аммиака выражается термохимическим уравнением:
4NH3(г) 3O2(г) = 2N2(г) 6H2O(ж); DH = 1530,28 кДж. Вычислите теплоту образования NH3(г).
38. Сравните термическую устойчивость нитратов калия, свинца и серебра. Напишите уравнения реакций их термического разложения.
39. По таблицам DG0обр,298 и S0298, рассчитайте, какое количество теплоты выделится при разложении 1 г AgNО3?
40. При взаимодействии трех молей оксида азота N2O с аммиаком образуются азот и пары воды. Тепловой эффект реакции равен –877,76 кДж. Напишите термохимическое уравнение этой реакции и вычислите теплоту образования N2O(r).
41.Стандартные изобарные потенциалы HCl, HBr, HJ в водных растворах равны: -124,0 кДж/моль, -100,0 кДж/моль и -48,0 кДж/моль соответственно. Как изменится устойчивость кислот при переходе вниз по подгруппе?
42. Сравните изобарные потенциалы реакций:
MnO(к) Н2О(ж)=Mn(ОН)2(ж) DG0298=-120 кДж/моль
Mn2O3(к) 3Н2О(ж)=2Mn(OH)3 DG0298= 76 кДж/моль.
Какой из оксидов MnO или Mn2O3 обладает более сильными основными свойствами.
43.Сравним стандартные теплоты реакции:
Na(к) 1/2F2=NaF(к) -544,0 кДж/моль
Na(к) 1/2Cl2(г)=NaCl(к) -400,0 кДж/моль
Na(к) 1/2Br2(г)=NaBr(к) -344,0 кДж/моль
Na(к) 1/2J2(г)=NaJ(к) -268,0 кДж/моль
Какой из галогенидов натрий наиболее устойчив?
44.Для получения серной кислоты используются следующие реакции:
DН0 DS0 DG0
S(к) О2(г)=SO2(г) -70,9 2,7 -71,7
SO2(г) 1/2О2(г)=SO3(г) -23,7 -22,5 -17,0
SO3 Н2О(ж)=Н2SO4(ж) -35,4 -73,2 -32,5
Что Вы можете сказать об энергетической устойчивости SO2 и SO3.
45.При комнатной температуре олово может существовать в двух модификациях: серое олово и белой олово. Основываясь на термических характеристиках, данных в таблице
| Олово | DН0обр кДж/моль | S0 Дж/моль×К |
| Sn (белое) | ||
| Sn (серое) | -2 |
Определите, какое олово термически устойчиво при стандартной температуре.
46. При сгорании газообразного аммиака, образуются пары воды и оксид азота NO(г). Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект в расчете на 1 моль NH3(г).
Дата добавления: 2022-02-16; просмотров: 61 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.031 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
Тема 3. ХИМИЧЕСКАЯ КИНЕТИКА
Химическая кинетика – это учение о химическом процессе, его механизме и закономерности протекания во времени. При исследовании химических реакций применяют как методы химической термодинамики, так и методы химической кинетики. Химическая термодинамика позволяет вычислить тепловой эффект данной реакции, а также предсказать, осуществима ли данная реакция и состояние её равновесия, т.е. предел, до которого она может протекать. Но для практики нужно знать не только возможности осуществления данной реакции, но и скорость её протекания. Ответ на этот вопрос даёт химическая кинетика.
Скорость химической реакции – это изменение концентрации одного из реагирующих веществ в единицу времени в единице реакционного пространства.
 ,
,
где С – молярная концентрация одного из реагирующих веществ. Знак « » относится к изменению концентрации вещества, образующегося в результате реакции, а знак «-», к изменению концентрации вещества, вступающего в реакцию.
Скорость реакции зависит от многих факторов:
1) Природы реагирующих веществ. Так, например, взаимодействие между электролитами, где вещества находятся в ионном виде, протекает практически мгновенно в отличие от взаимодействия молекул с ковалентными связями (органические неполярные растворители);
2) Физического состояния веществ. При изучении скорости химической реакции необходимо различать реакции в гомогенных и гетерогенных системах. Гомогенныминазывают такие однородные системы, между составными частями которых нет каких-либо поверхностей раздела, например, газовые смеси или растворы.
Гетерогенными называют такие разнородные системы, составные части (фазы) которых отделены друг от друга поверхностями раздела. Сами фазы однородны, т.е. гомогенны. Например, жидкости, сосуществующие с парами или кристаллами, несмешивающиеся жидкости, или же жидкости, сосуществующие одновременно с кристаллами и с газами. Таким образом, системы могут состоять из двух, трех и большего числа фаз и реакция протекает на границе раздела фаз.
Скорость гетерогенных реакций зависит от площади поверхности, на которой они протекают. Увеличение площади поверхности твердого вещества путем измельчения приводит к возрастанию скорости реакции.
.
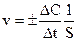 ,
,
где S – площадь границы раздела фаз.
Дата добавления: 2022-02-16; просмотров: 4 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.017 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
где [А], [В2] – молярные концентрации реагирующих веществ, а коэффициент k называется константой скорости химической реакции, который зависит от природы реагирующих веществ.
Данную формулу можно применять, если в качестве реагирующих веществ выступают идеальные газы или сильно разбавленные растворы. Если в реакции участвуют вещества в твердой фазе, то при записи закона действия масс их не нужно учитывать.
Формулу также нельзя применить к реакциям сумма показателей степеней концентраций которых больше трех. Так как вероятность одновременного столкновения трех и более молекул невелика, такие реакции идут в несколько стадий.
Пример 2.Как изменится скорость реакции: NO(г.) O2(г.) ↔ NO2(г.), если уменьшить объем реакционного сосуда в 3 раза?
Решение.Расставим коэффициенты в уравнении: 2NO(г.) O2(г.) ↔ 2NO2(г.)
До изменения объема скорость реакции выражалась уравнением: υ1 = k[NO]2[O2].
Вследствие уменьшения объема концентрация каждого из реагирующих веществ возросла в 3 раза. Следовательно, теперь: υ2 = k(3[NO])2(3[O2]) = 27 k [ NO ]2[O2].
Сравнивая выражения для υ1 и υ2 видим, что скорость реакции возросла в 27 раз.
Ответ: скорость реакции возросла в 27 раз.
5) Влияние катализаторов. Вводимые в реакционную систему в небольших количествах, катализаторы значительно изменяют скорость реакции и выделяются в конце реакции в химически неизменном состоянии.
Каждая реакция характеризуется энергетическим барьером (который помогает снизить катализатор). Для его преодоления необходима энергия активации ЕА – некоторая избыточная энергия (по сравнению со средней энергией молекул при данной температуре), которой должны обладать молекулы для того, чтобы их столкновение было эффективным. С ростом температуры число активных молекул быстро увеличивается, что и приводит к резкому возрастанию скорости реакции.
Зависимость константы скорости реакции от энергии активации выражается уравнением Аррениуса:
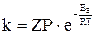 ,
,
где Z-число столкновений молекул в секунду в единице объёма, Т-температура, R-универсальная газовая постоянная, Р — вероятность того, что столкновение двух молекул приведёт к образованию нового вещества.
Пример 3.Энергия активации некоторой реакции в отсутствие катализатора равна 75,24 кДжмоль, а с катализатором – 50,14 кДж/моль. Во сколько раз возрастёт скорость реакции в присутствии катализатора, если реакция протекает при 298 К.
Решение.Обозначим энергию активации реакции без катализатора через ΕА1, а с катализатором через ΕА2; соответствующие константы скорости реакции обозначим через k и k’. Используя уравнение Аррениуса находим:
 отсюда:
отсюда: 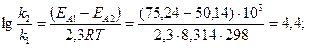
Ответ:скорость реакции возросла в 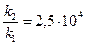 (25 тысяч раз).
(25 тысяч раз).
6) Влияние инициаторов. Имеется большая группа химических реакций – окисление молекулярным кислородом, процессы полимеризации и др., которые начинаются в присутствии инициаторов. Инициаторами называют вещества, которые легко распадаются на активные частицы (радикалы, свободные атомы, возбужденные молекулы и др.). В качестве инициаторов используют пары натрия, некоторые перекисные и азосоединения. Реакции, протекающие с участием активных частиц, называются цепными.
7) Влияние электромагнитного излучения. Реакции, протекающие под влиянием электромагнитного излучения ультрафиолетового или видимого участка спектра, называются фотохимическими. При поглощении кванта света молекулы возбуждаются и становятся реакционноспособными. К фотохимическим реакциям относятся фотосинтез, выцветание красок и др.
Большинство химических реакций обратимы, то есть протекают одновременно во взаимно противоположных направлениях. Состояние химического равновесия сохраняется до тех пор, пока не изменятся внешние условия. В этом случае могут неодинаково измениться скорости прямой и обратной реакции, и произойдет сдвиг (смещение) равновесия.
Закономерности, которые наблюдаются при смещении химических равновесий, охватывает принцип Ле Шателье:
если на систему, находящуюся в состоянии равновесия, оказать какое-либо внешнее воздействиее, то в системе усилится реакция (прямая или обратная), течение которой ослабляет влияние этого воздействия.
Следствие 1. При увеличении температуры ускоряются и прямая, и обратная реакции, а равновесие смещается в сторону эндотермической реакции, а при уменьшении замедляются и прямая, и обратная реакции, а равновесие смещается в сторону экзотермической реакции.
Следствие 2. Принимая во внимание, что молярные объемы различных газов при одинаковых условиях также одинаковы при увеличении давления в газовых смесях равновесие смещается в сторону образования меньшего числа молей газов, а при увеличении давления – в сторону образования большего числа молей газов.
В процессах, протекающих в жидеих фазах значительных изменений объемов происходить не может и изменение давления не вызывает значительных смещений равновесий.
Следствие 3. При увеличении концентрации какого либо компонента системы равновесие смещается в сторону расхода этого компонента.
Следствие 4. Участие катализатора приводит к равномерному ускорению как прямой, так и обратной реакции и в связи с этим не оказывает влияния на смещение равновесия.
Химическая реакция mA nB↔pC qD (где n, m, p и q указывают число молекул А, В, С и D) протекает при постоянных давлении и температуре. В ходе реакции число молей исходных веществ А и В уменьшается, а число молей продуктов реакции C и D увеличивается.
. Химическое равновесие это состояние системы, при котором скорость прямой реакции равна скорости обратной реакции. применив закон действия масс для гомогенной системы, зависимость прямой и обратной реакции от концентрации реагирующих веществ определяется выражениями:
vпр.=kпр.[А]m[В]n, vобр.=kобр.[С]p[D]qи при vпр.= vобр. получим что


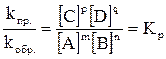 .
. 
Константа равновесия системы представляет собой отношение констант скорости прямой и обратной реакции или отношение произведения концентрации продуктов реакции к произведению концентраций исходных веществ.
Величина Кр связана с изменением энергии Гиббса следующим уравнением:
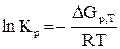
Пример 4.При некоторой температуре константа диссоциации йодовородорода на простые вещества равна 6,25·10-2. Какой процент HI диссоциирует при этой температуре?
Решение.Уравнение диссоциации HI:
2HI(г.) ↔ H2(г.) I2(г.)
Обозначим начальную концентрацию HI через С (моль/л). Если к моменту наступления равновесия из каждых С молей йодоводорода диссоциировало х молей, то при этом, согласно уравнения реакции, образовалось 0,5 молей водорода и йода соответственно. Таким образом, равновесные концентрации составляют: [HI]=(C – x) моль/л; [H2] = [I2] = 0,5х моль/л
Подставим эти значения в выражение константы равновесия реакции:
Кравн =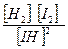
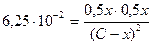 , х = 0,333
, х = 0,333
если С – 100%, то х=33,3%
Ответ:33,3%
Пример 5.В каком направлении сместится равновесие в системах: а) СО(г.) Сl2(г.) ↔ СОСl2(г.); б) 2HI(г.) ↔ H2(г.) I2(г.), если при неизменной температуре увеличить давление газовой смеси.
Решение.а) Протекание реакции в прямом направлении приводит к уменьшению общего числа молей газов, т.е. к уменьшению давления в системе. Поэтому, согласно принципу Ле-Шателье, повышение давления вызовет смещение равновесия в сторону прямой реакции.
б) Протекание реакции не сопровождается изменением числа молей газов, и изменение давления не вызовет смещение равновесия в системе.
Пример 6.Используя справочные данные, найти значение температуры, при которой константа равновесия реакции образования водяного газа: С(графит) Н2О(г.) ↔ СО(г.) Н2(г.) равна единице.
Решение.Из уравнения 1пКравн= — ∆Gp,T / (R ∙ T) следует, что при Кравн=1 стандартная энергия Гиббса химической реакции равна нулю. Тогда из соотношения ∆G0T = ∆H0T — T∆S0T вытекает, что Т = ∆H0T / ∆S0T. Воспользовавшись табличными данными находим, что ∆Н = 131,3 кДж, а ∆S = 0,1336 кДж/К, отсюда Т = 131,3 / 0,1336 = 983 К.
Ответ:983 К.
Контрольные вопросы
47. Во сколько раз изменится скорость реакции: 2А(г.) В(г.) → А2В(г.), если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 2 раза? В каком направлении сместится равновесие данной реакции с повышением давления?
48. Во сколько раз следует увеличить концентрацию вещества В в системе: 2А(г.) В2(г.)→ 2АВ(г.), чтобы при уменьшении концентрации вещества А в 4 раза скорость реакции не изменилась?
49. В каком направлении произойдет смещение равновесия при повышении температуры систем: СОСl2 ↔ CO Cl2, ∆H = -113 кДж; 2SO3 = 2SO2 O2, ∆H = 192 кДж?
50. В 2 сосуда одной и той же вместимости помещены: в первый – 1 моль газа А и 2 моля газа В, во второй – 2 моля газа А и 1 моль газа В при одинаковой температуре. Будет ли различаться скорость реакции между газами А и В в этих сосудах, если скорость реакции выражается: а) уравнением U1= k 1[А][В]; б) уравнением U2 = k2[А]2[В] ?
51. Как изменится скорость реакции: NO(г.) О2(г.) → NO2(г.), если а) увеличить давление в системе в 3 раза; б) уменьшить объем системы в 3 раза; в) повысить концентрацию NO в 3 раза?
52. Чему равен температурный коэффициент скорости реакции, если при увеличении температуры на 30 градусов скорость реакции увеличивается в 15,6 раза?
53. Вычислите, во сколько раз возрастает скорость химической реакции при увеличении температуры на 40 0С, если температурный коэффициент этой реакции равен 3.
54. Температурный коэффициент скорости некоторой реакции равен 2,3. Во сколько раз увеличится скорость реакции при повышении температуры на 25 градусов.
55. Некоторая реакция при температуре 25 0С завершается за два часа. Через какое время закончится эта реакция при температуре 75 0С, если ее температурный коэффициент равен двум.
56. В системе: А(г.) 2В(г.) → С(г.) равновесные концентрации равны: [А] = 0,06 моль/л; [В] = 0,12 моль/л; [С] = 0,216 моль/л. Найдите константу равновесия реакции.
57. Рассчитайте константу равновесия реакции: SO3(г.) ↔ SO2(г.) О2(г.), пользуясь справочными данными ∆G.
58. Реакция восстановления диоксида углерода углем выражается уравнением: СО2(г) С(тв.) = 2СО(г), DH= -172,6 кДж. В какую сторону сместится равновесие в системе при повышении температуры; нарушится ли равновесие при увеличении давления?
59. Во сколько раз следует увеличить давление газовой смеси, чтобы скорость образования АВ по реакции 2А В Û 2АВ возросла в 1000 раз?
60. Константа равновесия реакции: FеО(к.) СО(г.) ↔ Fе(к.) СО2(г.) при некоторой температуре равна 0,5. Найдите равновесные концентрации
61. Вычислите равновесные концентрации водорода и йода если известно, что их начальные концентрации составляли 0,02 моль/л, а равновесная концентрация НI – 0,03 моль/л. Вычислите константу равновесия.
62. В какую сторону сместится равновесие в системе N2 3Н2 Û 2NН3 ; DH= -92,4 кДж при понижении давления ? Ответ дайте на основании принципа Ле Шателье и подтвердите расчетом скоростей прямой и обратной реакцией при условии, что давление понизилось в 3 раза.
63. Химическое равновесие реакции разложения оксида азота (IV) до оксида азота (II) и кислорода установилось при следующих концентрациях: [NО2] = 0,06 моль/л, [NО] = 0,24 моль/л и [О2] = 0,12 моль/л. Рассчитайте константу равновесия данной реакции и исходную концентрация оксида азота (IV).
64. Как изменится скорость химической реакции: С(т.) H2(г.) ↔ CH4(г), если концентрацию водорода уменьшить в 3 раза?
65. В каком направлении сместится равновесие: Н2(г.) О2(г.) ↔ Н2О(г.), ∆Н0 = -483,6 кДж а) при повышении давления; б) при повышении температуры. Ответ обоснуйте.
66. В каком направлении сместится равновесие: СаСО3(к.) ↔ СаО(к.) СО2(г.) ∆Н0= 179 кДж а) при повышении давления; б) при повышении температуры. Ответ обоснуйте.
67. В каком направлении сместится равновесие СО(г.) О2(г.) ↔ СО2(г.), ∆Н0= –556 кДж а) при понижении температуры; б) при повышении давления. Ответ обоснуйте.
68. В каком направлении сместится равновесие N2(г.) О2(г.) ↔ NО(г.), ∆Н0= 180 кДж а) при понижении температуры; б) при повышении давления. Ответ обоснуйте.
69. Вычислите температуру, при которой константа равновесия реакции NО2(г.) ↔ N 2О4(г.) равна единице. В каком направлении сместится равновесие при температуре более низкой, чем полученная.
70. Найдите температуру, при которой константа равновесия реакции НСl(г.) О2(г.) ↔ Н2О(г.) Сl2(г.) равна единице.
Дата добавления: 2022-02-16; просмотров: 27 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.017 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
Химическое обменное взаимодействие ионов растворенной соли с водой, приводящее к образованию слабодиссоциирующих продуктов (молекул слабых кислот или оснований, анионов кислых или катионов основных солей) и сопровождающееся изменением рН среды, называется гидролизом.
Пример 1. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN, б) Nа2СО3, в) ZnSО4. Определите реакцию среды растворов этих солей.
Решение:
а) Цианид калия KCN — соль слабой одноосновной кислоты HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К и анионы CN—. Катионы К не могут связывать ионы ОН— воды, так как КОН — сильный электролит. Анионы CN— связывают ионы Н воды, образуя молекулы слабого электролита HCN. Соль гидролизуется, как говорят, по аниону. Ионно-молекулярное уравнение гидролиза:
CN— Н2О Û HCN ОН—,
или в молекулярной форме:
KCN H2O Û HCN KOH
В результате гидролиза в растворе появляется некоторый избыток ионов ОН—, поэтому раствор KCN имеет щелочную реакцию (pH>7).
б) Карбонат натрия Na2CО3 — соль слабой многоосновной кислоты и сильного основания. В этом случае анионы СО32-, связывая водородные ионы воды, образуют анионы кислой соли НСО3— , а не молекулы Н2СО3, так как ионы НСО3— диссоциируют гораздо труднее, чем молекулы Н2СО3. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
СО32- Н2О Û НСО3— ОН—,
или в молекулярной форме
Na2CО3 H2O Û NaHCO3 NaOH
В растворе появляется избыток ионов ОН—, поэтому раствор Na2CO3 имеет щелочную реакцию (рН> 7).
в) Сульфат цинка ZnSО4 — соль слабого многоосновного основания Zn(OH)2 и сильной кислоты H2SO4. В этом случае Zn2 связывают гидроксидные ионы воды, образуя катионы основной соли ZnOH . Образование молекул Zn(OH)2 не происходит, так как ионы ZnOН диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
Zn2 H2O Û ZnOH Н ,
или в молекулярной форме
2ZnSО4 2H2O Û (ZnOH)2SО4 H2SО4.
В растворе появляется избыток ионов водорода, поэтому раствор ZnSО4 имеет кислотную реакцию (рН<7).
Общая жесткость воды выражается суммой миллиграмм — эквивалентов ионов Са2 и Мg2 (иногда Fe2 ), содержащихся в 1 л воды (мг-экв/л). Один миллиграмм-эквивалент жесткости отвечает содержанию 20,04 мг/л Са2 или 12,16 Мg2 .
Пример 2. Определение общей жесткости воды по количеству содержащихся в воде солей. Рассчитайте общую жесткость воды (в мг-экв/л), если в 0,25 л воды содержится 16,20 мг гидрокарбоната кальция, 2,92 мг гидрокарбоната магния, 11,10 мг хлорида кальция и 9,50 мг хлорида магния.
Решение. Общая жесткость данного образца воды равна сумме временной и постоянной жесткости и обусловливается содержанием в ней солей, придающих ей жесткость.
Определяем эквивалентные массы солей обусловливающих жесткость воды (расчет эквивалентных масс через молекулярные массы (используя таблицу Менделеева)):
для Са(НСО3)2 Э = М/2 = (40 (1 12 16∙3)∙2)/2=162,11/2 = 81,05 г/моль;
для Mg(HCO3)2 Э = М/2 = 146,34/2 = 73,17 г/моль;
для CaCl2 Э = М/2 = 110,99/2 = 55,49 г/моль;
для MgCl2 Э = М/2 = 95,21/2 = 47,60 г/моль.
Жесткость воды Ж выражается в миллиграмм-эквивалентах двухзарядных катионов металлов Ca2 , Mg2 , Fe2 и других или соответствующих им солей, содержащихся в 1 л воды:
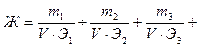 …,
…,
где m1, m2, m3 – содержание в воде двухзарядных катионов металлов (или соответствующих им солей), мг; Э1, Э2, Э3 – эквиваленты катионов металлов (или соответствующих им солей); V – объем воды, л.
 мг-экв/л.
мг-экв/л.
Пример 3. Сколько граммов CaSО4 содержится в 1 м3воды, если ее жесткость, обусловленная присутствием этой соли, равна 4 мг-экв/л?
Решение. Мольная масса CaSО4 136,14 г/моль; эквивалентная масса равна 136,14/2=68,07 г/моль. В 1 м3 воды жесткостью 4 мг-экв/л содержится 4•1000= 4000 мг-экв, или 4000·68,07=272280 мг = 272,280 г CaSО4.
Пример 4. Определение временной и постоянной жесткости воды по количеству реагентов, необходимых для устранения жесткости. Для устранения общей жесткости по известково-содовому методу к 50 л воды добавлено 7,4 г Ca(OH)2 и 5,3 г Na2CO3. Рассчитайте временную и постоянную жесткость воды.
Решение. Добавление к воде Ca(OH)2 может устранить временную жесткость, а добавление Na2CO3 – постоянную жесткость. При добавлении этих реагентов к воде происходят следующие химические реакции:
Me(HCO3)2 Ca(OH)2 = ¯MeCO3 ¯CaCO3 2H2O
Me(NO3)2 Na2CO3 = ¯MeCO3 2NaNO3
(Me2 : Ca2 , Mg2 , Fe2 и др.)
Временная жесткость воды Жвр измеряется числом миллиграмм-эквивалентов гидроксида кальция, участвующего в реакции, а постоянная жесткость Жпост – числом миллиграмм-эквивалентов карбоната натрия:
Жвр = mCa(OH)2/(ЭCa(OH)2 V); Жпост = mNa2CO3/(ЭNa2CO3V);
ЭCa(OH)2 = М/2 = 74,09/2 = 37,04 г/моль;
ЭNa2CO3 = М/2 = 106,00/2 = 53,00 г/моль;
Жвр = 7400/(37,04·50) = 4 мг-экв/л;
Жпост = 5300/(53,00·50) = 2 мг-экв/л.
Общая жесткость воды равна
Жобщ = Жвр Жпост = 4 2 = 6 мг-экв/л (вода средней жесткости).
Контрольные вопросы.
71. К раствору Nа2СО3 добавили cледующие вещества:
а) НСl, б) NaOH, в) Сu(NO3)2, г) K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза соответствующих солей.
72. К раствору А12(SO4)3 добавили следующие вещества:
a) H2SO4, б) КОН, в) Na2SO3, г) ZnSO4. В каких случаях гидролиз сульфата алюминия усилится? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза соответствующих солей.
73. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: FeCl3 или FeCl2? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза этих солей.
74. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: NaCN или NaClO? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза этих солей.
75. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: MgCl2 или ZnCl2? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза этих солей.
76. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: Na2CO3 или Na2SO3? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза этих солей.
77. К раствору FeCl3, добавили следующие вещества: а) НС1, б) КОН, в) ZnCl2, г) Na2CO3. В каких случаях гидролиз хлорида железа (III) усилится? Почему? Составьте молекулярные и ионно-молекулярные уравнения гидролиза соответствующих солей.
78. Присутствие каких солей обусловливает жесткость природной воды? Как можно устранить карбонатную и некарбонатную жесткость воды? Рассчитайте сколько граммов Са(НСО3)2 содержится в 1м3 воды, жесткость которой равна 3 мг-экв/л.
79. Определите карбонатную жесткость воды, в 1л которой содержится по 100 мг Са(НСО3)2, Mg(HCO3)2 и Fe(HCO3)2.
80. Сколько гашеной извести необходимо прибавить к 1 м3 воды, чтобы устранить ее временную жесткость, равную 7,2 мг-экв/л?
81. Устранение временной жесткости 100 л воды, вызванной присутствием Mg(HCO3)2, потребовало 4 г NaOH. Составить уравнение реакции и рассчитать, чему равна жесткость воды.
82. Определите жесткость воды, в литре которой содержится 0,324 г гидрокарбоната кальция. Сколько граммов соды нужно прибавить к 2 м3 этой воды для устранения ее жесткости?
83. В чем сущность ионитного способа устранения жесткости воды? Рассчитайте жесткость воды, содержащей в 1 л 0,005 моля гидрокарбоната кальция.
84. Жесткая вода содержит в литре 50 мг Са(НСО3)2 и 15 мг CaSO4. Сколько граммов карбоната натрия потребуется для устранения жесткости 1 м3 этой воды?
85. Некарбонатная жесткость воды равна 3,18 мг-экв/л. Какую массу Na3PO4 нужно добавить, чтобы умягчить 1 м3 воды?
86. Вычислите жесткость воды, если в литре воды содержится 202,5 мг Ca(HCO3)2 и 285 мг MgCl2.
87. Определить, чему равна жесткость воды, в 1 л которой содержится 240 мг MgSO4. Сколько граммов соды потребуется прибавить к 100 л этой воды для устранения жесткости?
88. Рассчитайте, сколько должна весить накипь, выпавшая при выпаривании 100 л воды, если жесткость обусловлена только присутствием гидрокарбоната кальция и равна 5 мг-экв/л?
Дата добавления: 2022-02-16; просмотров: 139 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.024 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
При решении данного раздела см. в Приложении табл.3 «Стандартные электродные потенциалы ( 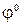 ) некоторых металлов (ряд напряжений)»
) некоторых металлов (ряд напряжений)»
Если металлическую пластину опустить в воду, то катионы металла на её поверхности гидратируются полярными молекулами воды и переходят в жидкость. При этом электроны, в избытке остающиеся в металле, заряжают его поверхностный слой отрицательно. Возникает электростатическое притяжение между перешедшими в жидкость гидратированными катионами и поверхностью металла. В результате этого в системе устанавливается подвижное равновесие:
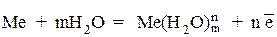 ;
;
в растворе на металле
где n — число электронов, принимающих участие в процессе. На границе металл-жидкость возникает двойной электрический слой, характеризующийся определенным скачком потенциала – электродным потенциалом. Абсолютное значение электродных потенциалов измерить не удается. Электродные потенциалы зависят от ряда факторов (природы металла, концентрации, температуры и др.). Поэтому обычно определяют относительные электродные потенциалы в определенных условиях – так называемые стандартные электродные потенциалы ( 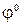 ).
).
Стандартным электродным потенциалом металла называют его электродный потенциал, возникающий при погружении металла в раствор собственного иона с концентрацией (или активностью), равной 1 моль/л, измеренный по сравнению со стандартным водородным электродом, потенциал которого при 25оС условно принимается равным нулю ( 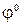 =0;
=0;  ).
).
Располагая металлы в ряд по мере возрастания их стандартных электродных потенциалов ( 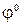 ), получаем так называемый ряд напряжений.
), получаем так называемый ряд напряжений.
Положение того или иного металла в ряду напряжений характеризует его восстановительную способность, а также окислительные свойства его ионов в водных растворах при стандартных условиях. Чем меньше значение 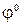 , тем большими восстановительными способностями обладает данный металл в виде простого вещества и тем меньшие окислительные способности проявляют его ионы, и наоборот. Электродные потенциалы измеряются в приборах, которые получили название гальванических элементов. Окислительно-восстановительная реакция, которая характеризует работу гальванического элемента, протекает в направлении, в котором ЭДС элемента имеет положительное значение. В этом случае
, тем большими восстановительными способностями обладает данный металл в виде простого вещества и тем меньшие окислительные способности проявляют его ионы, и наоборот. Электродные потенциалы измеряются в приборах, которые получили название гальванических элементов. Окислительно-восстановительная реакция, которая характеризует работу гальванического элемента, протекает в направлении, в котором ЭДС элемента имеет положительное значение. В этом случае 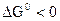 , так как
, так как 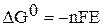 , где n — число электронов, принимающих участие в процессе; F – число Фарадея; Е – ЭДС гальванического элемента. Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода:
, где n — число электронов, принимающих участие в процессе; F – число Фарадея; Е – ЭДС гальванического элемента. Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода:
 .
.
Пример 1.Стандартный электродный потенциал никеля больше, чем кобальта (см. табл.3). Изменится ли это соотношение, если изменить потенциал никеля в растворе его ионов с концентрацией 0,001 моль/л, а потенциалы кобальта – в растворе с концентрацией 0,1 моль/л?
решение:электродный потенциал металла ( 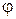 ) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
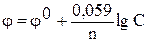 ,
,
где 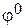 – стандартный электродный потенциал; n — число электронов, принимающих участие в процессе; С – концентрация (при точных вычислениях — активность) гидратированных ионов металла в растворе, моль/л;
– стандартный электродный потенциал; n — число электронов, принимающих участие в процессе; С – концентрация (при точных вычислениях — активность) гидратированных ионов металла в растворе, моль/л; 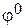 для никеля и кобальта соответственно равны –0,250 и –0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
для никеля и кобальта соответственно равны –0,250 и –0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
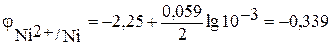 В,
В,
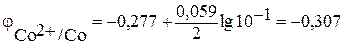 В.
В.
Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Пример2. Магниевую пластинку опустили в раствор его соли. При этом электродный потенциал магния оказался равен –2,363В. Вычислите концентрацию ионов магния (в моль/л).
Решение. Подобные задачи также решаются на основании уравнения Нернста (см. пример 1):

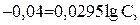
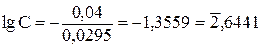 ,
,
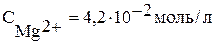 .
.
Пример 3.Составьте схему гальванического элемента, в котором электродами являются магниевая и цинковая пластинки, опущенные в растворы их ионов с активной концентрацией 1 моль/л. Какой металл является анодом, какой катодом? Напишите уравнение окислительно-восстановительной реакции, протекающей в этом гальваническом элементе, и вычислите его ЭДС.
Решение. Схема данного гальванического элемента
(-) Mg | Mg2 || Zn2 | Zn ( ).
Вертикальной линией обозначается поверхность раздела между металлом и раствором, а двумя – границу раздела двух жидких фаз – пористую перегородку (мили соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,363 В) и является анодом,на котором протекает окислительный процесс:
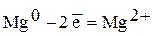 (1).
(1).
Цинк, потенциал которого –0,763 В, — катод, т.е. электрод на котором протекает восстановительный процесс:
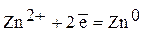 (2).
(2).
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента/, можно получить, сложив электронные уравнения анодного (1) и катодного(2) процессов:
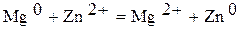 .
.
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода. Так как концентрация ионов в растворе равна 1 моль/л, то ЭДС элемента равна разности стандартных потенциалов двух его электродов:
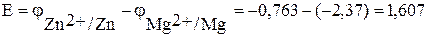 В.
В.
Контрольные вопросы
97. Рассчитайте ЭДС элемента Zn 2Ag «Zn2 2Ag, в котором при 298К установилось равновесие. Цинковый и серебряный электроды опущены в растворы их солей с активной концентрацией их ионов 1 моль/л. Напишите для данного гальванического элемента электронные уравнения реакций, протекающих на аноде и катоде. Составьте схему.
98. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один никелевый электрод находится в 0,001 М растворе, а другой такой же электрод в 0,01 М растворе сульфата никеля.
99. рассчитайте стандартную ЭДС элемента, в котором установилось равновесие: Mg Zn2 «Mg2 Zn; aZn2 =10-2 моль/л, àMg2 =10-3 моль/л. Напишите электронные уравнения электронных процессов.
100. Рассчитайте ЭДС элемента, в котором при 298К установилось равновесие: Cd Cu2 «Cd2 Cu; à Cu2 =10-3 моль/л, аCd2 =10-2 моль/л. Напишите электронные уравнения электродных процессов.
101. Рассчитайте ЭДС элемента, в котором при 298К установилось равновесие: Fe 2Ag «Fe2 2Ag, при аFe2 =10-2моль/л, аAg =10-3моль/л. Напишите электронные уравнения электродных процессов.
102. Составьте схему элемента при аАg =10-1моль/л у одного электрода и aАg =10-4 моль/л у другого электрода. Укажите, какой из электродов будет анодом, а какой катодом. Рассчитайте ЭДС элемента.
103. Составьте схему элемента при aZn2 =10-2 моль/л у одного электрода и aZn2 =10-6 моль/л у другого электрода. Укажите, какой из электродов будет анодом, а какой катодом. Рассчитайте ЭДС элемента.
104. Определите активность ионов Cu2 в растворе, в котором установилось равновесие: Zn Cu2 «Zn2 Cu, если при 298 К ЭДС элемента равна 1,16 В и aZn2 =10-2 моль/л. Напишите уравнения электродных процессов.
105. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из алюминиевых электродов, опущенных: первый в 0,01 М, второй — в 0,1 М раствора Al(NO3)3.
106. Гальванический элемент составлен из стандартного цинкового электрода и хромового электрода, погруженного в раствор, содержащий ионы Cr3 . Определите концентрацию ионов Cr3 , если ЭДС этого гальванического элемента равна 0.
107.Вычислите ЭДС гальванического элемента, составленного из стандартного водородного электрода и цинкового электрода, погруженного в раствор ZnSO4, в котором концентрация ионов [Zn2 ]=0,01моль/л. Составьте электронные уравнения процессов, происходящих на электродах при работе этого элемента.
108.При какой концентрации ионов алюминия значение потенциала алюминиевого электрода становится равным стандартному потенциалу водородного электрода. Составьте схему гальванического элемента и уравнения электродных процессов.
109.Составьте схему, напишите электронные уравнения электродных процессов, вычислите ЭДС медно-кадмиевого гальванического элемента, в котором Cd2 = 0,1 моль/л, а Cu2 = 0,01 моль/л.
110. Никелевый и кобальтовый электроды опущены соответственно в растворы Ni(NO3)2 и Co(NO3)2. В каком соотношении должна быть концентрация ионов этих металлов, чтобы потенциалы обоих электродов были одинаковыми? Составьте схему гальванического элемента и уравнения электродных процессов.
111. Гальванический элемент составлен из стандартного водородного электрода и медного электрода, погруженного в раствор своей соли с концентрацией [Cu2 ]=0,1моль/л. Составьте схему, напишите электронные уравнения электродных процессов и вычислите эдс этого гальванического элемента.
112. Составьте схему гальванического элемента, состоящего из пластин свинца и цинка, погруженных в растворы солей. Напишите электронные уравнения электродных процессов. Какой концентрации надо взять ионы цинка (в моль/л), чтобы ЭДС элемента стала равной нулю, если [Рв2 ]=0,01 моль/л.
113. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из пластин кадмия и магния, погруженных в растворы своих солей с концентрацией 0,1 моль/л.
114. Вычислите ЭДС гальванического элемента, состоящего из стандартного водорода и магниевого электрода, погруженного в раствор MgCl2, в котором [Mg2 ]=0,001моль/л. Составьте электронные уравнения электродных процессов.
115. Составьте схему, напишите электронные уравнения электродных процессов, вычислите ЭДС медно-кадмиевого гальванического элемента, в котором Cd2 = 1 моль/л, а Cu2 = 0,001 моль/л.
116. Гальванический элемент составлен из стандартного цинкового электрода и хромового электрода, погруженного в раствор, содержащий ионы Cr3 . Определите концентрацию ионов Cr3 , если ЭДС этого гальванического элемента равна 0.
Дата добавления: 2022-02-16; просмотров: 174 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.011 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
Пример 1.Какая масса меди выделяется на катоде при электролизе раствора CuSO4 в течение 1 ч при силе тока 4A, если выход по току равен 100%? Приведите схему электролиза раствора сульфата меди.
Решение.Согласно законам Фарадея
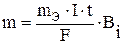 , (1)
, (1)
где m – масса вещества, окисленного или восстановленного на электроде; mэ – эквивалентная масса вещества; I – сила тока, А; t – продолжительность электролиза, с; F – число Фарадея, равное 96500 кл ; Вi – выход по току, % .
эквивалентная масса меди в CuSO4 равна:

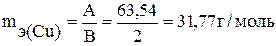 ,
,
где А – атомная масса меди, В – валентность меди.
Подставив в формулу (1) значения mэ=31,77 г/моль, I = 4 А, t = 3600 с, Вi=1, получим
 .
.
схема электролиза раствора сульфата меди:
Пример 2. Вычислите эквивалентную массу металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 кл электричества и на катоде выделяется 11,742 г металла.
Решение.Изформулы (1) 

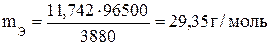 , где
, где
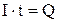 -количество электричества, Кл.
-количество электричества, Кл.
Пример 3.Какие реакции протекают на электродах при электролизе раствора К2SO4, Чемуравна сила тока при электролизе раствора в течении 1 ч 40 мин 25 с , если на катоде выделилось 1,4 л водорода?
Решение. Преобразуем формулу (1) 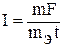 , так как дан объем водорода, то отношение
, так как дан объем водорода, то отношение  заменяем отношением
заменяем отношением 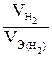 , где
, где 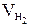 -объем водорода, л;
-объем водорода, л; 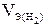 = 11,2 л/моль эквивалентный объем водорода, t = 6025 c (1 ч 40 мин 25 с= 6025 c). Тогда:
= 11,2 л/моль эквивалентный объем водорода, t = 6025 c (1 ч 40 мин 25 с= 6025 c). Тогда:
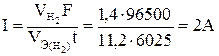
В водном растворе сульфата калия протекают реакции диссоциации по уравнениям: 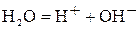 и
и 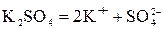
схема электролиза раствора сульфата калия:
На аноде выделяется кислород, так как ион 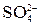 в этих условиях не окисляется. на катоде выделяется водород, так как стандартный потенциал калия (щелочной металл) более отрицателен, чем потенциал водородного электрода (см. в Приложении табл.3 «Стандартные электродные потенциалы (
в этих условиях не окисляется. на катоде выделяется водород, так как стандартный потенциал калия (щелочной металл) более отрицателен, чем потенциал водородного электрода (см. в Приложении табл.3 «Стандартные электродные потенциалы ( 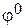 ) некоторых металлов (ряд напряжений)» и в водных растворах разряд этих ионов на катоде не происходит.
) некоторых металлов (ряд напряжений)» и в водных растворах разряд этих ионов на катоде не происходит.
Контрольные вопросы.
117. Определите массу хрома, которая выделится на катоде при электролизе сульфата хрома в течение 3-х часов при токе 13,4 А, если выход хрома по току равен 50%. Приведите схему электролиза раствора сульфата хрома.
118. Какие реакции протекают на электродах при электролизе раствора сульфата цинка: а) с графитовым анодом; б) с цинковым анодом. Как изменится концентрация ионов цинка в растворе в обоих случаях, если через раствор пропустить ток силой 26,8 А в течение 1 часа. Выход по току на катоде цинка 50%, на аноде — 100%.
119. При пропускании тока, силой 2 А в течение 1 часа 14 мин 24 с через водный раствор хлорида металла (II) на одном из графитовых электродов выделился металл массой 2,94 г. Чему равна атомная масса металла, если выход по току 100%, и что это за металл. Напишите уравнения реакций, протекающих на электродах.
120. При пропускании тока, силой 2 А в течение 1 часа 14 мин 24 с через водный раствор хлорида металла (II) на одном из графитовых электродов выделился металл массой 2,94 г. Чему равна атомная масса металла, если выход по току 100%, и что это за металл. Напишите уравнения реакций, протекающих на электродах.
121. При электролизе сульфата натрия получили при н. у. Н2 объемом 448 л. Напишите уравнение реакций, протекающих на нерастворимых аноде и катоде и рассчитайте, сколько времени протекал электролиз, если ток был 100 А.
122. При электролизе раствора сульфата меди на аноде выделился кислород
объемом 560 мл, измеренный при н. у. Сколько граммов меди выделилось на катоде? Приведите схему электролиза.
123. Электролиз раствора сульфата цинка проводили с нерастворимым анодом в течении 6,7 часов, в результате чего выделился кислород объемом 5,6 л, измеренный при н. у. Вычислите ток и массу осажденного цинка при выходе его по току 70%. Приведите схему электролиза.
124. Напишите уравнение реакций, протекающих на нерастворимых электродах при электролизе водного раствора КОН. Какие вещества и в каком объеме можно получить при н. у., если пропустить ток 13,4 А в течении 2-х часов.
125. Напишите уравнение реакций, протекающих на графитовых электродах при электролизе: а) расплава MgCl2, б) раствора MgCl2. Сколько времени необходимо вести электролиз при токе 2 А, чтобы на катоде выделилось вещество массой 2,43 г (для реакций а) и б) ).
126. Через раствор PbSO4 пропущено 2 F электричества. Как изменится количество Pb2 в растворе, если электроды: а) графитовые, б) свинцовые. Выход по току свинца составляет на катоде 50%, на аноде — 100%.
127. Найти эквиваленты олова, зная, что при токе, силой 2,5 А из раствора SnCl2 за 30 минут выделяется 2,77 г олова. Написать схему электролиза раствора SnCl2.
128. При электролизе водного раствора Cr2(SO4)3 током, силой 2 А масса катода увеличилась на 8 г. В течении какого времени проводили электролиз? Составьте электронные уравнения процессов, происходящих при электролизе.
129. Сколько времени пропускали ток силой 8 А через раствор сульфата никеля, если масса никелевого анода стала на 0,8805 г меньше? (Написать схему электролиза сульфата никеля).
130. Составьте уравнения реакций происходящих при электролизе: а) раствора NaBr; б) расплава NaBr. Рассчитайте массу веществ, которые выделяются на электродах при прохождении 3,2 А.ч электричества.
131. Напишите уравнения реакций, протекающих на электродах при электролизе водного раствора нитрата меди: а) с графитовым анодом, б) с медным анодом. Рассчитайте массу веществ, выделившихся на электродах в случаях а и б при нахождении 6А в течении 2-х часов.
132. При электролизе водного раствора сульфата хрома (III) током силой 2 А масса катода увеличилась на 8 г. В течение какого времени проводили электролиз, если выход по току составляет 50%. Составьте схему электролиза соли.
133. При электролизе раствора CuSO4 на аноде выделилось 168 см3 газа (н.у.) Составьте электронные уравнения процессов, происходящих на электродах, и вычислите, какая масса меди выделилась на катоде.
134. В какой последовательности выделяются на катоде металлы при электролизе раствора, содержащего ионы Ni2 , Cu2 , Ag , Fe2 . Составьте схему электродных процессов при электролизе водного раствора NiSO4. Сколько граммов никеля выделится на катоде, если на процесс затрачено 13,4 А×ч. Выход по току никеля составляет 80%.
135. Электролиз раствора К2SО4 проводили с нерастворимыми электродами при токе 2,68А в течении 1 часа. Составьте уравнения процессов, происходящих на электродах, вычислите объем выделяющихся при н.у. на электродах веществ.
136. Рассчитайте выход по току кадмия, если при электролизе раствора CdCl2 в течении 1 часа на катоде выделился кадмий массой 5,62 г, а ток был равен 5,36А. Приведите схему электролиза CdCl2.
137. Напишите уравнение реакций, протекающих на нерастворимых электродах при электролизе водного раствора КОН. Какие вещества и в каком объеме можно получить при н. у., если пропустить ток 13,4 А в течении 3-х часов.
138. При электролизе раствора CuSO4 на аноде выделилось 334 см3 газа (н.у.) Составьте электронные уравнения процессов, происходящих на электродах, и вычислите, какая масса меди выделилась на катоде.
139. Напишите уравнения реакций, протекающих на электродах при электролизе водного раствора нитрата свинца: а) с графитовым анодом, б) со свинцовым анодом. Рассчитайте массу веществ, выделившихся на электродах в случаях а и б при нахождении 6А в течении 2-х часов.
140. При электролизе раствора сульфата меди на аноде выделился кислород
объемом 1120 мл, измеренный при н. у. Сколько граммов меди выделилось на катоде? Приведите схему электролиза.
Дата добавления: 2022-02-16; просмотров: 140 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.032 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
Ионы или молекулы, которые восстанавливаются на катоде, называются деполяризаторами. При атмосферной коррозии – коррозии во влажном воздухе при комнатной температуре – деполяризатором является кислород.
Пример 1.Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворе. Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Решение.Цинк имеет более отрицательный потенциал (-0,763 В), чем кадмий (-0,403 В), поэтому он является анодом, а кадмий — катодом.
Так как ионы Zn2 с гидроксильной группой образуют нерастворимый гидроксид, то продуктом коррозии будет Zn(ОН)2.
Контрольные вопросы.
141. Две цинковые пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. Какая из этих пластинок быстрее подвергается коррозии? Почему? составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок.
142. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары Mg — Pb.
143. Составьте электронные уравнения коррозии железа, покрытого цинком, и железа, покрытого свинцом в кислой среде и во влажном воздухе.
144. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии Al — Pb.
145. Составьте электронные уравнения анодного и катодного процессов коррозии никеля, покрытого медью при нарушении покрытия во влажном воздухе и в соляной кислоте.
146. Какие процессы возможны при контакте железа с раствором соляной кислоты. Какие методы защиты железа от коррозии можно рекомендовать в этом случае. Напишите уравнения процессов.
147. В раствор соляной кислоты поместили две алюминиевых пластинки, одна из которых частично покрыта медью. В каком случае процесс коррозии алюминия происходит интенсивнее. Составьте электронные уравнения анодного и катодного процессов. Ответ мотивируйте.
148. В раствор электролита, содержащего растворенный кислород, опустили две цинковых пластинки, одна из которых частично покрыта медью. В каком случае процесс коррозии цинка происходит интенсивнее. Составьте электронные уравнения анодного и катодного процессов.
149. Объясните, почему в атмосферных условиях железо коррозирует, а золото нет. Объяснение подтвердите расчетами.
150. Железное изделие покрыли свинцом. Какое это покрытие? Анодное или катодное? Почему? Составьте уравнения анодного и катодного процессов коррозии этого изделия при нарушении целостности покрытия во влажном воздухе и в растворе соляной кислоты. Какие продукты коррозии образуются в первом и втором случаях.
151. Какое покрытие металла называется анодным, а какое катодным. Назовите металлы, которые можно использовать для анодного и катодного покрытия железа во влажном воздухе и в сильно кислой среде. Напишите уравнения процессов, протекающих при коррозии луженого железа.
152. В чем сущность протекторной защиты металлов от коррозии. Приведите пример протекторной защиты железа в электролите, содержащем растворенный кислород. Составьте уравнение анодного и катодного процессов.
153. Медь не вытесняет водород из разбавленных кислот. Почему? Однако, если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинается бурное выделение водорода. Объясните это явление, составьте уравнение анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
154. Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении целостности покрытия. Составьте уравнение анодного и катодного процессов.
155. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары Mg — Ni.
156. Составьте электронные уравнения коррозии железа, покрытого магнием, и железа, покрытого свинцом в кислой среде и во влажном воздухе.
157. Составьте электронные уравнения катодного и анодного процессов с кислородной и водородной деполяризацией при коррозии пары Al – Ni
158. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина. Почему. Составьте электронные уравнения катодного и анодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа.
159. Как протекает атмосферная коррозия железа, покрытого слоем серебра, если покрытие нарушено. Составьте электронные уравнения катодного и анодного процессов. Каков состав продуктов коррозии
160. Составьте электронные уравнения процессов, происходящих при коррозии сплава Sn-Zn в кислой среде и во влажном воздухе.
161. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары Mg — Zn.
162. Составьте электронные уравнения коррозии железа, покрытого алюминием, и железа, покрытого никелем в кислой среде и во влажном воздухе.
163. Составьте электронные уравнения катодного и анодного процессов с кислородной и водородной деполяризацией при коррозии пары Al – Pb.
Дата добавления: 2022-02-16; просмотров: 64 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.018 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав
§
| Порядко- вый номер элемента | Периоды | Элемент | Потенциал иониза- ции, эВ | Электро-отрицатель-ность, эВ |
| I | H | 2,15 | ||
| He | 24,48 | — | ||
| II | 5,37 | |||
| Be | 9,3 | 1,5 | ||
| B | 8,28 | 2,0 | ||
| C | 11,24 | 2,5 | ||
| N | 12,54 | 3,0 | ||
| O | 13,61 | 3,5 | ||
| F | 17,42 | 4,0 | ||
| Ne | 21,55 | — | ||
| III | Na | 5,14 | 0,9 | |
| Mg | 7,64 | 1,2 | ||
| Al | 7,98 | 1,5 | ||
| Si | 8,14 | 1,8 | ||
| P | 10,55 | 2,1 | ||
| S | 10,35 | 2,5 | ||
| Cl | 13,01 | 3,0 | ||
| Ar | 15,75 | — | ||
| IV | K | 4,23 | 0,8 | |
| Ca | 6,11 | 1,0 | ||
| Sc | 6,56 | 0,9 | ||
| Ti | 6,73 | 1,5 | ||
| V | 6,74 | 1,6 | ||
| Cr | 6,76 | 1,6 | ||
| Mn | 7,43 | 1,5 | ||
| Fe | 7,90 | 1,8 | ||
| Co | 7,89 | 1,7 | ||
| Ni | 7,63 | 1,8 | ||
| Cu | 7,72 | 1,9 | ||
| Zn | 9,39 | 1,6 | ||
| Ga | 6,00 | 1,6 | ||
| Ge | 7,88 | 2,0 | ||
| As | 9,81 | 2,0 | ||
| Se | 9,75 | 2,4 | ||
| Br | 11,84 | 2,9 | ||
| Kr | 13,99 | 2,9 | ||
| V | Rb | 4,18 | 0,8 | |
| Sr | 5,69 | 1,0 | ||
| Y | 6,38 | 1,2 | ||
| Zr | 6,83 | 1,4 | ||
| Nb | 6,88 | 1,6 | ||
| Mo | 7,13 | 1,8 | ||
| Tc | 7,23 | 1,9 | ||
| Ru | 7,36 | 2,2 | ||
| Rh | 7,46 | 2,2 | ||
| Rd | 8,33 | 2,2 | ||
| Ag | 7,57 | 1,9 | ||
| Cd | 8,99 | 1,7 | ||
| Zn | 5,78 | 1,7 | ||
| Sn | 7,33 | 1,8 | ||
| Sb | 8,64 | 1,9 | ||
| Te | 9,01 | 2,1 | ||
| I | 10,44 | 2,5 | ||
| Xe | 12,12 | — | ||
| VI | Cs | 3,78 | 0,7 | |
| Ba | 5,81 | 0,9 | ||
| La | 5,61 | 0,9 | ||
| Hf | 5,5 | 1,3 | ||
| Ta | 7,7 | 1,5 | ||
| W | 7,98 | 1,7 | ||
| Re | 7,87 | 1,9 | ||
| Os | 8,7 | 2,2 | ||
| Ir | 9,2 | 2,2 | ||
| Pt | 8,96 | 2,2 | ||
| Au | 9,22 | 2,4 | ||
| Hg | 10,43 | 1,9 | ||
| Tl | 6,1 | 1,8 | ||
| Rb | 7,41 | 1,8 | ||
| Bi | 7,27 | 1,9 | ||
| Po | 8,2 | 2,0 | ||
| At | 9,2 | 2,2 | ||
| Rn | 10,74 | — | ||
| VII | Fr | 3,98 | 0,7 | |
| Ra | 5,27 | 0,9 | ||
| Ac | 6,89 | 1,1 | ||
| Ku | — | — |
Таблица 2.
Стандартные теплоты ( энтальпия ) образования DН0298;
энтропии S0298 и энергии Гиббса образования D G0298
Некоторых веществ
| Вещество | DН0298 кДж/моль | S0298 Дж ( моль ×К ) | DG0298 кДж/моль |
| Простые вещества | |||
| Ag(к) | 42,55 | ||
| Аl( к) | 28,33 | ||
| Br( г) | 152,21 | ||
| C( графит) | 5,74 | ||
| Cl( г) | 222,95 | ||
| Cu | 33,14 | ||
| Fe( к) | 27,15 | ||
| H2( г) | 130,52 | ||
| Hg(ж) | 75,90 | ||
| Mg( к) | 32,68 | ||
| N2( г) | 191,50 | ||
| О2(г) | 205,04 | ||
| S(к, ромб.) | 32,9 | ||
| Ti(k) | 30,6 | ||
| Неорганические соединения | |||
| Ag2O(к) | -31,1 | 121,0 | -11,3 |
| AgNO3 (к) | -124,5 | 140,9 | -33,6 |
| Al2O3( к) | -1676 | 49,9 | -1582 |
| Al2(SO4)3 (к) | -3442 | 239,2 | -3101 |
| В2Н6 ( г) | 38,5 | 232,0 | 89,6 |
| BaCO3(к) | -1202 | 112,1 | -1164,8 |
| ВaO( к) | -553,54 | 70,29 | -525,84 |
| Ba (OH)2(к) | -943,49 | 100,83 | -855,42 |
| CO( г) | -110,53 | 197,55 | -137,15 |
| CO2(г) | -393,51 | 213,66 | -394,37 |
| CaO( к) | -635,09 | 38,07 | -603,46 |
| CaCO3 (к) | -1206,83 | 91,71 | -1128,35 |
| Ca(OH)2 | -985,12 | 83,39 | -897,52 |
| CS2 | 88,7 | 151,0 | 64,4 |
| C2H2 | 226,75 | 200,82 | 209,20 |
| CrCl3(к) | -556,47 | 123,01 | -486,37 |
| FeO(к) | -264,8 | 60,75 | -244,3 |
| Fe2O3(к) | -822,16 | 87,45 | -740,34 |
| Fe3O4(к) | -1117,1 | 146,2 | -1014,2 |
| Fe(OH)2(к) | -561,7 | 88,0 | -479,7 |
| Fe(OH)3(к) | -826,6 | 105,0 | -699,6 |
| HCl( г) | -92,31 | 186,79 | -95,30 |
| H2O( к) | -291,85 | (39,33) | — |
| H2O( ж) | -285,83 | 69,95 | -237,23 |
| H2O( г) | -241,81 | 188,72 | -228,61 |
| Н2О2(ж) | -187,8 | 109,5 | -120,4 |
| HCN( г ) | 135,0 | 113,1 | 125,5 |
| H2SO4(ж) | -813,99 | 156,90 | -690,14 |
| HNО3(ж) | -173,00 | 156,16 | -79,90 |
| HgCl2 | -229,00 | 242,3 | -197,4 |
| HgO(к) красн. | -90,9 | 70,29 | -58,6 |
| HgS(к)α | -59,0 | 82,4 | -51,4 |
| KCl( к) | -436,68 | 82,55 | -408,93 |
| K2Cr2O7(к) | -2067,27 | 291,21 | -1887,85 |
| KMnO4(к) | -828,89 | 171,54 | -729,14 |
| KNO3 (к) | -493,2 | 132,93 | -393,1 |
| K2SO4(к) | -1433,69 | 175,56 | -1316,04 |
| MnO2(к) | -521,49 | 53,14 | -466,68 |
| MgC( к) | -601,49 | 27,07 | -569,27 |
| MnSO4(к) | -3089,50 | 348,1 | -2635,1 |
| NH3(г) | -46,2 | 192,5 | -16,7 |
| NH4Cl( к) | -314,2 | 94,5 | -203,2 |
| N2H4( г) | -50,50 | 12,1 | 149,2 |
| NaBr | -151,86 | 62,1 | — |
| NO( г) | 91,26 | 210,64 | 87,58 |
| NO2(г) | 240,2 | 51,5 | |
| NaOH( ж) | -426,35 | 64,43 | -380,29 |
| Na2SO3( к) | -1089,43 | 146,02 | -1001,21 |
| Na2SO4(к) | -4324,75 | 591,87 | -3644,09 |
| Pb3O4(к) | -723,41 | 211,29 | -606,17 |
| PbCl2(к) | -359,82 | 135,98 | -314,56 |
| PbО2(к) | -276,56 | 71,92 | -217,55 |
| Pb(NO3)2 (к) | -451,7 | 217,9 | -256,9 |
| SO2 (г) | -296,90 | 248,1 | -300,21 |
| SO3 (ж) | -439,0 | -368,4 | |
| TiO2(к) | -938,6 | 49,92 | -883,3 |
| ZnO(к) | -350,6 | 43,64 | -320,7 |
| Zn(NO3)2(к)· 6H2O | -2306,8 | 462,3 | -1174,9 |
| Zn(NO3)2(к) | -483,7 | — | — |
Таблица 3
Стандартные электродные потенциалы ( j 0 )
Дата добавления: 2022-02-16; просмотров: 15 | Нарушение авторских прав
lektsii.net — Лекции.Нет — 2022-2022 год. (0.026 сек.)
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав

