- 2 какие из перечисленных ниже названий соответствуют формуле н2o: оксид водорода, гидрид кислорода, пероксид водорода, водород, вода, кислородный водород?
- Водородные соединения металлов
- Водородные соединения. оксиды
- Летучие водородные соединения
- Положение в периодической системе химических элементов
- Применение водорода
- Соединения водорода
- Способы получения
- Способы получения аммиака
- Способы получения сероводорода
- Способы получения силана
- Способы получения фосфина
- Строение и физические свойства
- Физические свойства
- Химические свойства
- Химические свойства прочих водородных соединений
- Химические свойства сероводорода
- Химические свойства силана
- Химические свойства фосфина
- Электронное строение водорода
2 какие из перечисленных ниже названий соответствуют формуле н2o: оксид водорода, гидрид кислорода, пероксид водорода, водород, вода, кислородный водород?
Н2O — оксид водорода, вода, гидрид кислорода.

Решебник
по
химии
за 8 класс (О.С.Габриелян, 2022 год),
задача №2
к главе «Глава 3. Соединения химических элементов. § 18. Важнейшие классы бинарных соединений — оксиды и летучие водородные соединения».
Все задачи
Водородные соединения металлов
Соединения металлов с водородом — солеобразные гидриды МеНх. Это твердые вещества белого цвета с ионным строением. Устойчивые гидриды образуют активные металлы (щелочные, щелочноземельные и др.).
Водородные соединения. оксиды
На этом уроке учащиеся на наглядных примерах разберут отличия водородных соединений и оксидов, научатся называть и составлять их формулы, изучат свойства наиболее распространенных оксидов и водородных соединений. Благодаря иллюстрациям и разнообразным примерам ученикам понравится изложение нового материала.
Само
название «водородные соединения» говорит о том, что в состав данных
соединений входит водород. К таким соединениям относятся гидриды и
летучие водородные соединения. Давайте разберемся, в чем их отличие.
Гидриды
– это бинарные соединения металлов I
и
II A
групп
с водородом. Например: CaH2,
NaH, BaH2,
LiH. Все эти гидриды твердые,
нелетучие, тугоплавкие вещества с ионным типом связи.
Летучие
водородные соединения – это бинарные соединения неметаллов с
водородом. Эти соединения могут быть как жидкостями (например, Н2О),
так игазами (HCl,
NH3).
Рассмотрим
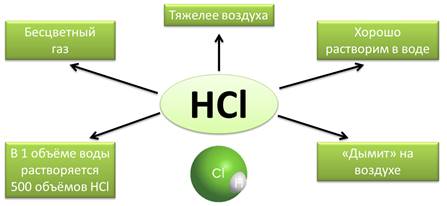
свойства хлороводорода – HCl.
Это бесцветный газ, тяжелее воздуха, хорошо растворим в воде. В 1 объёме
воды растворяется 500 объёмов хлороводорода. Хлороводород «дымит» на
воздухе, т.е. он поглощает пары воды из воздуха, образуя при этом туманное
облако.
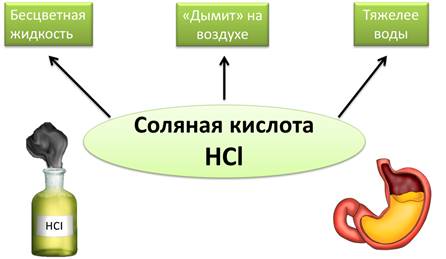
Раствор
хлороводорода в воде называют соляной кислотой. Это бесцветная
жидкость, «дымит» на воздухе, тяжелее воды. Соляная кислота содержится в
желудочном соке человека и некоторых животных.
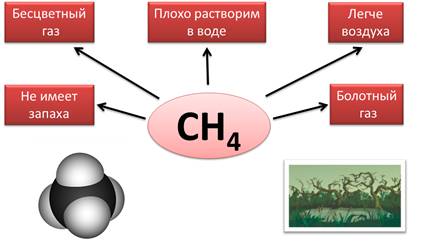
Еще
одни важным летучим водородным соединением является метан – СН4.
Метан – бесцветный газ, плохо растворим в воде, легче воздуха, не имеет
запаха. Его еще называют болотным газом, т.к. он образуется на дне болот
и водоемов при разложении растительных остатков без доступа кислорода. Кроме
того, метан содержится в природном и попутном нефтяном газе.
Известным
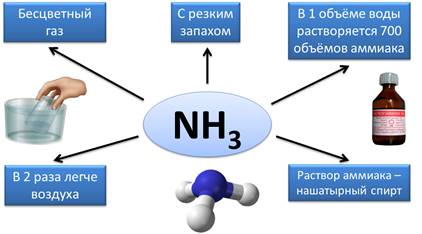
и распространенным водородным соединением является аммиак – NH3.
Аммиак является бесцветным газом, имеет резкий запах, в 1 объёме воды растворяется
700 объёмов аммиака, он почти в 2 раза легче воздуха. Раствор аммиака в воде
называют нашатырным спиртом, который широко используют в медицине.
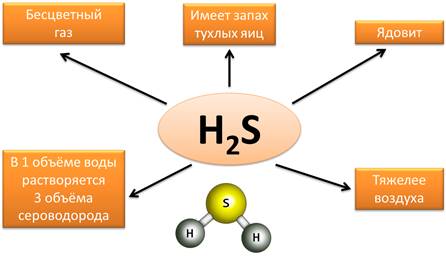
Сероводород
– H2S
– тоже известное летучее водородное соединение. Он является бесцветным газом,
имеет запах тухлых яиц, ядовит, в 1 объеме воды растворяется 3 объёма
сероводорода, он тяжелее воздуха.
Оксиды
Оксиды
–
это сложные вещества, состоящие из двух элементов, одним из которых является
кислород в степени окисления -2.
В
названии оксидовсначала указывают слово оксид в
именительном падеже (от лат. названия кислорода – «оксигениум»), а затем
название элемента в родительном падеже.

Например:
CaO –оксид
кальция, K2O
– оксид калия, Al2O3
– оксид алюминия. А если элемент имеет несколько степеней
окисления или переменную валентность, то после названия оксида в скобках
римскими цифрами указывают численное значение степени окисления. Например: Fe2O3
– оксид железа (III)
(читается:
«оксид железа три»), CuO
– оксид меди (II)
(читается: «оксид меди два»), CrO3
– оксид хрома (VI)
(читается: «оксид хрома шесть»).
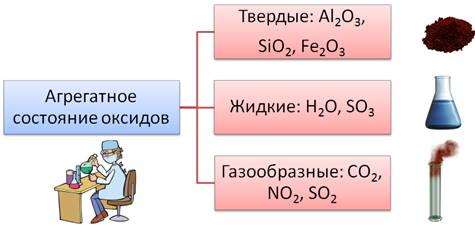
По
агрегатному состоянию оксиды делят натвёрдые: к ним
относятся такие оксиды, как Al2O3,
SiO2,
Fe2O3 и
др., жидкие оксиды – это H2O,
SO3,
газообразными являются такие оксиды, как СО2, NO2,
SO2 и
др.
Познакомимся
с вами с наиболее важными оксидами.
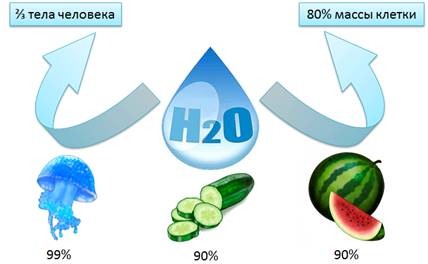
Вода
– Н2О – самое распространенное и самое
необходимое вещество на планете. Почти ¾ поверхности земного шара
занято водой. Однако, это вода морей и океанов, которая является солёной.
Она непригодна для питья, для сельского хозяйства, для промышленности. Кроме
того, тело человека на 2/3 состоит из воды. Вода составляет до 80%
массы клетки и выполняет важные функции: защитную, транспортную и др. У
некоторых медуз вода занимает почти 99% от массы тела. Содержание воды в
огурцах и арбузах превышает 90%. Большинство реакций и процессов в различных
отраслях промышленности тоже протекают в растворах. Однако запасы пресной воды
малы, всего 3% от общего объёма, поэтому нужно беречь и экономить воду.
Без воды невозможно представить жизнь человека, который потребляет ее для
бытовых нужд.
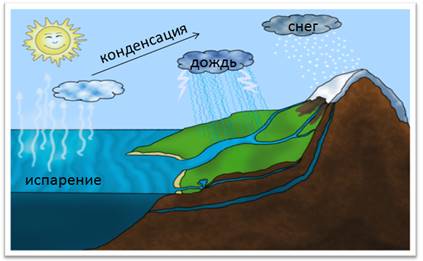
В
природе постоянно происходит круговорот воды. Под влиянием солнечного
тепла часть воды испаряется в атмосферу. При охлаждении воздуха образуются
водяные капельки, из которых состоят облака. Эти мелкие капельки сливаются в
более крупные и выпадают на землю в виде осадков: снега, дождя, града.
Круговорот
воды в природе
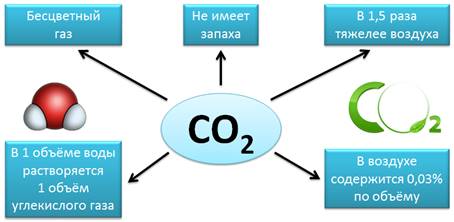
Еще
одним известным оксидом является диоксид углерода, углекислый газ, или оксид
углерода (IV)
– CO2.
Это бесцветный газ, не имеет запаха, в 1,5 раза тяжелее воздуха. В 1
объёме воды растворяется 1 объем углекислого газа. В воздухе содержится
0,03% (по объему) диоксида углерода.
Большое
количество углекислого газа вызывает удушье. Например, в «Собачьей
пещере» вблизи Неаполя, известной еще из древности, заходившие сюда собаки
постоянно погибали из-за скопившегося газа, который стелется по дну пещеры
слоем до полуметра. Углекислый газ образуется при дыхании, сгорании топлива,
тлении и гниении различных организмов. Большое содержание углекислого газа
в минеральной воде «Нарзан», находящейся в Кисловодске. Углекислый газ
используют для получения газированных вод, а твердый диоксид углерода, или«сухой лед» используют для хранения продуктов питания, в частности
мороженого. Т.к. углекислый газ не поддерживает горение, его используют
для тушения пожаров. В медицине углекислый газ используют для углекислотных
ванн.
Негашеная
известь, или СаО, является белым, тугоплавким веществом,
которое энергично реагирует с водой, при этом образуется гашеная известь.
Негашеная известь применяется для получения вяжущих строительных материалов.
Основная
часть литосферы – это оксид кремния (IV)
– SiO2.
Он входит в состав минералов и горных пород. Этот оксид образует кварц,
кварцевый песок, кремнезем, горный хрусталь и др. соединения.
Еще
одно соединение, которое является основой литосферы – это оксид алюминия – Al2O3.
Он также входит в состав минералов и горных пород. Этот оксид образует
корунд, рубин, сапфир, каолин и др. соединения.
Летучие водородные соединения
Соединения водорода с неметаллами — летучие водородные соединения.
Положение в периодической системе химических элементов
Водород расположен в главной подгруппе I группы и в первом периоде периодической системы химических элементов Д.И. Менделеева.
Применение водорода
Применение водорода основано на его физических и химических свойствах:
- как легкий газ, он используется для наполнения аэростатов (в смеси с гелием);
- кислородно-водородное пламя применяется для получения высоких температур при сварке металлов;
- как восстановитель используется для получения металлов (молибдена, вольфрама и др.) из их оксидов;
- водород используется для получения аммиака и искусственного жидкого топлива;
- получение твердых жиров (гидрогенизация).
Соединения водорода
Основные степени окисления водорода 1, 0, -1.
Типичные соединения водорода:
| Степень окисления | Типичные соединения |
| 1 | кислоты H2SO4, H2S, HCl и др. вода H2O и др. летучие водородные соединения (HCl, HBr) кислые соли (NaHCO3 и др.) основания NaOH, Cu(OH)2 основные соли (CuOH)2CO3 |
| -1 | гидриды металлов NaH, CaH2 и др. |
Способы получения
Еще один важный промышленный способ получения водорода — паровая конверсия метана. При взаимодействии перегретого водяного пара с метаном образуется угарный газ и водород:
СН4 Н2O → СО 3Н2
Также возможна паровая конверсия угля:
C0 H2 O → C 2O H20
Способы получения аммиака
В лаборатории аммиак получают при взаимодействии солей аммония с щелочами. Поскольку аммиак очень хорошо растворим в воде, для получения чистого аммиака используют твердые вещества.
Например, аммиак можно получить нагреванием смеси хлорида аммония и гидроксида кальция. При нагревании смеси происходит образование соли, аммиака и воды:
2NH4Cl Са(OH)2 → CaCl2 2NH3 2Н2O
Тщательно растирают ступкой смесь соли и основания и нагревают смесь. Выделяющийся газ собирают в пробирку (аммиак — легкий газ и пробирку нужно перевернуть вверх дном). Влажная лакмусовая бумажка синеет в присутствии аммиака.
Видеоопытполучения аммиака из хлорида аммония и гидроксида кальция можно посмотреть здесь.
Еще один лабораторныйспособ получения аммиака – гидролиз нитридов.
Например, гидролиз нитрида кальция:
Ca3N2 6H2O → ЗСа(OH)2 2NH3
В промышленности аммиак получают с помощью процесса Габера: прямым синтезом из водорода и азота.
N2 3Н2 ⇄ 2NH3
Процесс проводят при температуре 500-550оС и в присутствии катализатора. Для синтеза аммиака применяют давления 15-30 МПа. В качестве катализатора используют губчатое железо с добавками оксидов алюминия, калия, кальция, кремния. Для полного использования исходных веществ применяют метод циркуляции непрореагировавших реагентов: не вступившие в реакцию азот и водород вновь возвращают в реактор.
Более подробно про технологию производства аммиака можно прочитать здесь.
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например, при действии соляной кислоты на сульфид железа (II):
FeS 2HCl → FeCl2 H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
S H2 → H2S
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопытполучения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: хлорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
2CrCl3 3Na2S 6H2O → 2Cr(OH)3 3H2S↑ 6NaCl
Способы получения силана
Силан образуется при взаимодействии соляной кислоты с силицидом магния:
Mg2Si 4HCl → 2MgCl2 SiH4
Видеоопытполучения силана из силицида магния можно посмотреть здесь.
Способы получения фосфина
В лаборатории фосфин получают водным или кислотным гидролизом фосфидов – бинарных соединений фосфора и металлов.
Например, фосфин образуется при водном гидролизе фосфида кальция:
Ca3P2 6H2O → 3Са(ОН)2 2PH3
Или при кислотном гидролизе, например, фосфида магния в соляной кислоте:
Mg3P2 6HCl → 3MgCl2 2PH3↑
Еще один лабораторныйспособ получения фосфина – диспропорционирование фосфора в щелочах.
Например, фосфор реагирует с гидроксидом калия с образованием гипофосфита калия и фосфина:
4P 3KOH 3H2O → 3KH2PO2 PH3↑
Строение и физические свойства
Все летучие водородные соединения — газы (кроме воды).
| CH4 — метан | NH3 — аммиак | H2O — вода | HF –фтороводород |
| SiH4 — силан | PH3 — фосфин | H2S — сероводород | HCl –хлороводород |
| AsH3 — арсин | H2Se — селеноводород | HBr –бромоводород | |
| H2Te — теллуроводород | HI –иодоводород |
Физические свойства
Молекулы воды связаны водородными связями: nH2O = (Н2O)n, поэтому вода жидкая в отличие от ее газообразных аналогов H2S, H2Se и Н2Те.
Химические свойства
1. Вода реагирует с металлами и неметаллами.
1.1. С активными металлами вода реагирует при комнатной температуре с образованием щелочей и водорода:
2Na 2H2O → 2NaOH H2
- с магнием реагирует при кипячении:
Mg 2H2O → Mg(OH)2 H2
- алюминий не реагирует с водой, так как покрыт оксидной плёнкой. Алюминий, очищенный от оксидной плёнки, взаимодействует с водой, образуя гидроксид:
2Al 6H2O = 2Al(OH)3 3H2
- металлы, расположенные в ряду активности от Al до Н, реагируют с водяным паром при высокой температуре, образуя оксиды и водород:
Fe 4Н2O → Fe3O4 4Н2
- металлы, расположенные в ряду активности от после Н, не реагируют с водой:
Ag Н2O ≠
2.Вода реагирует с оксидами щелочных и щелочноземельных металлов, образуя щелочи (с оксидом магния – при кипячении):
Н2O СаО = Са(OH)2
3.Вода взаимодействует с кислотными оксидами (кроме SiO2):
P2O5 3H2O = 2H3PO4
4.Некоторые соли реагируют с с водой. Как правило, в таблице растворимости такие соли отмечены прочерком:
Например, сульфид алюминия разлагается водой:
Al2S3 6H2O → 2Al(OH)3 3H2S
5.Бинарные соединения металлов и неметаллов, которые не являются кислотами и основаниями, разлагаются водой.
Например, фосфид кальция разлагается водой:
Са3Р2 6Н2О → 3Са(ОН)2 2РН3↑
6.Бинарные соединения неметаллов также гидролизуются водой.
Например, фосфид хлора (V) разлагается водой:
PCl5 4H2O → H3PO4 5HCl
6.Некоторые органические вещества гидролизуются водой или вступают в реакции присоединения с водой (алкены, алкины, алкадиены, сложные эфиры и др.).
Химические свойства прочих водородных соединений
Кислотыобразуют в водном растворе: водородные соединения VIA (кроме воды) и VIIA подгрупп.
Прочитать про химические свойства галогеноводородов вы можете здесь.
Химические свойства сероводорода
1.В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например, сероводород реагирует с гидроксидом натрия:
H2S 2NaOH → Na2S 2H2OH2S NaOH → NaНS H2O
2.Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
2H2S O2 → 2S 2H2O
В избытке кислорода:
2H2S 3O2 → 2SO2 2H2O
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S Br2 → 2HBr S↓
H2S Cl2 → 2HCl S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
H2S 4Cl2 4H2O → H2SO4 8HCl
Например, азотная кислота окисляет сероводород до молекулярной серы:
H2S 2HNO3(конц.) → S 2NO2 2H2O
При кипячении сера окисляется до серной кислоты:
H2S 8HNO3(конц.) → H2SO4 8NO2 4H2O
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например, оксид серы (IV) окисляет сероводород:
2H2S SO2 → 3S 2H2O
Соединения железа (III) также окисляют сероводород:
H2S 2FeCl3 → 2FeCl2 S 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
3H2S K2Cr2O7 4H2SO4 → 3S Cr2(SO4)3 K2SO4 7H2O
2H2S 4Ag O2 → 2Ag2S 2H2O
Серная кислота окисляет сероводород либо до молекулярной серы:
H2S H2SO4(конц.) → S SO2 2H2O
Либо до оксида серы (IV):
H2S 3H2SO4(конц.) → 4SO2 4H2O
4.Сероводород в растворе реагирует с растворимыми солями тяжелых металлов: меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например, сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
H2S Pb(NO3)2 → PbS 2HNO3
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопытвзаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Химические свойства силана
1.Силан — неустойчивое водородное соединение (самовоспламеняется на воздухе). При сгорании силана на воздухе образуется оксид кремния (IV) и вода:
SiН4 2О2 = SiO2 2Н2О
Видеоопытсгорания силана можно посмотреть здесь.
2. Силан разлагается водой с выделением водорода:
SiH4 2H2O → SiO2 4H2
3. Силан разлагается (окисляется) щелочами:
SiH4 2NaOH H2O → Na2SiO3 4H2
4. Силан при нагревании разлагается:
SiH4 → Si 2H2
Химические свойства фосфина
1.В водном растворе фосфин проявляет очень слабые основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H ), он превращается в ион фосфония. Основные свойства фосфина гораздо слабее основных свойств аммиака. Проявляются при взаимодействии с безводными кислотами.
Например, фосфин реагирует с йодоводородной кислотой:
PH3 HI → PH4I
Соли фосфония неустойчивые, легко гидролизуются.
2.Фосфин PH3 – сильный восстановитель за счет фосфора в степени окисления -3. На воздухе самопроизвольно самовоспламеняется:
2PH3 4O2 → P2O5 3H2O
PH3 2O2 → H3PO4
3. Как сильный восстановитель, фосфин легко окисляется под действием окислителей.
Например, азотная кислота окисляет фосфин. При этом фосфор переходит в степень окисления 5 и образует фосфорную кислоту.
PH3 8HNO3 → H3PO4 8NO2 4H2O
Серная кислота также окисляет фосфин:
PH3 3H2SO4 → H3PO4 3SO2 3H2O
С фосфином также реагируют другие соединения фосфора, с более высокими степенями окисления фосфора.
Например, хлорид фосфора (III) окисляет фосфин:
2PH3 2PCl3 → 4P 6HCl
Электронное строение водорода
Электронная конфигурация водорода в основном состоянии:
1H 1s1 1s ![]()
Атом водорода содержит на внешнем энергетическом уровне один неспаренный электрон в основном энергетическом состоянии.
Степени окисления атома водорода — от -1 до 1. Характерные степени окисления -1, 0, 1.

