Пропан C3H8 – это предельный углеводород, содержащий три атома углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, нерастворим в воде и не смешивается с ней.
Алканы – это предельные углеводороды, содержащие только одинарные связи между атомами С–С в молекуле, т.е. содержащие максимальное количество водорода.
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Языки:
|
|
|
Применить к найденному
Общее число найденных записей: 1.
Показано записей: 1.
- Жидкость или газ
- Что такое пропан и бутан и как их получают
- Чем алканы отличаются от других химических соединений
- Получение пропана в промышленности
- Химические свойства алканов
- В чем разница между бутаном и пропаном
- Изомерия пропана
- Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- Синтез Фишера-Тропша
- Гомологический ряд алканов
- Пропан
- Варианты формулы:
- Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- Термические травмы
- Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование пропана
- Преимущества газовых смесей с пропаном
- Синтез Фишера-Тропша
- Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование алканов
- Реакции окисления алканов
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- Строение пропана
- Можно ли смешивать пропан и сжиженный газ?
- Структурная изомерия
- Номенклатура алканов
- Что лучше использовать в качестве топлива
- Химические свойства пропана
- Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
- Гидрирование алкенов и алкинов
- Электролиз солей карбоновых кислот (электролиз по Кольбе)
- Пропан — это жидкость или газ?
- Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- Как используют пропан и бутан
- Токсичность
- Строение алканов
- Оптическая изомерия
- Взрывоопасность
- Изомеризация алканов
- Реакции разложения
- 2.1. Дегидрирование и дегидроциклизация
- 2.2. Пиролиз (дегидрирование) метана
- 2.3. Крекинг
- Гомологический ряд пропана
- Опасность и поражающие факторы
- Дегидрирование пропана
- Получение алканов в промышленности
- Немного физики
- Окисление пропана
- 3.1. Полное окисление – горение
- Различие между жидким и газообразным пропаном
Жидкость или газ

Популярный горючий углеводород с формулой C3H8 образуется при переработке нефти. Он имеет невысокую себестоимость и хорошую теплоотдачу, практичен для использования в быту и на производстве. Пропан называют газом, но хранится он как жидкость: в герметичных резервуарах. На самом деле это соединение объединяет свойства обоих агрегатных состояний, переходя из одного в другое при изменении окружающих условий.
Что такое пропан и бутан и как их получают
Пропан и бутан, как и все алканы, – это горючие вещества, которые используются в качестве топлива. Однако из-за разных физических свойств они имеют разную специализацию. Пропан и бутан – это гомологи метана.
Их можно получить из природного сырья – например, газа, горного воска или нефти. Кроме того, пропан и бутан можно синтезировать из смеси оксида углерода и водорода.
Лабораторным путем бутан и пропан получают с помощью каталитического гидрирования пропена, пропина, бутена и бутина, а также по реакции Вюрца.
04.10.2021
Время чтения: минут
- Оглавление статьи:
- Чем алканы отличаются от других химических соединений
- Что такое пропан и бутан и как их получают
- Как используют пропан и бутан
- В чем разница между бутаном и пропаном
- Что лучше использовать в качестве топлива: пропан или бутан
Бутан и пропан – это химические углеводородные соединения, которые имеют как сходства, так и различия. Основным сходством является их гомологическое родство и их принадлежность к классу алканов, которые также известны как «парафины». В данной статье мы расскажем о том, что такое пропан и бутан; к какому классу химических соединений они относятся; в чем их основные сходства и различия; а также расскажем, какое топливо лучше всего выбрать для заправки газгольдеров.
Чем алканы отличаются от других химических соединений
«Парафины» – это химические соединения, которые имеют низкую реакционную способность. Алканы не растворяются в воде и не имеют какого-либо цвета. При горении алканы выделяют очень много тепла, а пламя их – бесцветное или светло-голубое. Этот класс соединений активно применяют в промышленности, в частности – при синтезировании топлива и нефти.
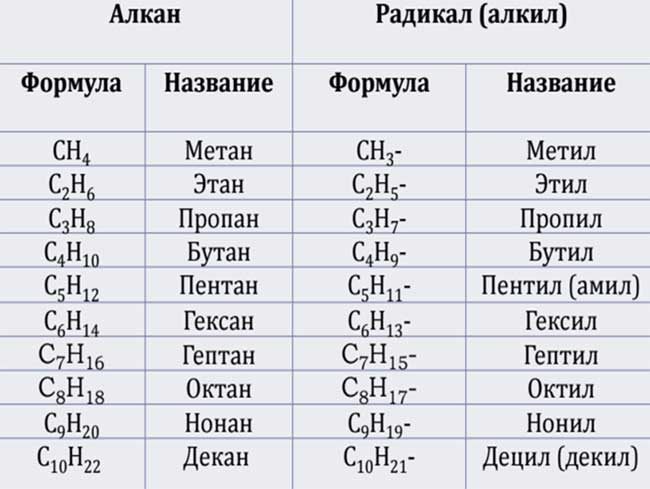
В таблице вы можете увидеть список веществ, которые относятся к классу алканов.
Получение пропана в промышленности
В промышленности пропан получают из нефти, каменного угля, природного и попутного газа. При переработке нефти используют ректификацию, крекинг и другие способы.
Химические свойства алканов
Алканы – предельные углеводороды, поэтому они не могут вступать в реакции присоединения.
Для предельных углеводородов характерны реакции:
- разложения,
- замещения,
- окисления.
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для алканов характерны только радикальные реакции.
Алканы устойчивы к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагируют с концентрированными кислотами, щелочами, бромной водой.
В чем разница между бутаном и пропаном
Пропан имеет химическую формулу С3Н8, а бутан — С4Н10. Эти газы имеют похожий молекулярный вес и теплопроводность. Основным отличием этих алканов друг от друга является их температура кипения.
Температура кипения бутана составляет около -1 градуса по Цельсию, тогда как у пропана этот показатель равен -43 градусам по Цельсию. При достижении этих значений бутан и пропан переходят из газообразного состояние в состояние жидкости, т.е. сжижаются.
Из этого складывается и разная специфика использования этих газов.
Бутан менее устойчив к воздействию низких температур, поэтому его сложно эксплуатировать в холодное время года.
У пропана же другой значимый недостаток – его опасно использовать как топливо при воздействии высоких температур. При нагреве пропан расширяется и давит на стенки газгольдера или баллона. Это может привести к появлению трещины стенок сосуда и к его взрывы.

Пропан более взрывоопасен, так как не выдерживает длительное воздействие высоких температур.
Изомерия пропана
Для пропана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Декарбоксилирование солей карбоновых кислот (реакция Дюма)
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия:

Синтез Фишера-Тропша
Из синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды:
nCO + (3n+1)H2 = CnH2n+2 + nH2O
Это промышленный процесс получения алканов.
Из угарного газа и водорода можно получить пропан:
3CO + 7H2 = C3H8 + 3H2O
Гомологический ряд алканов
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Все алканы легче воды, не растворимы в воде и не смешиваются с ней.
Пропан
Брутто-формула:
C3H8
CAS# 74-98-6
Категории:
Алканы
PubChem CID: 6334
| ChemSpider ID: 6094
| CHEBI:32879
| CB2194886
Названия
Русский:
- Пропан(IUPAC) [Wiki]
English:
- EINECS:270-653-6
- Propane(IUPAC) [Wiki]
Варианты формулы:
CH3-CH2-CH3
H-C-C-C-H; H|#2|H; H|#3|H; H|#4|H
/\
$slope(45)H|C<_(A170,d+)H><`/wH>\C<`/wH><\dH>/C<\wH><_(A10,d+)H>`|H
H3C/\CH3
Вещества, имеющие отношение…
Предыдущий гомолог:
Этан
Следущий гомолог:
Бутан
Химический состав
Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета.
Например, хлорметан реагирует с натрием с образованием этана:
![]()
Хлорэтан взаимодействует с натрием с образованием бутана:
![]()
Реакция больше подходит для получения симметричных алканов.
При проведении синтеза со смесью разных галогеналканов образуется смесь разных алканов.
Например, при взаимодействии хлорметана и хлорэтана с натрием помимо пропана образуются этан и бутан.
![]()
Термические травмы
Попадая на кожу, например при заправке сжиженного топлива в баллон, пропан приводит к образованию ожогов. Повреждение это носит термический, а не химический характер, как склонны думать многие обыватели. При переходе из жидкой фазы в газообразную, пропан отдаёт внутреннюю энергию в окружающее пространство и, как следствие, резко становится холодным. Владельцы баллонов, наверняка, могли наблюдать, как охлаждается и покрывается изморозью газовой редуктор в их домашней сети.
Ожог пропаном характеризуется покраснением, жжением, частичным онемением поражённого участка. В серьезных случаях появляются волдыри, и может начаться некроз тканей. К счастью, для удаления ожогов хорошо подходит медикаментозное лечение.
Похожие статьи
- Какой газовый баллон выбрать?
- Как подключить к плите газовый баллон
- Виды газовых горелок
Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Пропан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании пропана образуется смесь хлорпроизводных.
Например, при хлорировании пропана образуются 1-хлорпропан и 2-хлопропан:

Бромирование протекает более медленно и избирательно.
Избирательность бромирования: сначала замещается атом водорода у третичного атома углерода, затем атом водорода у вторичного атома углерода, и только затем первичный атом.
С третичный–Н > С вторичный–Н > С первичный–Н
Например, при бромировании пропана преимущественно образуется 2-бромпропан:
Хлорпропан может взаимодействовать с хлором и дальше с образованием дихлорпропана, трихлорпропана, тетрахлорпропана и т.д.
1.2. Нитрование пропана
Пропан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в пропане замещается на нитрогруппу NO2.
Например. При нитровании пропана образуется преимущественно 2-нитропропан:

Преимущества газовых смесей с пропаном
Области применения сжиженного пропана:
- в домашних условиях: для работ кухонных плит, отопления хозяйственных и жилых помещений;
- в качестве автомобильного топлива;
- для строительных и ремонтных работ;
- в производственных циклах различных отраслей промышленности
Так как пропан в различных условиях легко преобразуется из газа в жидкость и обратно, его очень выгодно использовать для различных нужд. Это топливо не требует применения дорогостоящих технологий изготовления, хранится в металлических баллонах различного объема, его легко транспортировать к любому месту назначения. В отличие от метана, который требует особых условий и стоит в несколько раз дороже.
Похожие статьи
- Почему газ горит желтым или красным цветом
- Как изготавливаются баллоны с пропаном
- Преимущества и недостатки тороидальных баллонов для ГБО
Синтез Фишера-Тропша
Из синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды:
nCO + (2n+1)H2 = CnH2n+2 + nH2O
Это промышленный процесс получения алканов.
Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Алканы реагируют с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:
![]()
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:

Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно.
При хлорировании алканов с углеродным скелетом, содержащим более 3 атомов углерода, образуется смесь хлорпроизводных.
Например, при хлорировании пропана образуются 1-хлорпропан и 2-хлопропан:

Бромирование протекает более медленно и избирательно.
Избирательность бромирования: сначала замещается атом водорода у третичного атома углерода, затем атом водорода у вторичного атома углерода, и только затем первичный атом.
С третичный–Н > С вторичный–Н > С первичный–Н
Например, при бромировании 2-метилпропана преимущественно образуется 2-бром-2-метилпропан:

Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:
![]()
Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:

Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:

1.2. Нитрование алканов
Алканы взаимодействуют с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140оС и под давлением. Атом водорода в алкане замещается на нитрогруппу NO2.
При этом процесс протекает также избирательно.
С третичный–Н > С вторичный–Н > С первичный–Н
Например. При нитровании пропана образуется преимущественно 2-нитропропан:

Реакции окисления алканов
Алканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.).
3.1. Полное окисление – горение
Алканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты.
CH4 + 2O2 → CO2 + 2H2O + Q
Уравнение сгорания алканов в общем виде:
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Например, горение пропана в недостатке кислорода:
2C3H8 + 7O2 → 6CO + 8H2O
Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода:
CH4 + O2 → C + 2H2O
Эта реакция используется для получения сажи.
3.2. Каталитическое окисление
- Каталитическое окисление бутана – промышленный способ получения уксусной кислоты:
![]()
- При каталитическом окислении метана кислородом возможно образование различных продуктов в зависимости от условий проведения процесса и катализатора. Возможно образование метанола, муравьиного альдегида или муравьиной кислоты:

- Важное значение в промышленности имеет паровая конверсия метана: окисление метана водяным паром при высокой температуре.
![]()
Продукт реакции – так называемый «синтез-газ».
Строение пропана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp3:

При образовании связи С–С происходит перекрывание sp3-гибридных орбиталей атомов углерода:

При образовании связи С–H происходит перекрывание sp3-гибридной орбитали атома углерода и s-орбитали атома водорода:

Четыре sp3-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109о 28′ друг к другу:

Это соответствует тетраэдрическому строению.
Например, в молекуле пропана C3H8 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет образует угол, т.е. геометрия молекулы — уголковая или V-образная.

Можно ли смешивать пропан и сжиженный газ?
Пропан и сжиженный нефтяной газ нельзя комбинировать ни в одном оборудовании. LPG не может быть заменен, если для работы газовой плиты требуется газообразный пропан. Аналогичным образом, пары пропана нельзя использовать с газовым котлом, предназначенным для сжиженного газа.
Структурная изомерия
Для алканов характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
Например.
Для н-бутана (алкана с линейной цепью) существует изомер с разветвленным углеродным скелетом – изобутан
С увеличением числа атомов углерода в молекуле увеличивается количество изомеров, соответствующих данной формуле. У метана CH4, этана C2H6 и пропана C3H8 структурных изомеров нет.
Количество изомеров в ряду алканов:
| Молекулярная формула | Число структурных изомеров |
| C4H10 | 2 |
| C5H12 | 3 |
| C6H14 | 5 |
| C7H16 | 9 |
| C8H18 | 18 |
| C9H20 | 35 |
| C10H22 | 75 |
Номенклатура алканов
В названиях алканов используется суффикс -АН.
Например, алкан имеет название 2-метилпропан.

Для простейших алканов (метан, этан, пропан, бутан и изобутан) используют тривиальные названия. Начиная с пятиатомного углероводорода, в названии неразветвленных (нормальных) алканов используют корень, который показывает число атомов углерода в молекуле, и добавляют соответствующий суффикс (для алканов – ан, для алкенов – ен, и т.д.).
Название разветвленных алканов строится по следующим правилам:
1. Выбирают главную углеродную цепь. При этом считают, что углеводородные радикалы, которые не входят в главной цепь, являются в ней заместителями. При этом главная цепь должна быть самой длинной. Например, в молекуле на рисунке главной является цепь, отмеченная на рисунке а:
Главная цепь должна быть самой разветвленной.
Например, в молекуле, изображенной на рисунках а и б, выделены цепи с одинаковым числом атомов углерода. Но главной будет цепь, изображенная на рисунке а, т.к. от нее отходит 2 заместителя, а от цепи на рисунке б – только один:
2. Нумеруют атомы углерода в главной цепи так, чтобы атомы углерода, которые соединены с заместителями, получили минимальные возможные номера. Причем нумерацию следует начинать с более близкого к старшей группе конца цепи.
3. Называют все радикалы, указывая впереди цифры, которые обозначают их расположение в главной цепи.
Например, 2-метилпропан:

Для одинаковых заместителей эти цифры указывают через запятую, при этом количество одинаковых заместителей обозначается приставками ди- (два), три- (три), тетра- (четыре), пента- (пять) и т.д.
Например, 2,2-диметилпропан или 2,2,3-триметилпентан.
4. Названия заместителей со всеми приставками и цифрами располагают в алфавитном порядке.
Например: 2,2-диметил-3-этилпентан.
5. Называют главную углеродную цепь, т.е. соответствующий нормальный алкан.
Например, название молекулы на рисунке:

2,2,4-триметил-4-этилгексан
Что лучше использовать в качестве топлива
Какой же газ лучше всего использовать при заправке газгольдера? В соответствии с ГОСТ для заправки газгольдеров допустимо использование технического пропана(ПТ), технического бутана (БТ), а также их смеси (СПБТ).
Следует помнить о том, что недопустимо использование бутан-бутиленовой фракции (ББФ), которая представляет собой дешевое низкокачественное сырье. Используя ББФ вы ускоряете процесс износа оборудования.
Какое сырье лучше использовать для заправки газгольдера зависит от климатических условий и типа газгольдера.
«Летняя» смесь от «зимней» отличается соотношением бутана и пропана. В «летней» топливе пропан составляет порядка 50 % , в том время как в «зимнем» топливе пропан составляет около 80%. Вследствие этого, «зимнее» топливо традиционно стоит дороже, чем «летнее», так как пропан – более дорогой вид газа, в отличии от бутана.
В случае с заправкой газгольдеров желание сэкономить может привести к сбою в работе оборудования. Если вы заправили газгольдер смесью, которая преимущественно состоит из бутана, вы рискуете остаться без источника тепла в периоды понижения температур.
Оптимальным решением будет заправки 50/50. В холодное время года вы можете положиться на тепло от сжигания пропана, а при потеплении – бутана.
Наши специалисты оказывают комплексные услуги по газификации объектов и помогут вам выбрать оптимальный состав топлива для газгольдера.
Химические свойства пропана
Пропан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для пропана характерны реакции:
- разложения,
- замещения,
- окисления.
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для пропана характерны радикальные реакции.
Пропан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
![]()
При гидрировании этилена образуется этан:
![]()
При полном гидрировании ацетилена также образуется этан:
![]()
При гидрировании циклопропана образуется пропан:

Гидрирование алкенов и алкинов
Пропан можно получить из пропилена или припина:
![]()
При гидрировании пропена образуется пропан:
![]()
При полном гидрировании пропина также образуется пропан:
![]()
Электролиз солей карбоновых кислот (электролиз по Кольбе)
Это электролиз водных растворов солей карбоновых кислот.
В общем виде:
2R–COONa + 2H2O → H2 + 2NaOH + 2CO2 + R–R
В водном растворе ацетат натрия практически полностью диссоциирует:
CH3COONa → CH3COO– + Na+
При этом на катод притягиваются катионы натрия Na+ и молекулы воды H2O.
Разряжаться на катоде будут молекулы воды:
Kатод(-): 2H2O + 2e = H2 + 2OH–
На аноде окисляются ацетат-ионы, а именно, атом углерода карбоксильной группы.
При этом от карбоксильной группы отрывается углекислый газ и остаются метильные радикалы, которые образуют газообразный этан:
Aнод(+): 2CH3COO– – 2e = 2CO2 + CH3–CH3
Суммарное уравнение электролиза водного раствора ацетата натрия:
2CH3COONa + 2H2O = H2 + 2NaOH + 2CO2 + CH3–CH3
Пропан — это жидкость или газ?
Пропан представляет собой легковоспламеняющийся углеводород с тремя атомами углерода и химической формулой C 3 H 8. Пропан в природе не встречается. Газ образуется как побочный продукт при переработке нефти и газа при добыче из скважин. Природный газ и сырая нефть перерабатываются для получения сжиженного нефтяного газа (LPG), который используется в качестве топлива для отопления, приготовления пищи, транспорта, промышленности и сельского хозяйства.
Хранение пропана требует сжижения. Это означает, что единственный способ хранения пропана — это превращение его в жидкость или сжиженный газ. Газ сжимается до состояния жидкости для хранения и транспортировки при температуре 0 °C и давлении 1 атм (стандартные стандартные условия). Для этого процесса требуется минимальная температура -160°C. Таким образом, LPG является очень холодным веществом, которое может нанести серьезный вред коже. Когда температура пропана поднимается выше -160°C градусов ниже нуля, он превращается из жидкости в газ или пар. Это парообразное состояние отмечает разницу между LPG и пропаном. При комнатной температуре и давлении пропан становится одновременно жидкостью и газом.
Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета.
При проведении синтеза со смесью разных галогеналканов образуется смесь разных алканов.
Например, при взаимодействии хлорметана и хлорэтана с натрием помимо пропана образуются этан и бутан.
![]()
Декарбоксилирование солей карбоновых кислот (реакция Дюма)
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
При взаимодействии бутаноата натрия с гидроксидом натрия при сплавлении образуются пропан и карбонат натрия:
CH3–CH2–CH2–COONa + NaOH → CH3–CH2–CH3 + Na2CO3
Как используют пропан и бутан
Пропан и бутан часто используют как пропеллент. Это вещества, которые создают в аэрозольных баллонах избыточное давление и позволяет вытеснить из баллона летучее(основное) вещество. Так как пропан и бутан, как и все алканы, не имеют запаха, его можно использовать в освежителях воздуха и дезодорантах. Пропан и бутан также используют в пищевой промышленности при создании холодильных установок в качества хладогентов.

Пропан и бутан используются в качестве пропеллентов в аэрозолях(освежителях воздуха, дезодорантах и средствах от насекомых).
Пропан применяют в качестве заправок не только для автомобилей, но и зажигалок, а также как топливо в портативных электрогенераторах.
Бутан имеет менее разноплановую специализацию, так как его трудно эксплуатировать в период холодов.
Но чаще всего пропан и бутан используют в качестве автомобильного топлива, а также источника питания для газовых плит и систем отопления.
Токсичность
Будучи малотоксичным соединением пропан, попавший внутрь организма, способен вызвать острые аллергические реакции, оказать негативное воздействие на нервную систему и привести к смерти, если пострадавшему не будет своевременно оказана медицинская помощь.
Признаки отравления пропаном:
- Начальные: покраснение слизистой глаз, слезотечение, сонливость, слабость и головокружение.
- Тяжелые формы интоксикации: учащённый пульс, судороги, посинение, непроизвольные мочеиспускания и потеря сознания.
В случаях, когда пары пропана успели полностью заполнить помещение и вытеснить другие газы, человек задыхается после 2-3 совершённых вздохов и падает без сознания.
Строение алканов
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp3:

При образовании связи С–С происходит перекрывание sp3-гибридных орбиталей атомов углерода:

При образовании связи С–H происходит перекрывание sp3-гибридной орбитали атома углерода и s-орбитали атома водорода:

Четыре sp3-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109о 28′ друг к другу:

Это соответствует тетраэдрическому строению молекулы.
Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода



Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов углерода.
Наример, пространственное строение н-бутана — зигзагообразное

Оптическая изомерия
Если атом углерода в молекуле связан с четырьмя различными заместителями (атомами или атомными группами), например:

то возможно существование двух соединений с одинаковой структурой, но различным пространственным строением.Молекулы таких соединений относятся друг к другу, как зеркальные изображение и предмет. При этом никаким вращением нельзя получить одну молекулу из другой.
Взрывоопасность
Газ — тяжелее воздуха, и его пары способны накапливаться в помещениях, вблизи повреждённых участков газопроводов и прохудившихся ёмкостей. Если вовремя не обнаружить утечки и не перекрыть подачу, вскоре его пары достигнут взрывоопасной концентрации в 2-10%. В таком газовом растворе любая искра, в т. ч электрическая, может стать причиной катастрофы.
Взрывоопасность паров данного СУГ – самый мощный и наиболее коварный из поражающих факторов. По этой причине действующие нормы возлагают на владельцев газовых баллонов обязанность по проведению их регулярной переаттестации, а в состав пропан-бутановой смеси подмешиваются сильнопахнущие одоранты.
Изомеризация алканов
Под действием катализатора и при нагревании неразветвленные алканы, содержащие не менее четырех атомов углерода в основной цепи, могут превращаться в более разветвленные алканы.
Например, н-бутан под действием катализатора хлорида алюминия и при нагревании превращается в изобутан:

Реакции разложения
2.1. Дегидрирование и дегидроциклизация
Дегидрирование – это реакция отщепления атомов водорода.
В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др.
Уравнение дегидрирования алканов в общем виде:
CnH2n+2 → CnH2n-х + (х+1)H2
При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, разрываются связи С–Н у соседних атомов углерода и образуются двойные и тройные связи.
Например, при дегидрировании этана образуются этилен или ацетилен:
При дегидрировании бутана под действием металлических катализаторов образуется смесь продуктов. Преимущественно образуется бутен-2:
![]()
Если бутан нагревать в присутствии оксида хрома (III), преимущественно образуется бутадиен-1,3:
![]()
Алканы с более длинным углеродным скелетом, содержащие 5 и более атомов углерода в главной цепи, при дегидрировании образуют циклические соединения.
При этом протекает дегидроциклизация – процесс отщепления водорода с образованием замкнутого цикла.
Пентан и его гомологи, содержащие пять атомов углерода в главной цепи, при нагревании над платиновым катализатором образуют циклопентан и его гомологи:

Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:


Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:

2.2. Пиролиз (дегидрирование) метана
При медленном и длительном нагревании до 1500оС метан разлагается до простых веществ:
![]()
Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен:![]()
Пиролиз метана – промышленный способ получения ацетилена.
2.3. Крекинг
Крекинг – это реакция разложения алкана с длинной углеродной цепью на алканы с более короткой углеродной цепью и алкены.
Крекинг бывает термический и каталитический.
Термический крекинг протекает при сильном нагревании без доступа воздуха.
При этом получается смесь алканов и алкенов с различной длиной углеродной цепи и различной молекулярной массой.
Например, при крекинге н-пентана образуется смесь, в состав которой входят этилен, пропан, метан, бутилен, пропилен, этан и другие углеводороды.

Каталитический крекинг проводят при более низкой температуре в присутствии катализаторов. Процесс сопровождается реакциями изомеризации и дегидрирования. Катализаторы каталитического крекинга – цеолиты (алюмосиликаты кальция, натрия).
Гомологический ряд пропана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Опасность и поражающие факторы

Сжиженные пропан-бутановые смеси являются одним из наиболее востребованных видов топлива для приготовления пищи и обогрева в загородных домах, туристических походах. Основными причинами широкого распространения и народной любви стали удобство использования, доступность и безопасность в сравнении с другими горючими газами. Тем не менее, пропан требует серьезного отношения, поскольку его утечки тоже периодически становятся причиной гибели людей.
Дегидрирование пропана
Дегидрирование – это реакция отщепления атомов водорода.
В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др.
При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, разрываются связи С–Н у соседних атомов углерода и образуются двойные и тройные связи.
Например, при дегидрировании пропана образуются пропен (пропилен) или пропин:
CH3-CH2-CH3 → CH3-CH=CH2 + H2
CH3-CH2-CH3 → CH3-C≡CH + 2H2
Получение алканов в промышленности
В промышленности алканы получают из нефти, каменного угля, природного и попутного газа. При переработке нефти используют ректификацию, крекинг и другие способы.
Немного физики
Пропановые баллоны содержат углеводород в сжиженной форме. Это обеспечивает высокое давление, при котором газ становится плотным и значительно уменьшается в объеме, достигая показателя 0,493 т/м³. Снижение температуры до -42°С также приводит к сжижению этого соединения, а при показателях ниже -180°С оно замерзает.
Но для эксплуатационных целей пропан не замораживают, а сжимают. В резервуарах он хранится под увеличенным давлением: около 8-12 атм., имеет характерные для плотных тел единицы измерения: в литрах и килограммах. Но обращаться с такой жидкостью привычным образом не удастся. Ее не получится отлить в канистру, как масло или бензин, измерить объем «на глаз». Баллоны для хранения этого вида топлива имеют герметичную конструкцию, их изготавливают из стали.
При использовании необходимое количество пропана или его смеси подается в систему, где сгорает с выделением большого объема тепла. Для регуляции давления газовой струи применяют специальные устройства — редукторы.
При выходе в открытое пространство с нормальным атмосферным давлением и комнатной температурой сжиженное соединение вновь быстро принимает газообразную форму: расширяется более, чем в 22 раза, соединяясь с воздушными массами.
В обычных условиях пропан проявляет свойства газа. Он полностью прозрачен, невидим, не имеет собственного запаха, очень плохо растворяется в воде. На воздухе образует взрывоопасную смесь. Обнаружить такое соединение в пространстве без специального оборудования невозможно, поэтому перед использованием к газу добавляют специальные одоранты — вещества с резким химическим запахом, которые сигнализируют об утечках газа.
Окисление пропана
Пропан– слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.).
3.1. Полное окисление – горение
Пропан горит с образованием углекислого газа и воды. Реакция горения пропана сопровождается выделением большого количества теплоты.
C3H8 + 5O2 → 3CO2 + 4H2O + Q
Уравнение сгорания алканов в общем виде:
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
При горении пропана в недостатке кислорода может образоваться угарный газ СО или сажа С.
Различие между жидким и газообразным пропаном
И газ, и жидкий пропан имеют свое применение, однако они не взаимозаменяемы. Сжиженный нефтяной газ — это топливо в жидком состоянии. Он становится газом при температуре выше -160°C либо при отсутствии давления.
Когда пропан находится в сосуде под давлением, он становится жидкостью. Если жидкий пропан вытесняется из баллона, он превращается в газ при температуре 0 °C и давлении 1 атм. Пропан обычно используется в качестве газа для отопления, приготовления пищи и в качестве автомобильного топлива, поэтому его хранят и доставляют в жидком виде.
Пропан в парообразном состоянии бесцветен и не имеет запаха. Поскольку он подвержен воспламенению и взрыву, его распространение представляет опасность. Пары пропана также тяжелее воздуха. Это свойство не вызывает беспокойства, пока он находится на улице, где подвергается воздействию воздуха. Однако в замкнутом пространстве, пропан опустится в самую нижнюю точку, например, на пол, и останется там, где искра может его воспламенить.
