- Составление формулы оснований
- Валентность — как определить? примеры и определение
- Валентность алюминия в соединениях
- Вопросы:
- Общие сведения о валентности алюминия
- Ответы задачник кузнецова н.е., лёвкин а.н. химия 8 класс 1.6. валентность химических элементов вопросы и задания 1.69-1.74 решебник гдз
- Составление формулы кислот
- Составление формулы оксидов по валентности элементов
- Составление формулы солей
- Таблица валентности химических элементов (1 часть):
- Таблица валентности химических элементов (2 часть):
- Таблица валентности химических элементов (3 часть):
- Таблица валентности химических элементов.
- Таблица характерных значений валентностей некоторых атомов химических соединений.
- Таблица элементов с постоянной валентностью.
Составление формулы оснований
Важный нюанс, который неободимо знать — группы атомов могут рассматриваться, как единое целое.
Составление формул оснований по валентности элементов отличается от составления формулы оксидов лишь тем, что вместо атома кислорода в формуле стоит гидроксогруппа OH. В случае, если гидроксогруппа в формуле повторяется несколько раз, она берется в скобки.
В качестве примера составим составим формулу гидроксида магния.
На первом месте в основаниях стоит атом металла, гидроксогруппа — на втором.
- Mg OH
- MgII OHI
- НОК = 2·1 = 2
- для Mg: 2:2=1; OH: 2:1=2
- Ca(OH)2
Валентность — как определить? примеры и определение
Валентность азота в данном химическом соединении равна трем.
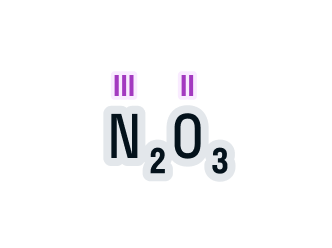
Встречаются бинарные соединения (то есть соединения, состоящие только из двух видов атомов), в которых неизвестны валентности обоих атомов элементов. Как найти валентности химических элементов в этом случае?
Для определения значения валентности необходимо запомнить, что неметаллы в бинарных соединениях, расположенные на втором месте, проявляют свою низшую валентность.
Например, в сульфидах (FeS) сера расположена на втором месте и проявляет низшую валентность, равную двум.
Тогда валентность железа в данном сульфиде можно рассчитать по приведенному выше алгоритму — ее значение равно двум.

В хлоридах (например, AgCl) хлор проявляет низшую валентность, равную единице.
Валентность алюминия в соединениях
Алюминий — тринадцатый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в третьем периоде в IIIA группе. В ядре атома алюминия содержится 13 протонов и 14 нейтронов (массовое число равно 27). В атоме алюминия есть три энергетических уровня, на которых находятся 13 электронов (рис. 1).
Электронная формула атома алюминия в основном состоянии имеет следующий вид:
1s22s22p63s23p1.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Так как на третьем энергетическом слое помимо 3s-подуровня есть еще и 3p-подуровень, две орбитали которого не заняты электронами, то пара электронов 3s-подуровня распаривается и один из них занимает вакантную орбиталь 3p-подуровня. Это означает, что для атома алюминия характерно наличие возбужденного состояния:
Наличие трех неспаренных электронов свидетельствует о том, что алюминий проявляет валентность III в своих соединения (AlIII2O3, AlIII(OH)3, AlIIICl3и др.). Валентность алюминия постоянная.
Вопросы:
1. Составьте формулы следующих соединений:
2. Перепишите формулы и обозначьте римскими цифрами валентность элементов в соединениях с кислородом, зная, что в данных соединениях он двухвалентен:
N2O, Р2O5, N2O3, CaO, СO2, SO3, NO.
3. Сера образует с водородом соединение H2S. Составьте формулы соединений серы с натрием, кальцием и алюминием, в которых сера проявляет такое же значение валентности, как в указанном соединении с водородом.
Общие сведения о валентности алюминия
Алюминий – серебристо-белый легкий металл. Он легко вытягивается в проволоку и прокатывается в тонкие листы. Кристаллизуется в гранецентрированной кубической решетке. Обладает высокой электрической проводимостью и теплопроводностью. Температуры плавления и кипения равны 660oС и -2500oС, соответственно.
При комнатной температуре алюминий не изменяется на воздухе, но лишь потому, что его поверхность покрыта тонкой пленкой оксида, обладающей очень сильным защитным действием.
Ответы задачник кузнецова н.е., лёвкин а.н. химия 8 класс 1.6. валентность химических элементов вопросы и задания 1.69-1.74 решебник гдз
Ответы Задачник Кузнецова Н.Е., Лёвкин А.Н. ХИМИЯ 8 КЛАСС 1.6. Валентность химических элементов Вопросы и задания 1.69-1.74 РЕШЕБНИК ГДЗ
Красным цветом даются ответы, а фиолетовым ― объяснения. |
Задание 1-69
Укажите валентности элементов в соединениях:
а) C
IV
F
4I
, V
2V
O
5II
, Zn
II
Cl
2I
, Cu
II
O
II
, Cu
2I
O
II
, Mg
3II
P
2III
;
б) Ca
II
Br
2I
, S
IV
O
2II
, As
2V
O
5II
, Al
2III
S
3II
, Ba
3II
P
2III
, Fe
II
O
II
;
в) N
II
O
II
, N
2III
O
3II
, S
VI
O
3II
, Na
2I
S
II
, S
VI
F
6I
, B
III
Br
3I
;
г) Na
3I
N
III
, P
2V
O
5II
, Ba
II
Cl
2I
, Mg
3III
P
2II
, Pb
IV
O
2II
, Pb
II
O
II
.
Задание 1-70
Составьте формулы веществ по валентностям элементов:
а) MoO3, Sb2O5, MgO, CuCl2, Cu2O;
б) Li3N2, SO2, P2O5, Cl2O7, CaO;
в) BaI2, MnO2, Ag2O, FeO, PH3;
г) FeCl2, FeCl3, SO2, Mn2O7, AlP, WO3.
Задание 1-71
Составьте формулы соединений элементов с постоянными валентностями
а) алюминия с кислородом; Al2O3
б) лития с кислородом; Li2O
в) кислорода с фтором; OF2
г) цинка с кислородом; ZnO
д) бора с фтором; BF3
е) цинка с фтором. ZnF2
Задание 1-72
Учитывая, что хлор в соединениях PbCl2, AsCl3, SbCl5, SnCl4 одновалентен, определите валентности элементов и составьте формулы их соединений с кислородом.
Валентности в соединениях данных элементов с хлором: PbIICl2, AsIIICl3, SbVCl5, SnIVCl4
Формулы данных элементов с кислородом : PbO, As2O3, Sb2O5, SnO2
Задание 1-73
Определите валентности элементов в соединениях CuF2, SF6, PF5, SiF4 и составьте формулы их соединений с кислородом
Валентности в соединения некоторых элементов с фтором: CuIIF2, SVIF6, PVF5, SiIVF4
Соединения данных элементов с кислородом: CuO, SO3, P2O5, SiO2
Задание 1-74
Приведите примеры соединений элементов с кислородом, в которых эти элементы имеют валентности:
а) II, IV, VI; CaO, SO2, SO3
б) I, III, V. Ag2O, Al2O3, P2O5
Составление формулы кислот
На первом месте в формуле кислот стоит атом(ы) водорода, кислотный остаток — на втором.
В качестве примера составим формулу серной кислоты.
- H SO4
- HI SO4II
- НОК = 2·1 = 2
- для H: 2:1=2; SO4: 2:2=1
- H2SO4
Потренируемся в решении обратной задачи, когда по готовой формуле надо определить валентность элементов.
Составление формулы оксидов по валентности элементов
В качестве примера составим формулу оксида железа (III).
- В оксид железа входят железо и кислород: Fe O;
- Указываем валентность этих элементов: FeIII OII;
- Находим наименьшее общее кратное (НОК): 3·2=6;
- Делим НОК на число единиц валентности каждого элемента:
- для Fe — 6:3=2;
- для O — 6:2=3.
- Записываем полученные индексы справа внизу от элемента: Fe2O3.
Составление формулы солей
В солях «роль» гидроксогруппы OH играют кислотные остатки.
На первом месте в формуле средней соли стоит атом(ы) металла, кислотный остаток — на втором.
В качестве примера составим формулу соли фосфата натрия.
- Na PO4
- NaI PO4III
- НОК = 3·1 = 3
- для Na: 3:3=1; PO4: 3:1=3
- Na3PO4
Таблица валентности химических элементов (1 часть):
| Атомный номер | Химический элемент | Символ | Валентность | Примеры соединений | Примечание |
| 1 | Водород | H | I | HCl, H2O2 | |
| 2 | Гелий | He | отсутствует | ||
| 3 | Литий | Li | I | LiOH, Li2O | |
| 4 | Бериллий | Be | I, II | ||
| 5 | Бор | B | III | B2O3 | |
| 6 | Углерод | C | II, IV | ||
| 7 | Азот | N | I, II, III, IV |
| В азотной кислоте (HNO3) и своем высшем оксиде (N2O5) атом азота образует только четыре ковалентные связи, являясь четырехвалентным |
| 8 | Кислород | O | II | (NO)F, CaO, O2, H2O2,Cl2O, H2O | |
| 9 | Фтор | F | I | HF, (NO)F | |
| 10 | Неон | Ne | отсутствует | ||
| 11 | Натрий | Na | I | Na2S, Na2O | |
| 12 | Магний | Mg | II | Mg(NO3)2 | |
| 13 | Алюминий | Al | III | Al2O3, Al2S3, AlCl3 | |
| 14 | Кремний | Si | II, IV | ||
| 15 | Фосфор | P | III, V |
| |
| 16 | Сера | S | II, IV, VI |
| |
| 17 | Хлор | Cl | I, III, IV, V, VI, VII |
| |
| 18 | Аргон | Ar | отсутствует | ||
| 19 | Калий | K | I | KOH, K2O, K2S | |
| 20 | Кальций | Ca | II | Ca(OH)2 | |
| 21 | Скандий | Sc | III | Sc2O3 | |
| 22 | Титан | Ti | II, III, IV | ||
| 23 | Ванадий | V | II, III, IV, V | ||
| 24 | Хром | Cr | II, III, VI | ||
| 25 | Марганец | Mn | II, III, IV, VI, VII |
| |
| 26 | Железо | Fe | II, III |
| |
| 27 | Кобальт | Co | II, III | ||
| 28 | Никель | Ni | II, III | ||
| 29 | Медь | Cu | I, II | ||
| 30 | Цинк | Zn | II | ZnSO4, ZnO, ZnS |
Таблица валентности химических элементов (2 часть):
| 31 | Галлий | Ga | I, II, III | ||
| 32 | Германий | Ge | II, IV | ||
| 33 | Мышьяк | As | III, V | ||
| 34 | Селен | Se | II, IV, VI | ||
| 35 | Бром | Br | I, III, V, VII | ||
| 36 | Криптон | Kr | отсутствует | ||
| 37 | Рубидий | Rb | I | RbOH | |
| 38 | Стронций | Sr | II | SrO | |
| 39 | Иттрий | Y | III | Y(NO3)3 | |
| 40 | Цирконий | Zr | II, III, IV | ||
| 41 | Ниобий | Nb | I, II, III, IV, V | ||
| 42 | Молибден | Mo | II, III, IV, V, VI |
| |
| 43 | Технеций | Tc | II, III, IV, V, VI, VII |
| |
| 44 | Рутений | Ru | II, III, IV, V, VI, VII, VIII |
| |
| 45 | Родий | Rh | II, III, IV, V, VI |
| |
| 46 | Палладий | Pd | II, IV | ||
| 47 | Серебро | Ag | I, II, III | ||
| 48 | Кадмий | Cd | I, II | ||
| 49 | Индий | In | I, II, III | ||
| 50 | Олово | Sn | II, IV | ||
| 51 | Сурьма | Sb | III, V | ||
| 52 | Теллур | Te | II, IV, VI | ||
| 53 | Йод | I | I, III, V, VII | ||
| 54 | Ксенон | Xe | отсутствует | ||
| 55 | Цезий | Cs | I | Cs2O | |
| 56 | Барий | Ba | II | Ba(OH)2 | |
| 57 | Лантан | La | III | La2(SO4)3 | |
| 58 | Церий | Ce | III, IV | ||
| 59 | Празеодим | Pr | II, III, IV | ||
| 60 | Неодим | Nd | II, III |
Таблица валентности химических элементов (3 часть):
| 61 | Прометий | Pm | III | PmBr3 | |
| 62 | Самарий | Sm | II, III | ||
| 63 | Европий | Eu | II, III | ||
| 64 | Гадолиний | Gd | II, III | ||
| 65 | Тербий | Tb | II, III, IV | ||
| 66 | Диспрозий | Dy | II, III | ||
| 67 | Гольмий | Ho | III | Ho2(SO4)3 | |
| 68 | Эрбий | Er | III | Er2O3 | |
| 69 | Тулий | Tm | II, III | ||
| 70 | Иттербий | Yb | II, III | ||
| 71 | Лютеций | Lu | III | LuBr3 | |
| 72 | Гафний | Hf | I, II, III, IV | ||
| 73 | Тантал | Ta | I, II, III, IV, V |
| |
| 74 | Вольфрам | W | II, III, IV, V, VI |
| |
| 75 | Рений | Re | I, II, III, IV, V, VI, VII |
| |
| 76 | Осмий | Os | I, II, III, IV, V, VI, VII, VIII |
| |
| 77 | Иридий | Ir | I, II, III, IV, V, VI |
| |
| 78 | Платина | Pt | II, III, IV, V, VI | ||
| 79 | Золото | Au | I, II, III, V | ||
| 80 | Ртуть | Hg | I, II | ||
| 81 | Таллий | Tl | I, II, III | ||
| 82 | Свинец | Pb | II, IV | ||
| 83 | Висмут | Bi | III, V | ||
| 84 | Полоний | Po | II, IV, VI | ||
| 85 | Астат | At | нет данных | ||
| 86 | Радон | Rn | отсутствует | ||
| 87 | Франций | Fr | I | FrOH | |
| 88 | Радий | Ra | II | Ra(OH)2 | |
| 89 | Актиний | Ac | III | Ac2O3 | |
| 90 | Торий | Th | II, III, IV | ||
| 91 | Протактиний | Pa | II, III, IV, V | ||
| 92 | Уран | U | III, IV, V, VI | ||
| 93 | Нептуний | Np | III, IV, V, VI, VII | ||
| 94 | Плутоний | Pu | III, IV, V, VI, VII | ||
| 95 | Америций | Am | II, III, IV, V, VI | ||
| 96 | Кюрий | Cm | II, III, IV | ||
| 97 | Берклий | Bk | III, IV | ||
| 98 | Калифорний | Cf | II, III, IV | ||
| 99 | Эйнштейний | Es | II, III | ||
| 100 | Фермий | Fm | II, III |
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента.
Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента.
Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
Коэффициент востребованности 5 686
Таблица валентности химических элементов.
Порядковый номер химического элемента, он же: атомный номер, он же: зарядовое число атомного ядра, он же: атомное число | Русское / Английское наименование | Химический символ | Валентность |
1 | Водород / Hydrogen | H | (-1), 1 |
2 | Гелий / Helium | He | 0 |
3 | Литий / Lithium | Li | 1 |
4 | Бериллий / Beryllium | Be | 2 |
5 | Бор / Boron | B | -3, 3 |
6 | Углерод / Carbon | C | ( 2), 4 |
7 | Азот / Nitrogen | N | -3, -2, -1, ( 1), 2, 3, 4, 5 |
8 | Кислород / Oxygen | O | -2 |
9 | Фтор / Fluorine | F | -1, ( 1) |
10 | Неон / Neon | Ne | 0 |
11 | Натрий / Sodium | Na | 1 |
12 | Магний / Magnesium | Mg | 2 |
13 | Алюминий / Aluminum | Al | 3 |
14 | Кремний / Silicon | Si | -4, ( 2), 4 |
15 | Фосфор / Phosphorus | P | -3, 1, 3, 5 |
16 | Сера / Sulfur | S | -2, 2, 4, 6 |
17 | Хлор / Chlorine | Cl | -1, 1, ( 2), 3, ( 4), 5, 7 |
18 | Аргон / Argon | Ar | 0 |
19 | Калий / Potassium | K | 1 |
20 | Кальций / Calcium | Ca | 2 |
21 | Скандий / Scandium | Sc | 3 |
22 | Титан / Titanium | Ti | 2, 3, 4 |
23 | Ванадий / Vanadium | V | 2, 3, 4, 5 |
24 | Хром / Chromium | Cr | 2, 3, 6 |
25 | Марганец / Manganese | Mn | 2, ( 3), 4, ( 6), 7 |
26 | Железо / Iron | Fe | 2, 3, ( 4), ( 6) |
27 | Кобальт / Cobalt | Co | 2, 3, ( 4) |
28 | Никель / Nickel | Ni | ( 1), 2, ( 3), ( 4) |
29 | Медь / Copper | Сu | 1, 2, ( 3) |
30 | Цинк / Zinc | Zn | 2 |
31 | Галлий / Gallium | Ga | ( 2). 3 |
32 | Германий / Germanium | Ge | -4, 2, 4 |
33 | Мышьяк / Arsenic | As | -3, ( 2), 3, 5 |
34 | Селен / Selenium | Se | -2, ( 2), 4, 6 |
35 | Бром / Bromine | Br | -1, 1, ( 3), ( 4), 5 |
36 | Криптон / Krypton | Kr | 0 |
37 | Рубидий / Rubidium | Rb | 1 |
38 | Стронций / Strontium | Sr | 2 |
39 | Иттрий / Yttrium | Y | 3 |
40 | Цирконий / Zirconium | Zr | ( 2), ( 3), 4 |
41 | Ниобий / Niobium | Nb | ( 2), 3, ( 4), 5 |
42 | Молибден / Molybdenum | Mo | ( 2), 3, ( 4), ( 5), 6 |
43 | Технеций / Technetium | Tc | 6 |
44 | Рутений / Ruthenium | Ru | ( 2), 3, 4, ( 6), ( 7), 8 |
45 | Родий / Rhodium | Rh | ( 2), ( 3), 4, ( 6) |
46 | Палладий / Palladium | Pd | 2, 4, ( 6) |
47 | Серебро / Silver | Ag | 1, ( 2), ( 3) |
48 | Кадмий / Cadmium | Cd | ( 1), 2 |
49 | Индий / Indium | In | ( 1), ( 2), 3 |
50 | Олово / Tin | Sn | 2, 4 |
51 | Сурьма / Antimony | Sb | -3, 3, ( 4), 5 |
52 | Теллур / Tellurium | Te | -2, ( 2), 4, 6 |
53 | Иод / Iodine | I | -1, 1, ( 3), ( 4), 5, 7 |
54 | Ксенон / Xenon | Xe | 0 |
55 | Цезий / Cesium | Cs | 1 |
56 | Барий / Barium | Ba | 2 |
57 | Лантан / Lanthanum | La | 3 |
58 | Церий / Cerium | Ce | 3, 4 |
59 | Празеодим / Praseodymium | Pr | 3 |
60 | Неодим / Neodymium | Nd | 3, 4 |
61 | Прометий / Promethium | Pm | 3 |
62 | Самарий / Samarium | Sm | ( 2), 3 |
63 | Европий / Europium | Eu | ( 2), 3 |
64 | Гадолиний / Gadolinium | Gd | 3 |
65 | Тербий / Terbium | Tb | 3, 4 |
66 | Диспрозий / Dysprosium | Dy | 3 |
67 | Гольмий / Holmium | Ho | 3 |
68 | Эрбий / Erbium | Er | 3 |
69 | Тулий / Thulium | Tm | ( 2), 3 |
70 | Иттербий / Ytterbium | Yb | ( 2), 3 |
71 | Лютеций / Lutetium | Lu | 3 |
72 | Гафний / Hafnium | Hf | 4 |
73 | Тантал / Tantalum | Ta | ( 3), ( 4), 5 |
74 | Вольфрам / Tungsten | W | ( 2), ( 3), ( 4), ( 5), 6 |
75 | Рений / Rhenium | Re | (-1), ( 1), 2, ( 3), 4, ( 5), 6, 7 |
76 | Осмий / Osmium | Os | ( 2), 3, 4, 6, 8 |
77 | Иридий / Iridium | Ir | ( 1), ( 2), 3, 4, 6 |
78 | Платина / Platinum | Pt | ( 1), 2, ( 3), 4, 6 |
79 | Золото / Gold | Au | 1, ( 2), 3 |
80 | Ртуть / Mercury | Hg | 1, 2 |
81 | Талий / Thallium | Tl | 1, ( 2), 3 |
82 | Свинец / Lead | Pb | 2, 4 |
83 | Висмут / Bismuth | Bi | (-3), ( 2), 3, ( 4), ( 5) |
84 | Полоний / Polonium | Po | (-2), 2, 4, ( 6) |
85 | Астат / Astatine | At | нет данных |
86 | Радон / Radon | Rn | 0 |
87 | Франций / Francium | Fr | нет данных |
88 | Радий / Radium | Ra | 2 |
89 | Актиний / Actinium | Ac | 3 |
90 | Торий / Thorium | Th | 4 |
91 | Проактиний / Protactinium | Pa | 5 |
92 | Уран / Uranium | U | ( 2), 3, 4, ( 5), 6 |
Чего не указано в таблице валентности, это то, что валентность элемента может быть постоянной и переменной.
Виды валентности | ||
Постоянная (у металлов главных подгрупп) | Переменная (у неметаллов и металлов побочных подгрупп) | |
Высшая (равна номеру группы) | Низшая (равна разности между числом 8 и номером группы) | |
Знание валентности элементов необходимы для правильного составления химических формул соединений.
Таблица характерных значений валентностей некоторых атомов химических соединений.
Элементы | Валентность | Примеры соединений |
H, F, Li, Na, K | I | H2, HF, Li2O, NaCl, KBr |
O, Mg, Ca, Sr, Ba, Zn | II | H2O, MgCl2, CaH2, SrBr2, BaO, ZnCl2 |
B, Al | III | BCl3, AlBr3 |
C, Si | IV | CO2, CH4, SiO2, SiCl4 |
Cu | I, II | Cu2O, CuO |
Fe | II, III | FeCl2, FeCl3 |
Cr | II, III, VI | CrCl2, CrCl3, CrO3 |
S | II, IV, VI | H2S, SO2, SO3 |
N | III, IV | NH3, NH4Cl, HNO3 |
P | III, V | PH3, P2O5, H3PO4 |
Sn, Pb | II, IV | SnCl2, SnCl4, PbO, PbO2 |
Cl, Br, I | I, III, V, VII | HCl, ClF3, BrF5, IF7 |
Таблица элементов с постоянной валентностью.
Валентности | Элементы |
I | H, Na, Li, K, Rb, Cs |
II | O, Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd |
III | B, Al, Ga, In |

