– бесцветный сжатый сжиженный газ тяжелее воздуха, с резким запахом, не горюче.

- Что такое хлороводород, формула
- Свойства
- Где купить и сколько стоит
- Аварийная карточка (АХОВ)
- Применение
- Применение хлороводорода в металлургии и химпроме
- Применение хлороводорода в сфере продуктов питания и медицине
- Физические свойства, внешний вид
- Упаковка, транспортировка
- Безопасность
- Меры предосторожности, токсичность
- Ссылки
- Получение, уравнение хлорида водорода
- Заключение
Что такое хлороводород, формула
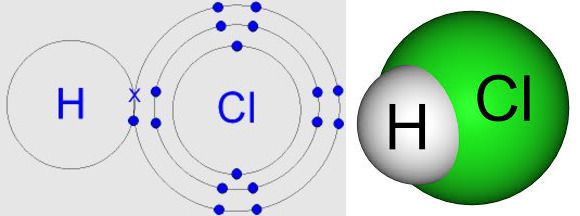
Хлороводород – это сложное бинарное соединение, относящееся к кислотам. Состоит из водорода и присоединённого к нему атома хлора, элементы связаны между собой полярной связью. Химическая формула – HСl.
В природе хлороводород встречается вблизи вулканических источников. При выделении с выбросами хлора формируется вещество. В естественном виде раствор хлорида водорода входит в состав желудочного сока человека. В комбинации с пепсином и другими ферментами он способствует расщеплению и перевариванию пищи. При избыточной секреции париетальными клетками желудка значение pH среды существенно понижается, возникает риск возникновения заболеваний желудочно-кишечного тракта: язвы, изжоги, гастроэзофагеального рефлюкса.
Хлороводород – это газ, водный раствор которого широко применяется во многих областях деятельности. Как отдельное вещество хлороводород часто используют в металлургии, при производстве стройматериалов, в органическом и неорганическом синтезе. Имеет большое значение для очистки металлических изделий, изготовления пищевых добавок, обогащения руды. Раствор хлорида водорода зарегистрирован как пищевая добавка, которой присвоен код Е507 – регулятор кислотности и антислёживающий агент.

- Что такое хлороводород, формула
- Физические свойства, внешний вид
- Химические свойства, реакции
- Получение, уравнение хлорида водорода
- Применение
- Меры предосторожности, токсичность
- Упаковка, транспортировка
- Где купить и сколько стоит
- Заключение
HCl, при обычных условиях бесцветный газ с резким запахом; на воздухе при поглощении влаги образует туман, представляющий собой мельчайшие капельки соляной кислоты (См. Соляная кислота). Масса 1 л Х. в. при 0°С и 0,1 Мн/м2(1 кгс/см2) 1,6391 г; плотность по воздуху 1,268; плотность жидкого Х. в при — 60°C 1,12 г/см3; tпл —114,2°С; tkип —85,1°С. Критические константы: температура 51,4°C; давление 8,45 Мн/м2 (84,5 кгс/см2); плотность 0,42 г/см3; удельный объём 2380 см3/г. Х. в. растворяется в воде с выделением тепла; при этом образуется соляная кислота. Под давлением 0,1 Мн/м2(1 кгс /см2) 1 л воды растворяет 500 л HCl при 2°С, 442 л при 20°C, 339 л при 60°C.
Получают Х. в. прямым синтезом из элементов или действием серной кислоты на хлорид натрия. Большие количества Х. в. получаются как побочный продукт при хлорировании (См. Хлорирование) органических соединений: RH + Cl2 = RCl + HCl (где R — радикал), а также при гидролизе хлорида магния: MgCl2 + H2O = MgO + 2HCl. Мировое производство Х. в. составляет около 10 млн. т (1975).
Х. в. используют для получения соляной кислоты, синтеза органических соединений, например Винилхлорида.
Лит.: Якименко Л. М., Производство хлора, каустической соды и неорганических хлорпродуктов, М., 1974; Якименко Л. М., Пасманик М. И., Справочник по производству хлора, каустической соды и основных хлорпродуктов, 2 изд., М., 1976.
Л. М. Якименко.
Большая советская энциклопедия. — М.: Советская энциклопедия.
.
Физические свойства растворов соляной кислоты разных концентраций приведены в таблице:
Водород хлористый (хлороводород) – это бесцветный сжатый сжиженный газ с резким запахом. Не горюче. Многие реакции могут привести к пожару или взрыву. Вещество может всасываться в организм при вдыхании.
Свойства
Водный раствор хлористого водорода называется соляной кислотой. При растворении в воде протекают следующие процессы:
HClг + H2Oж H3O+ж + Cl−ж
Процесс растворения сильно экзотермичен. С водой HCl образует азеотропную смесь, содержащую 20,24 % HCl.
Соляная кислота является сильной одноосновной кислотой, она энергично взаимодействует со всеми металлами, стоящими в ряду напряжений левее водорода, с основными и амфотерными оксидами, основаниями и солями, образуя соли — хлориды:
Хлориды чрезвычайно распространены и имеют широчайшее применение (галит, сильвин). Большинство из них хорошо растворяется в воде и полностью диссоциирует на ионы. Слаборастворимыми являются хлорид свинца (PbCl2), хлорид серебра (AgCl), хлорид ртути(I) (Hg2Cl2, каломель) и хлорид меди(I) (CuCl).
При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства:
При нагревании хлороводород окисляется кислородом (катализатор — хлорид меди(II) CuCl2):
Однако, концентрированная соляная кислота реагирует с медью, при этом образуется комплекс одновалентной меди:
Смесь 3 объемных частей концентрированной соляной и 1 объемной доли концентрированной азотной кислот называется «царской водкой». Царская водка способна растворять даже золото и платину. Высокая окислительная активность царской водки обусловлена присутствием в ней хлористого нитрозила и хлора, находящихся в равновесии с исходными веществами:
4 H3O+ + 3 Cl− + NO3− NOCl + Cl2 + 6 H2O
Благодаря высокой концентрации хлорид-ионов в растворе металл связывается в хлоридный комплекс, что способствует его растворению:
Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение):
Присоединяется к серному ангидриду, образуя хлорсульфоновую кислоту HSO3Cl:
Где купить и сколько стоит
Раствор хлороводорода можно купить у заводов-производителей по цене от 25 рублей за 1 кг. Хлорид водорода продаётся в магазинах реактивов по стоимости от 120 руб/л.
Аварийная карточка (АХОВ)
ХЛОРИСТЫЙ ВОДОРОД, КЛАСС ТОКСИЧЕСКОЙ ОПАСНОСТИ – 3ICSC: 0163
CAS № 7647-01-0 HCl Классификация ООН ООН № 1050 Молекулярная масса: 36.5Класс опасности ООН: 2.3ЕС № 017-002-00-2Вторичная опасность по ООН: 8
ВИДЫ ОПАСНОСТИ / ВОЗДЕЙСТВИЯОСТРАЯ ОПАСНОСТЬ / СИМПТОМЫПРЕДУПРЕЖДЕНИЕ
ПОЖАРНАЯ ОПАСНОСТЬ
Не горюче.
–
ВОЗДЕЙСТВИЕ
–
СТРОГИЕ МЕРЫ ГИГИЕНЫ! НЕ ДОПУСКАТЬ ВОЗДЕЙСТВИЯ НА (БЕРЕМЕННЫХ) ЖЕНЩИН!ТРАНСПОРТИРОВКА/ ХРАНЕНИЕ!
Вдыхание
Едкое. Ощущение жжения. Кашель. Затрудненное дыхание. Одышка. Боли в горле. Симптомы могут быть отсроченными (см. Примечания).
Вентиляция, местная вытяжка или защита органов дыхания.
Свежий воздух, покой. Полусидячее положение. Искусственное дыхание по показаниям. Обратиться за медицинской помощью.
Кожа
ПРИ КОНТАКТЕ С ЖИДКОСТЬЮ: ОБМОРОЖЕНИЕ. Едкое. Серьезные ожоги кожи. Боль.
Холодозащитные перчатки. Защитная одежда.
Сначала промыть большим количеством воды, затем удалить загрязненную одежду и снова промыть. Обратиться за медицинской помощью.
Глаза
Жжение. Боль. Неясность зрения. Сильные глубокие ожоги.
Защитные очки-маска, или защита глаз в сочетании с защитой органов дыхания.
Вначале промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это не трудно), затем доставить к врачу.
В случае пожара: охлаждать баллоны, обливая их водой. В случае возгорания в окрестностях: разрешены все средства пожаротушения.Провести эвакуацию из опасной зоны! Проконсультироваться со специалистом! Вентиляция. Удалить газ, используя мелкие брызги воды, (дополнительная личная защита: полный комплект защитной одежды, включая автономный дыхательный аппарат).При ликвидации аварий, связанных с проливом соляной кислоты необходимо изолировать опасную зону, удалить из нее людей, держаться с наветренной стороны, избегать низких мест. Непосредственно на месте аварии и в зонах заражения с высокими концентрациями на расстоянии до 50 м. от места разлива работы проводят в изолирующих противогазах ИП-4М, ИП-5 (на химически связанном кислороде) или дыхательных аппаратах АСВ-2, ДАСВ (на сжатом воздухе), КИП-8, КИП-9 (на сжатом кислороде) и средствах защиты кожи (Л-1, ОЗК, КИХ-4, КИХ-5). На расстоянии более 50 м от очага, где концентрация резко понижается, средства защиты кожи можно не использовать, а для защиты органов дыхания используют промышленные противогазы с коробками марок В, БКФ, а также гражданские противогазы ГП-5, ГП-7, ПДФ-2Д, ПДФ-2Ш в комплекте с дополнительным патроном ДПГ-3 или респираторы РПГ-67, РУ-60М с коробкой марки В.Нейтрализуют соляную кислоту и пары хлористого водорода следующими щелочными растворами:– 5%-ным водным раствором каустической соды (например, 50 кг каустической соды на 950 литров воды);– 5%-ным водным раствором содового порошка (например, 50 кг содового по-рошка на 950 литров воды);– 5%-ным водным раствором гашеной извести (например, 50 кг гашеной извести на 950 литров воды);– 5%-ным водным раствором едкого натра (например, 50 кг едкого натра на 950 литров воды);При разливе соляной кислоты и отсутствии обваловки или поддона место разлива ограждают земляным валом, осаждают пары хлористого водорода постановкой водяной завесы, (расход воды не нормируется), обезвреживают разлившуюся кислоту до безопасных концентраций водой (8 тонн воды на 1 тонну кислоты) с соблюдением всех мер предосторожности или 5%-ным водным раствором щелочи (3,5 тонны раствора на 1 тонну кислоты) и нейтрализуют 5%-ным водным раствором щелочи (7,4 тонны раствора на 1 тонну кислоты).Для распыления воды или растворов применяют поливомоечные и пожарные машины, авторазливочные станции (АЦ, ПМ-130, АРС-14, АРС-15), а также имеющиеся на химически опасных объектах гидранты и спецсистемы.Для утилизации загрязненного грунта на месте разлива соляной кислоты срезают поверхностный слой грунта на глубину загрязнения, собирают и вывозят на утилизацию с помощью землеройно-транспортных машин (бульдозеров, скреперов, автогрейдеров, самосвалов). Места срезов засыпают свежим слоем грунта, промывают водой в контрольных целях.Действия руководителя: изолировать опасную зону в радиусе не менее 50 метров, удалить из нее людей, держаться с наветренной стороны, избегать низких мест. В зону аварии входить только в полной защитной одежде.
Оказание первой медицинской помощи:В зараженной зоне: обильное промывание водой глаз и лица, надевание проти-вогаза, срочный вывод (вывоз) из очага.После эвакуации из зараженной зоны: согревание, покой, смывание кислоты с открытых участков кожи и одежды водой, обильное промывание глаз водой, при затруднении дыхания тепло на область шеи, подкожно – 1 мл. 0,1% раствора атропина сульфата. Немедленная эвакуация в лечебное учреждение.
ФИЗИЧЕСКОЕ СОСТОЯНИЕ, ВНЕШНИЙ ВИД: БЕСЦВЕТНЫЙ СЖАТЫЙ СЖИЖЕННЫЙ ГАЗ, С РЕЗКИМ ЗАПАХОМ.ФИЗИЧЕСКАЯ ОПАСНОСТЬ: Газ тяжелее воздуха.ХИМИЧЕСКАЯ ОПАСНОСТЬ: Водный раствор является сильной кислотой, он бурно реагирует с основаниями и коррозионно-агрессивен. Реагирует бурно с окислителями с образованием токсичного газа (хлора – см. ICSC # 0126). Агрессивно в отношении многих металлов в присутствии воды образуя горючий/взрывоопасный газ (водород- см. ICSC # 0001).НОРМАТИВЫ ДЛЯ РАБОЧЕЙ ЗОНЫ: TLV (предельная пороговая концентрация, США): 5 ppm; как (предельный пороговый уровень однократного воздействия, США (ACGIH 1999).ПУТИ ПОСТУПЛЕНИЯ: Вещество может всасываться в организм при вдыхании.РИСК ПРИ ВДЫХАНИИ:
При утечке содержимого очень быстро достигается опасная концентрация этого газа в воздухе.ВЛИЯНИЕ КРАТКОВРЕМЕННОГО ВОЗДЕЙСТВИЯ: Быстрое испарение жидкости может вызвать обморожение. Вещество оказывает разъедающее действие на глаза кожу и дыхательные пути. Вдыхание газа высокой концентрации может вызвать пневмонию и отек легких, приводя к синдрому дисфункции дыхательных путей (RADS) (см. Примечания). Эффекты могут быть отсроченными. Показано медицинское наблюдение.ВЛИЯНИЕ ДОЛГОВРЕМЕННОГО ИЛИ МНОГОКРАТНОГО ВОЗДЕЙСТВИЯ: Вещество может оказывать действие на легкие, приводя к хроническому бронхиту. Вещество может действовать на зубы, приводя к их эрозии.НАЛИЧИЕ СОЛЯНОЙ КИСЛОТЫ ОПРЕДЕЛЯЮТ:В воздухе промышленной зоны газоанализатором ОКА-Т-НCl, газосигнализато-ром ИГС-98-НCl, универсальным газоанализатором УГ-2 с диапазоном измере-ния 0-100 мг/м3, газоопределителем промышленных химических выбросов ГПХВ-2 в диапазоне 5-500 мг/м3.На открытом пространстве – приборами СИП «КОРСАР-Х».В закрытом помещении – СИП «ВЕГА-М»
ФИЗИЧЕСКИЕ СВОЙСТВА
ПРЕДЕЛЬНО ДОПУСТИМАЯ КОНЦЕНТРАЦИЯ (ПДК)
Температура кипения: -85°C
Температура плавления: -114°C
Плотность: 1.00045 г/л (газ)
Растворимость в воде, г/100 мл при 30°C: 67
Относительная плотность пара (воздух = 1): 1.3Koэффициент распределения октанол/вода как lg Pow: 0.25
Предельно допустимая концентрация (ПДК) в воздухе населенных пунктов составляет 0,2 мг/м3, в воздухе рабочей зоны производственных помещений 5 мг/м3.При концентрации 15 мг/м3 поражаются слизистые оболочки верхних дыхательных путей и глаз, появляется першение в горле, охриплость голоса, кашель, насморк, одышка, затрудняется дыхание. При концентрациях от 50 мг/м3 и выше возникают клокочущее дыхание, резкие боли за грудиной и в области желудка, рвота, спазм и отек гортани, потеря сознания. Концентрация 50-75 мг/м3 переносится с трудом. Концентрация 75-100 мг/м3 – непереносима. Концентрация 6400 мг/м3 в течение 30 минут – смертельна. Максимально допустимая концентрация при применении промышленных и гражданских противогазов составляет 16000 мг/м3.
Величина пределов профессионального воздействия не должна превышаться в течение какого-либо периода рабочего дня. Симптомы отека легких часто проявляются через несколько часов и обостряются при физической нагрузке. Поэтому требуется отдых и медицинское наблюдение. Должен рассматриваться вопрос о немедленном введении соответствующего средства врачом или лицом им уполномоченным. НЕ обливать водой прохудившуюся емкость (во избежание коррозии емкости). Перевернуть подтекающую емкость местом утечки кверху во избежании утечки газа в жидкой форме. Другие номера ООН: 2186 (охлаждающая жидкость) класс опасности: 2.3; побочная опасность: 8; 1789 (соляная кислота) класс опасности 8, группа упаковки II или III. Водный раствор может содержать до 38% Хлористого водорода.
Применение
Хлорид водорода используется во многих сферах. Большее количество произведенного хлороводорода поступает на нужды тяжёлой промышленности и химии. Меньшая доля потребляется промышленной отраслью и изготовлением строительных материалов. В связи с исключительной реакционной активностью применение хлороводорода актуально для выпуска глутамата натрия, соды, соли.
Применение хлороводорода в металлургии и химпроме
Вещество хлороводород ценится в области получения и обработки металлов. Это важный компонент такого технологического приёма, как травление. В ходе него производится очистка поверхностного слоя материала за счёт растворяющего действия хлорида водорода. Это совершается для достижения нескольких целей:
- удаление окалины;
- выявление структуры материалов;
- нанесение рельефного рисунка в художественной металлографии;
- создание проводящих дорожек для печатных плат и интегральных схем;
- вытравливание сверхмалых отверстий при конструировании мембран;
- полировка.
Хлорид водорода необходим для декапирования перед гальванической обработкой, когда удаляется грязь и различные окислы. При пайке вещество применяют для дезинфекции. Ингибированный хлороводород используют в смеси с ПАВ для промывки керамических изделий.
Это важный реактив для выпуска хлоридов, широко использующихся для самых разнообразных целей. Кроме того, он может выступать закислителем среды для нормализации прохождения реакций получения карбонатов и гашеной извести.
Применение хлороводорода в сфере продуктов питания и медицине
Пищевая добавка Е507 применяется прежде всего для изготовления инвертированного сиропа – смеси фруктозы и глюкозы. Он выступает как загуститель, заменяющий патоку. За счёт инвертного сахара начинки конфет и пирожных не засахариваются, сохраняют исходную структуру. Пищевую добавку Е507 как антиокислитель можно встретить в таких продуктах, как:
- зельтерская содовая;
- желатин;
- мелассное сусло.
В фармацевтике хлороводород в комбинации с пепсином используется как действующее вещество лекарственных препаратов для коррекции кислотности ЖКТ.
Физические свойства, внешний вид
При нормальных условиях хлороводород – это газ без цвета, с ярко выраженным резким запахом. При повышенной влажности дымит на открытом воздухе, его плотность составляет 1.477 г/л, молярная масса – 36,4606 г/моль. Хлороводород высоко гигроскопичен, быстро впитывает воду и легко растворяется в ней с образованием соляной кислоты. При низких отрицательных температурах из газообразного состояния переходит в жидкое и закипает – при -85,1°С, при дальнейшем снижении температурного режима преобразуется в твёрдое соединение (плавится при -144,22°С). Разлагается при 1500°С.
Твёрдые кристаллы хлорида водорода существуют в двух формах: кубические и ромбические. Они беловатые либо бесцветные, довольно крупные. Кристаллическая смесь характеризуется отсутствием аромата. Хлороводород, вода дают кристаллогидраты, которые описываются формулой HCl ∙ nH2O, где n = 2, 3, 6.
Водный раствор широко используется для получения хлоридов, для травления металлов, очистки поверхности сосудов, скважин от карбонатов, обработки руд, при производстве каучуков, глутамината натрия, соды, хлора и других продуктов. Также применяется в органическом синтезе.
Упаковка, транспортировка
Хлороводород содержится в цистернах и баллонах, снабжённых предохранителем со строго установленным давлением и заполненностью 65% объёма. Его следует хранить в сухих помещениях вдали от прямых солнечных лучей и температурным режимом, не достигающем 60 °С.
Безопасность
Вдыхание хлороводорода может привести к кашлю, удушью, воспалению носа, горла и верхних дыхательных путей, а в тяжёлых случаях, отёк легких, нарушение работы кровеносной системы, и даже смерть. Контактируя с кожей может вызывать покраснение, боль и серьёзные ожоги. Хлористый водород может вызвать серьёзные ожоги глаз и их необратимое повреждение.
Меры предосторожности, токсичность
Хлороводород крайне токсичен (3 класс опасности). Это сильнодействующий яд, оказывающий губительное воздействие на слизистые оболочки дыхательных путей и глаз. В период второй мировой войны он применялся как отравляющее боевое вещество. Вдыхание хлороводорода приводит к сильнейшему раздражению, кашлю, чиханию, отёку лёгких. При соприкосновении с кожей провоцирует покраснение, глубокие ожоги.
При работе с хлоридом водорода следует соблюдать меры безопасности: работать в перчатках и респираторе и под работающей тягой. При попадании на кожный покров следует обильно промыть водой и обратиться к специалисту.
Ссылки
Хлороводород отличается высокой степенью реактивной способности. Отмечено взаимодействие хлороводорода со многими соединениями различных классов. При смешивании с водой хлороводорода образуется кислота хлороводорода:
Вещество хлороводород реагирует с аммиаком, формируя в ходе реакции хлорид аммония:
Раствор хлороводорода реагирует с гидроксидами, при этом протекает реакция нейтрализации:
С активными щелочными металлами хлороводород реагирует с формированием схожих продуктов:
Хлороводород реагирует также с основными оксидами:
С амфотерными соединениями хлороводород реагирует с выделением хлористого железа:
Несмотря на сильные окислительные свойства, хлорид водорода может подвергаться окислению серьёзными реагентами, например, перманганатом:
По той же схеме идёт реакция с дихроматом:
Для хлорида водорода характерна реакция ионного обмена, при этом хлорид водорода реагирует с карбонатом натрия в растворе:
Хлороводород окисляет сильные оксиды до хлоридов:
В процессе реакции с сульфидом натрия он растворяется:
При подогревании хлороводород реагирует с пероксидами, при этом выделяется газообразный молекулярный кислород:
При комнатной температуре реакция идёт по-другому – при взаимодействии хлороводорода с пероксидом натрия формируется перекись водорода:
Взаимодействие хлороводорода с гидридами:
Получение, уравнение хлорида водорода
Раствор хлорида водорода получают путём сжижения газа либо путём взаимодействия непосредственных элементов на свету:
Наиболее распространённый способ получения хлорида водорода в лабораторных условиях заключается в действии на поваренную соль серной при 150 °С:
При получении с интенсивным нагреванием (до 550 °С) выход продукта более высок:
Хлорид водорода получают с помощью термолиза:
Другой вариант получения – разложение неустойчивых хлоритов:
Получить хлороводород возможно путём обработки галогенидов:
В промышленности предпочтение чаще всего отдаётся прямому синтезу из простых веществ за счёт экономного расхода реагентов и повышенной безопасности по сравнению с методикой добычи его по Леблану (через серную кислоту).
Добыча ведётся в специализированных установках, куда непрерывно подают хлор и водород, проходящие над горелкой. В этом пламени энергии сгорания вполне достаточно для формирования полноценного вещества хлороводорода. При этом водорода берётся избыточное количество за счёт чего экономится дорогой и ценный компонент.
В лабораторных условиях хлороводород получают, воздействуя концентрированной серной кислотой на хлорид натрия (поваренную соль) при слабом нагревании:
NaCl(тверд.) + H2SO4(конц.) = NaHSO4 + HCl↑
HCl↑ также можно получить гидролизом ковалентных галогенидов, таких, как хлористый фосфорил, тионилхлорид (SOCl2), и гидролизом хлорангидридов карбоновых кислот:
В промышленности хлороводород ранее получали в основном сульфатным методом (методом Леблана), основанном на взаимодействии хлорида натрия с концентрированной серной кислотой. В настоящее время для получения хлороводорода обычно используют прямой синтез из простых веществ:
H2 + Cl2 2HCl↑
В производственных условиях синтез осуществляется в специальных установках, в которых водород непрерывно сгорает ровным пламенем в токе хлора, смешиваясь с ним непосредственно в факеле горелке. Тем самым достигается спокойное (без взрыва) протекание реакции. Водород подается в избытке (5 — 10 %), что позволяет полностью использовать более ценный хлор и получить незагрязненную хлором соляную кислоту.
Соляную кислоту получают растворением газообразного хлороводорода в воде.
Заключение
Хлороводород – это опасный едкий реагент, окисляющие и очищающие свойства которого нашли применение в гидрометаллургии. Он также используется как основа для лекарств при пониженном pH, пищевая добавка Е507, способствующая поддержанию водородного показателя на определённом уровне.
Сайт предоставляет информацию в справочных целях, только для ознакомления. Поставить диагноз и назначить адекватное лечение может только врач! Медикаменты и народные средства должны назначаться специалистом, так как имеют противопоказания и побочные действия! Посещение и консультации квалифицированного специалиста строго обязательны!
