- Основы молекулярной физики и термодинамики: методические указания к практическим занятиям по курсу общей физики, страница 3
- Единицы измерения
- Коэффициент диффузии броуновской частицы
- Определение и формула коэффициента диффузии
- Решение определим среднюю арифметическую скорость молекул гелия при нормальных условиях р = 10 5 па, т = 273 к. (1)
- Формулы для коэффициента диффузии
Основы молекулярной физики и термодинамики: методические указания к практическим занятиям по курсу общей физики, страница 3
Задача 5. Вычислить коэффициент внутреннего трения и коэффициент
диффузии кислорода, находящегося при давлении 0,2 МПа и температуре 280 К.
Дано: p = 2·105 Па d= 2,9·10-10 м М = 32·10-3 кг/моль Т = 280 К | Решение: На |
η — ? D — ? |
 (1);
(1); 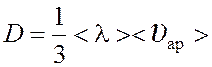 (2), где ρ – плотность газа; < λ >
(2), где ρ – плотность газа; < λ >
– средняя длина свободного пробега молекул; <υар> – средняя арифметическая скорость молекул.
Из (1) и (2) следует ![]() (3)
(3)
Среднюю арифметическую скорость и среднюю длину
свободного пробега молекул находим по формулам:
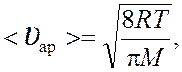 (4)
(4)
 , (5)
, (5)
где R = 8,31 Дж/(моль·К) – молярная газовая
постоянная; Т – термодинамическая температура; d = 2,9·10 –10 м – эффективный
диаметр молекулы кислорода; n0 – число
молекул в 1 м3(концентрация).
Из уравнения Менделеева — Клайперона определяем n0
(см. задачу
3):  (6)
(6)
где р – давление; k = 1,38·10 –23
Дж/К – постоянная Больцмана.
Подставляя (6) в уравнение (5), получаем: . (7)
. (7)
Окончательный вид расчетной формулы для коэффициента
диффузии найдем, подставляя выражения (4) и (7) в уравнение (2):
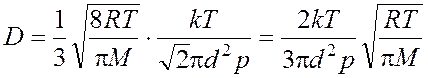 . (8)
. (8)
Плотность кислорода определяется по формуле: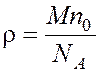 . С учетом (6) имеем:
. С учетом (6) имеем:  . (9)
. (9)
Подставляя (9) и (8) в (3), получаем расчетную формулу
для коэффициента внутреннего трения: 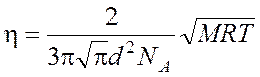 .
.
Вычисляем: 
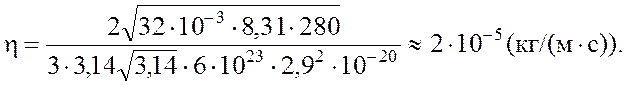
Ответ: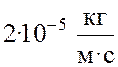 .
.
Задача 6. Наружная поверхность кирпичной стены площадью 25 м2 и толщиной 37 см имеет температуру 259 К, а внутренняя
поверхность–293 К. Помещение отапливается электроплитой. Определить ее
мощность, если температура в помещении поддерживается постоянной.
Теплопроводность кирпича 0,4 Вт/(м·К).
За время t – электроплита должна выделить такое же количество
теплоты: ![]() (2)
(2)
Приравнивая правые части уравнений (1) и (2), получаем:
 ,
,
откуда
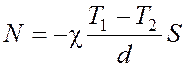 ,
, 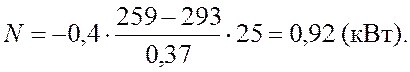
Ответ: 0,92
кВт.
2. Основы термодинамики
Задача 7. Чему равны средние кинетические энергии
поступательного и вращательного движения молекул, содержащихся в 2 кг водорода при температуре 400 К.
Дано: т = 2 кг Т = 400 К М = 2·10 –3 кг/моль | Решение: Считаем водород идеальным газом. Молекула водорода – |
<Eпост> — ? <Eвр> — ? |
число степеней свободы молекулы водорода равно
5. В среднем на одну степень свободы приходится энергия: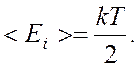 Поступательному
Поступательному
движению приписывается три (i = 3),
а вращательному две (i= 2)
степени свободы. Тогда энергия одной молекулы:
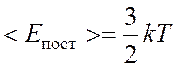 ,
, 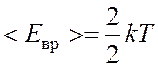 .
.
Число молекул, содержащихся в массе газа m:
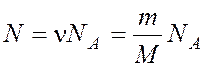 , где ν – число молей, NA – число
, где ν – число молей, NA – число
Авогадро. Тогда средняя кинетическая энергия поступательного движения молекул
водорода будет: 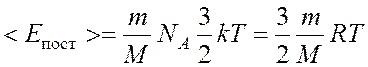 , (1) где
, (1) где
R = kNA – молярная
газовая постоянная.
Средняя кинетическая энергия вращательного движения
молекул водорода: 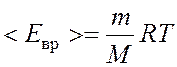 . (2)
. (2)
Подставляя числовые значения и формулы (1) и (2), имеем:

Ответ:
4986 кДж, 3324 кДж.
Задача 8. При адиабатическом сжатии давление воздуха было
увеличено от Р1 = 100 кПа до Р2 = 1 МПа.
Затем при неизменном объеме температура воздуха была понижена до
первоначальной. Определить давление Р3 газа в конце процесса.
§
можно определить ν:
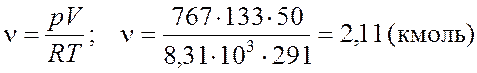
Число молекул N, содержащихся в данном объеме, находим, используя
число Авогадро NА
(которое определяет какое количество молекул содержится в одном киломоле).
Общее количество молекул, находящихся в массе m данного газа, может быть
установлено, так как известно число молей ν.
![]()
Подставляя в формулу число киломолей, устанавливаем
число молекул, содержащихся в объеме V: ![]() .
.
Плотность газа ρ = m/Vопределяем
из уравнения Менделеева — Клайперона:
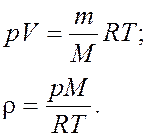
Подставляя числовые значения в единицах СИ в формулу, определим
плотность газа:
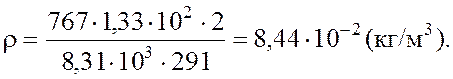
Удельный объем газа d определяем
из уравнения Менделеева — Клайперона:
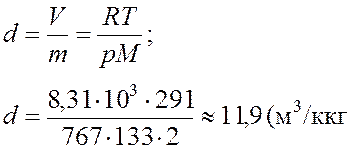
Ответ: 11,9
м3/кг.
Задача 2. В сосуде объемом 2 м3 находится смесь 4 кг гелия и 2 кг водорода при температуре 27°С. Определить давление и
молярную массу смеси газов.
М1 – егомолярная масса; V
– объем сосуда; Т –
температура газа; R= 8,31 Дж/(моль·К)
–молярная газовая постоянная; р2 –парциальное
давление водорода; m2 –
масса водорода; М2
– его молярная масса.
По закону Дальтона: ![]() (3)
(3)
Из уравнений (1) и (2) выразим р1 и
р2 и подставим в уравнение (3):
 (4)
(4)
С другой стороны, уравнение Менделеева — Клайперона
для смеси газов имеет вид:
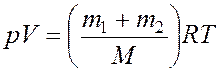 (5)
(5)
Сравнивая (4) и (5) найдем молярную массу смеси газов по формуле:
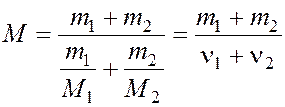 ,
,
(6)
где ν1 и ν2 – число молей гелия
и водорода соответственно.
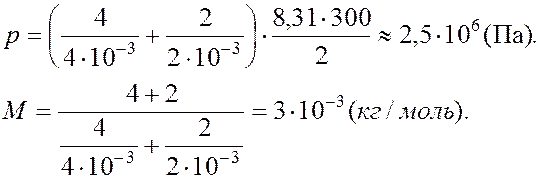
Ответ: 3·10-3 кг/моль.
Задача 3. При каком давлении средняя длина свободного пробега
молекул водорода <λ> = 2,5 см при температуре
68°С? Диаметр молекул водорода принять равным d = 2,3·10
–10 м.
Дано: <λ>= 2,5·10-2 м Т= 341 К d= 2,3·10-10 м NA = 6,02·1026 кмоль-1 | Решение: Давление |
р – ? |
Это проводится следующим образом:
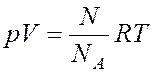 ;
;  ;
; 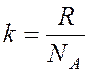 ;
;
где NA – число
Авогадро и k – постоянная Больцмана.
Следовательно, 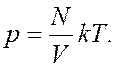 Так
Так
как 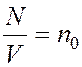 , имеем
, имеем ![]() .
.
Число молекул в 1 м3 выразим через среднюю длину свободного пробега. Из формулы 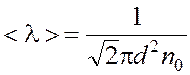 , находим
, находим 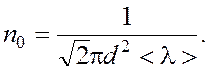 Таким образом:
Таким образом:
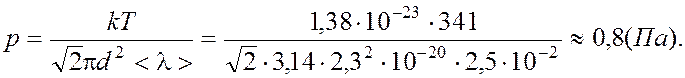
Ответ: 0,8
Па.
Задача 4. Определить
плотность разреженного азота, если средняя длина свободного пробега молекул 10 см. Какова концентрация молекул?
Дано: < λ >= 10 | Решение: Средняя |
р — ? n0 — ? |
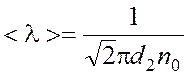 , (1)
, (1)
где
d–
эффективный диаметр молекул (для азота d = 0,31·10 –9 м).
Концентрацию молекул
найдем из равенства:
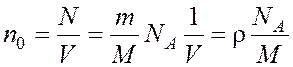 , (2) где
, (2) где
NA – число
Авогадро; М= 28·10 –3 кг/моль – молярная масса
азота.
Решая совместно уравнения (1) и (2), находим: 
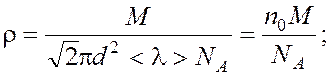
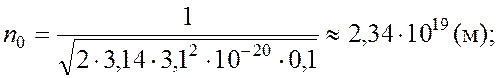
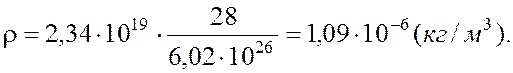
Ответ:
1,09·10-6 кг/м3.
Единицы измерения
Основной единицей измерения коэффициента диффузии в системе СИ является:
В СГС:
Коэффициент диффузии броуновской частицы
Для броуновской частицы, которую можно считать сферической коэффициент диффузии рассчитывают как:
где ![]()
![]()

![]()
![]()

![]()
Определение и формула коэффициента диффузии
Процесс диффузии двухкомпонентной системе для одномерного случая (![]()
![]()

![]()
![]()

![]()
![]()

![]()
![]()

![]()
Решение определим среднюю арифметическую скорость молекул гелия при нормальных условиях р = 10 5 па, т = 273 к. (1)
Решение Определим среднюю арифметическую скорость молекул гелия при нормальных условиях — страница №1/1

1.6. Процессы переноса
1.6.1.Средняя длина пробега молекул гелия при нормальных условиях равна
1.6. Процессы переноса
1.6.1.Средняя длина пробега молекул гелия при нормальных условиях равна
Решение
1. Определим среднюю арифметическую скорость молекул гелия при нормальных условиях р = 10 5 Па, Т = 273 К
![]() . (1)
. (1)
2. Подставим значение средней арифметической скорости в уравнение для коэффициента диффузии
![]() . (2)
. (2)
1.6.2. Диффузия кислорода при температуре Т = 273 К равна D = 1,910 5 м2/с. Определить при заданных условиях длину свободного пробега молекул.
Решение
1. Определим среднюю арифметическую скорость молекул кислорода при заданной температуре и молярной массе = 3210 3 кг/моль
![]() . (1)
. (1)
2. Запишем далее уравнение для коэффициента диффузии и решим его относительно средней длины свободного пробега
![]()
1.6.3. Определить отношение коэффициентов диффузии в двух состояниях азота N2: при нормальных условиях и при давлении р =100 Па с температурой Т = 300 К.
Решение
1.Для азота, находящегося в нормальных условиях уравнение коэффициента диффузии можно записать следующим образом
 , (1)
, (1)
где n1 концентрация молекул азота при нормальных условиях, молярная масса азота, d0 эффективный диаметр молекулы.
2. Выразим концентрацию n1 через давление
![]() . (2)
. (2)
3. Подставим значение концентрации молекул из уравнения (1) в уравнение (2)
 . (3)
. (3)
4. Запишем по аналогии с уравнением (3) соотношение для коэффициента диффузии для второго, заданного по условию задачи, состояния
 . (4)
. (4)
5. Найдём отношение D1/D2
 . (5)
. (5)
1.6.4. Найти отношение коэффициентов диффузии D1 газообразного кислорода О2 и газообразного водорода Н2, находящихся в одинаковых условиях.
1. Воспользуемся уравнением (1) предыдущей задачи
![]() ,
,  ,
, , (1)
где 1, 2 молярная масса кислорода и водорода, соответственно, d1, d2 эффективные диаметры молекул этих газов.
2. Найдём отношение коэффициентов диффузии
 . (2)
. (2)
1.6.5. Определить зависимость коэффициента диффузии D от температуры Т при изобарном изменении состояния. Привести качественный график зависимости.
Решение

1. Воспользуемся уравнением коэффициента диффузии, в котором концентрация молекул газа выражена через давление, коэффициент Больцмана и температуру, уравнение (3) задачи 1.6.3
![]() , (1)
, (1)
где С комбинация постоянных величин, входящих в уравнение (1).
2. Построим далее в относительных единицах график зависимости D .![]() .
.
1.6.6. Определить зависимость коэффициента диффузии D от температуры Т при изохорном изменении состояния. Привести качественный график зависимости.
Решение

1. Постоянство объёма и массы вещества обуславливает низменность концентрации молекул, таким образом, в уравнении коэффициента диффузии
![]() , (1)
, (1)
переменной величиной является только температура.
2. Коэффициент диффузии пропорционален корню квадратному из абсолютной температуры
![]() . (2)
. (2)
1.6.7. Определить зависимость коэффициента диффузии D от температуры Т при изобарном изменении состояния. Привести качественный график зависимости.
Решение
1. Воспользуемся уравнением (1) предыдущей задачи, выразив концентрацию молекул n через давление р и температуру Т

![]()
, (1)
![]() . (2)
. (2)
2. В уравнении (2) переменной величиной является только температура Т, потому его можно представить следующим образом
![]() , (3)
, (3)
т.е. коэффициент диффузии в изобарном процессе пропорционален корню квадратному из куба температуры.

1.6.8. Получить график зависимости коэффициента диффузии кислорода D от температуры Т в интервале температур 100 ≤ Т ≤ 1000 К при постоянном давлении p = const = 0,1 МПа.
Решение
1. Для получения графической зависимости ![]() воспользуемся уравнением (3) предыдущей задачи, определив предварительно численное значение коэффициента С
воспользуемся уравнением (3) предыдущей задачи, определив предварительно численное значение коэффициента С
![]()
,
![]() . (1)
. (1)
1.6.9. Во сколько раз изменится коэффициент диффузии молекул кислорода, находящихся в закрытом объёме, если количество молекул и температуру увеличить в четыре раза?
Решение
1. Увеличение числа молекул в четыре раза при фиксированном объёме приведёт к пропорциональному увеличению концентрации молекул. Уравнения для коэффициентов диффузии молекул газа в заданных условиях, с учётом уравнения (1) задачи 1.6.6 можно записать следующим образом
![]()
![]()
, (1)
2. Отношение коэффициентов диффузии, таким образом, определится соотношением
![]() . (2)
. (2)
1.6.10. Азот N2, находящийся в закрытом объёме подвергли мгновенному нагреву, увеличив температуру в 100 раз, так что половина молекул распалась на атомы. Во сколько раз, при этом, изменился коэффициент диффузии газа?
Решение
1. Если в первоначальном состоянии количество молекул обозначить через N, то после диссоциации молекул, количество частиц станет равным 1,5 N, другими словами, концентрация частиц увеличится в 1,5 раза.
2. Уравнения коэффициентов диффузии (1) предыдущей задачи можно переписать следующим образом
![]() ,
, ![]() ,
, . (1)
2. Изменение коэффициента диффузии представится следующим образом
![]() . (2)
. (2)
1.6.11. Определить динамическую вязкость кислорода О2, находящегося при температуре Т =273 К и давлении р = 0,1 МПа.
Решение
1. Коэффициент динамической вязкости идеального газа определяется уравнением
![]() , (1)
, (1)
где плотность газа, v средняя арифметическая скорость,![]() средняя длина свободного пробега молекул.
средняя длина свободного пробега молекул.
2. Плотность газа определим из уравнения Клайперона Менделеева
![]() . (2)
. (2)
3. Подставим в уравнение (1) значение плотности, средней арифметической скорости и средней длины свободного пробега
![]() . (3)
. (3)
4. Заменим далее значение концентрации n, воспользовавшись уравнением (1) задачи 1.6.7
![]() . (4)
. (4)
5. Подставим в уравнение (4) следующие значения параметров кислорода = 3210 3 кг/моль, d0 = 2,210 10м
![]() . (5)
. (5)
1.6.12. Определить среднюю длину свободного пробега ![]() молекул азота N2, находящегося в нормальных условиях, если его динамическая вязкость равна = 17 мкПас.
молекул азота N2, находящегося в нормальных условиях, если его динамическая вязкость равна = 17 мкПас.
Решение
1. Преобразуем уравнение (3) предыдущей задачи к следующему виду
![]() , (1)
, (1)
откуда
![]()
. (2)
2. Подставим в уравнение (2) заданные параметры: Т = 273 К, = 2810 3 кг/моль, р = 10 5 Па
![]() . (3)
. (3)
1.6.13. Найти динамическую вязкость гелия при нормальных условиях, если коэффициент диффузии равен D = 110 4 м2/с.
Решение
1. Запишем уравнения для коэффициентов динамической вязкости и диффузии
![]() . (1)
. (1)
2. Сравнение уравнений (1) даёт основание записать следующую зависимость для коэффициента динамической вязкости
![]() . (2)
. (2)
3. Плотность гелия ( = 410 3 кг/моль) определим из уравнения Клайперона Менделеева
![]() . (3)
. (3)
4. Подставим значение плотности из уравнения (3) в уравнение (2)
![]() . (4)
. (4)
1.6.14. Определить зависимость динамической вязкости от температуры Т при изобарном процессе. Зависимость представить графически.
Решение
1. Запишем уравнение коэффициента динамической вязкости
 , (1)
, (1)
![]() . (2)
. (2)

2. Таким образом, коэффициент динамической вязкости в изобарном процессе пропорционален единице, делённой на корень квадратной из абсолютной температуры. На рисунке в относительных единицах приведена зависимость = f(T)/
1.6.15.Определить зависимость динамической вязкости от температуры Т при изохорном процессе. Зависимость представить графически.

Решение
1. При V = сonst концентрация частиц остаётся тоже постоянной, поэтому, давление в уравнении плотности (3) предыдущей задачи целесообразно записать следующим образом
![]() . (1)
. (1)
2. Запишем уравнение для коэффициента динамической вязкости, подставив туда значения плотности , средней арифметической скорости v и средней длины свободного пробега ![]()
![]() , (2)
, (2)
из полученного уравнения (2) видно, что коэффициент динамической вязкости при изохорном процессе пропорционален корню квадратному из температуры, т.е. ![]() .
.
1.6.16. Установить зависимость коэффициента динамической вязкости от давления р при изотермическом процессе.
Решение
1. В данном случае целесообразно воспользоваться уравнением (1) задачи 1.6.14
![]() , (1)
, (1)
выразив концентрацию частиц тоже через давление
![]() . (2)
. (2)
2. Подставим значение концентрации n из уравнения (2) в уравнение для коэффициента динамической вязкости (1)
![]() . (3)
. (3)
3. Из уравнения (3) следует, после сокращения на р, что коэффициент динамической вязкости не зависит от давления.
1.6.17
.
Установить зависимость коэффициента динамической вязкости от давления р при изохорном процессе .Зависимость изобразить графически.
Решение
1. Запишем уравнение для коэффициента динамической вязкости в форме уравнения (3) предыдущей задачи
![]() . (1)
. (1)
2. Выразим далее переменную в данном случае величину Т из уравнения Клайперона Менделеева

![]()
(2)
и подставим это значение в уравнение (1)
![]() . (3)
. (3)
3. Таким образом ![]() . Качественный график зависимости = f(p) приведён на рисунке.
. Качественный график зависимости = f(p) приведён на рисунке.
1.6.18. Определить коэффициент динамической вязкости и коэффициент диффузии D воздуха, находящегося при нормальном давлении и температуре t = 10 0С. Диаметр молекул воздуха принять равным d0 310 10 м.
Решение
1.Определим коэффициент диффузии молекул воздуха
![]() . (1)
. (1)
2. Определим далее коэффициент динамической вязкости, выразив плотность воздуха из уравнения Клайперона Менделеева
![]() . (2)
. (2)
1.6.19. Имеются два известных идеальных газа, находящиеся в одинаковых условиях. Определить соотношение их коэффициентов динамической вязкости.
Решение
1. Введём следующие обозначения: молярные массы газов обозначим 1,2, эффективные диаметры молекул d1,d2. Коэффициенты динамической вязкости газов определяться следующими уравнениями
![]() ,
, ![]() ,
, (1)
2. Внесём молярные массы под корень и поделим уравнения (1) друг на друга
 . (2)
. (2)
Таким образом, при прочих равных условиях динамическая вязкость газов зависит от их молярных масс и эффективных диаметров молекул.
1.6.20. Заданы коэффициент динамической вязкости газа и коэффициент диффузии молекул D. Найти концентрацию молекул n.
Решение
1. Как было показано в задаче 1.6.18, коэффициент динамической вязкости и коэффициент диффузии связаны соотношением
![]() . (1)
. (1)
2. Преобразуем далее уравнение плотности следующим образом
![]()
![]()
. (2)
3. Подставим в уравнение (2) значение плотности из уравнения (1)
![]() . (3)
. (3)
1.6.21. Цилиндр радиусом R1 = 0,1 м и длиной l = 0,3 м на одной оси располагается внутри другого цилиндра радиусом R2 = 0,105 м. Малый цилиндр неподвижен, большой вращается вокруг геометрической оси с постоянной частотой n = 15 с 1. В пространстве между цилиндрами находится газ с коэффициентом динамической вязкости = 8,5 мкПа. Определить касательную силу F , действующую на поверхность внутреннего цилиндра площадью s = 1 м2 и приложенный к нему вращательный момент M(F).
Решение
1. Касательную силу, обусловленную эффектами вязкости, определим, воспользовавшись уравнением
 . (1)
. (1)

2. На внутренний неподвижный цилиндр действует пара сил, которые приложены в диаметрально противоположных точках неподвижного цилиндра. Модуль момента пары сил определяется в виде произведения модуля одной из сил на кратчайшее расстояние между линиями действия сил
![]()
1.6.21. Два горизонтальных диска радиусами R = 0,2 м расположены друг над другом так, что их оси совпадают. Расстояние между дисками d = 510 3 м. Верхний диск неподвижен, а нижний вращается с постоянной угловой скоростью = 62,8 рад/с. Между дисками находится воздух с коэффициентом динамической вязкости = 1,7210 5 Пас. Определить вращающий момент, приложенный к неподвижному диску.
Решение
1. Запишем уравнение касательной силы, возникающей вследствие эффектов внутреннего трения воздуха о поверхности диска
![]() . (1)
. (1)
2. На неподвижный диск будет действовать пара сил, приложенных в диаметрально противоположных точках обода неподвижного диска
![]() . (2)
. (2)
1.6.22. В ультраразреженном азоте, находящимся при давлении р = 1 мПа и температуре Т = 300 К, движутся друг относительно друга две параллельные пластины со скоростью u = 1 м/с. Расстояние между пластинами не изменяется и много меньше средней длины свободного пробега молекул. Определить силу внутреннего трения, действующую на пластины, если их площадь s = 1 м2.
Решение
1. Запишем уравнение силы внутреннего трения F
![]() , (1)
, (1)
в которое входит неизвестный коэффициент динамической вязкости.
2. Определим далее коэффициент динамической вязкости, воспользовавшись уравнением (3) задачи 1.6.16
![]() . (2)
. (2)
3. Поскольку расстояние между пластинами на много меньше средней длины свободного пробега молекул ультраразреженного газа, то можно принять, что z ![]() ,
,
![]() , (3)
, (3)
где ![]() средняя длина свободного пробега молекул газа.
средняя длина свободного пробега молекул газа.
4. Подставим значения z и в уравнение (1)
![]()

, (4)
после преобразований получим
![]() . (5)
. (5)
1.6.23. В разреженном газе с постоянной скоростью v движется шар радиуса r. Концентрация молекул газа n, масса одной молекулы m0, тепловые скорости молекул значительно меньше скорости шара. Определить силу сопротивления, действующую на шар.
Решение
1. Действующая со стороны газа на шар сила вызвана эффектами внутреннего трения.
![]() . (1)
. (1)
2. По условию задачи скорость шара во много раз больше средней арифметической скорости теплового движения молекул. Поэтому в первом приближении можно считать, что шар движется в неподвижной газовой среде, причём при соприкосновении с поверхностью шара молекулы изменяют свою скорость от нуля до v, поэтому v v, а z ![]() , т.е. длине свободного пробега.
, т.е. длине свободного пробега.
3. Определим коэффициент динамической вязкости разреженного газа
![]() . (2)
. (2)
3. Подставим значение в уравнение (1)
![]() , (3)
, (3)
где s = r2 площадь поперечного сечения шара.
4. Окончательное уравнение силы, действующей на шар примет следующий вид
![]() . (4)
. (4)
1.6.24. В разреженном газе с молярной массой движется в направлении своей оси диск радиуса r с постоянной скоростью v, которая много меньше средней арифметической скорости теплового движения. Определить силу, действующую на диск со стороны газа, если известны величина давления р и температуры Т.
Решение
1. Определим коэффициент динамической вязкости газа
![]() . (1)
. (1)
2. Изменение скорости молекул происходит на расстоянии равном средней длине свободного пробега молекул. Так как скорость диска меньше скорости движения молекул, то при попадании молекул на поверхность диска их скорость будет нулевой, другими словами,
![]() . (2)
. (2)

1.6.25. В разреженном газе с молярной массой движется пластина. Оценить, какую силу необходимо прикладывать к пластине в направлении движения, чтобы её скорость v была постоянной. Площадь пластины s, давление разреженного газа р, температура Т.Скорость пластины мала по сравнению со скоростью средней арифметической скоростью теплового движения молекул.
Решение
1. Движение пластины в разреженном газе будет замедленным, потому что вследствие эффектов внутреннего трения часть кинетической энергии будет расходоваться на совершение работы против силы внутреннего трения. Чтобы движение стало равномерным необходимо прикладывать в направлении движения силу, равную по модулю силе внутреннего трения.
2. Силу, обусловленную эффектами вязкости, определим, воспользовавшись уравнением (2) предыдущей задачи, с учётом того, что сила внутреннего трения будет приложена к двум поверхностям пластины, перпендикулярным направлению вектора скорости
![]() . (1)
. (1)
1.6.26. Дождевая капля радиусам r = 1,5 мм падает вертикально в воздушной среде при температуре воздуха Т = 300 К и нормальном атмосферном давлении. Диаметр молекул воздуха составляет d0 = 310 10 м. При решении считать, что справедлив закон Стокса. Оценить максимальную скорость капли.
Решение
1. Ускоренное движение дождевой капли происходит под действием двух, противоположно направленных сил: силы тяжести и силы сопротивления, возникающей вследствие вязкости воздуха
![]() . (1)
. (1)
2. Максимальной скорости капля достигнет в момент, когда сила тяжести станет равной силе сопротивления
![]() , (2)
, (2)
где = 103 кг/м3 плотность воды, g ускорение свободного падения, коэффициент динамической вязкости воздуха, vmax максимальная скорость дождевой капли.
3. Определим коэффициент динамической вязкости воздуха, воспользовавшись уравнением (1) задачи 1.6.24
![]() ,
,
![]() (3)
(3)
4. Разрешим уравнение (2) относительно максимальной скорости с учётом значения коэффициента динамической вязкости
![]() . (4)
. (4)
5. Следует отметить, что полученная величина скорости предполагает ламинарное обтекание сферической капли, т.е. без вихреобразования. Ситуация значительно отличается от реальной, по сути, в данной задаче не учитывается зависимость коэффициента аэродинамического сопротивления капли от скорости, которая будет иметь степенной вид.
1.6.27. В аэродинамической трубе продувается модель крыла самолёта со скоростью потока воздуха
v
= 200 м/с. Пограничный слой у крыла, где наиболее сильно проявляются эффекты внутреннего трения, составляет z = 0,02 м. Определить величину касательной силы F действующую на единичную площадь крыла. Испытания проводятся при температуре Т = 300 К.
Решение
1. В соответствии с законом Ньютона на единицу площади будет приходиться величина касательной силы внутреннего трения
![]() . (1)
. (1)
2. Значение коэффициента динамической вязкости воздуха определён в предыдущей задаче уравнением (3), будем считать, что скорость внутри пограничного слоя меняется линейно, от нуля на поверхности до скорости обтекания на границе слоя, т.е. v = v,
![]() . (2)
. (2)

1.6.28. Пространство между двумя коаксиальными цилиндрами заполнено кислородом при нормальном давлении р0 и температуре Т = 300 К. Радиусы цилиндров соответственно равны r1 = 0,1 м и r2 = 0,105 м. Внешний цилиндр вращается с постоянной угловой скоростью = 95 рад/с. Какой момент нужно приложить к внутреннему цилиндру, чтобы он не вращался? Длина цилиндров равна L = 0,4 м. Эффективный диаметр молекул кислорода принять равным d0 = 310-10 м.
Решение
1. Молекулы кислорода, адсорбированные на поверхности вращающегося цилиндра, будут иметь скорость поверхности v2 = r2. На поверхности внутреннего цилиндра скорость будет нулевой v1 = 0.
2. Касательная сила, действующая на поверхность цилиндра, обусловлена внутренним трением и определяется законом Ньютона
![]() , (1)
, (1)
где s = 2r1L площадь боковой поверхности внутреннего неподвижного цилиндра, z = r2 – r1 = 0,005 м расстояние между поверхностями цилиндров, на котором происходит изменение скорости молекул по линейному закону.
3. Определим далее коэффициент динамической вязкости кислорода при заданных условиях, воспользовавшись уравнением (3) задачи 1.6.26
 .(2)
.(2)
3. Подставим полученные значения величин в исходное уравнение касательной силы (1)
![]() . (3)
. (3)
4. Момент, действующий на внутренний цилиндр, определится как
![]() . (4)
. (4)
1.6.29. Пространство между двумя коаксиальными цилиндрами радиусами r1 = 5 см и r2 = 5,2 см заполнено газом. Внешний цилиндр вращается с постоянной угловой скоростью = 38 рад/с. Для сохранения неподвижности внутреннего цилиндра высотой L =0,2 м к нему приложили касательную силу F = 1,410 3 Н. Определить, используя эти данные, величину коэффициента динамической вязкости газа, заполняющего пространство между цилиндрами.
Решение
1. Коэффициент динамической вязкости выразим из закона Ньютона, определяющего силу внутреннего трения, используя уравнение (3) предыдущей задачи
 (1)
(1)

1.6.30. Между двумя длинными коаксиальными цилиндрами радиуса r1 и r2 находится разреженный газ. Внутренний цилиндр вращается с постоянной угловой скоростью 1. Оценить угловую скорость вращения внешнего цилиндра 2.
Решение
1. Наружный цилиндр раскручивается посредствам вращающего момента, обусловленного силами внутреннего трения, величина которых определяется законом Ньютона.
2. В стационарном состоянии цилиндры будут вращаться с постоянными угловыми скоростями 1 и 2, что даёт основание считать, что приложенные к ним касательные силы одинаковы, т.е.
![]() , (1)
, (1)
где s1 и s2 площади поверхностей коаксиальных цилиндров.
3. В данном случае: v1 = v1 = 1r1; 2 = v2 = 2r2; s1 = r1L; s2 = r2L. Таким образом, уравнение (1) перепишется следующим образом
 . (2)
. (2)
1.6.31. Вычислить теплопроводность гелия, находящегося при нормальных условиях.
Решение
1. Запишем уравнение коэффициента теплопроводности в виде
![]() . (1)
. (1)
2. Примем следующие значения входящих в уравнение (1) величин: d0 = 210 10 м; = 410 3 кг/моль; Т = 273 К.
3. Упростим уравнение (1) и подставим значения входящих в него величин
![]() . (2)
. (2)
1.6.32. В приближённой теории явлений переноса взаимосвязь между коэффициентами теплопроводности и динамической вязкости описывается соотношением / = сV, где сV удельная теплоёмкость газа при постоянном объёме. В более строгой теории соотношение представляется в виде / = КсV, где К = (9 — 5)/4 постоянный безразмерный коэффициент, определяемый значением показателя адиабаты. Используя табличные данные коэффициента теплопроводности, найти значение К для: 1) аргона Ar, 2) водорода H2, 3) кислорода O2, 4) паров воды H2O.
Решение
1. Примем для сравнения следующие значения коэффициентов теплопроводности для заданных веществ в газообразном состоянии
| № | Вещество | Динамическая вязкость , Пас | Теплопроводность , мВт/(мК) |
| 1 | Аргон (Ar) | 2,1510 5 | 16,2 |
| 2 | Водород (Н2) | 8,6610 6 | 24,1 |
| 3 | Кислород (О2) | 2,4410 5 | 24,4 |
| 4 | Пары воды (Н2О) | 8,3210 6 | 15,8 |
2. Определим значение коэффициента К и показателя адиабаты = (i 2)/i, где i число степеней свободы молекулы
| № | Вещество | Число степеней свободы i | Показатель адиабаты | Коэффициент К |
| 1 | Аргон (Ar) | 3 | 1,67 | 2,51 |
| 2 | Водород (Н2) | 5 | 1,4 | 1,9 |
| 3 | Кислород (О2) | 5 | 1,4 | 1,9 |
| 4 | Пары воды (Н2О) | 6 | 1,33 | 1,74 |
3. Вычислим удельные теплоёмкости газов при постоянном давлении, воспользовавшись уравнением
![]()
:
аргона ![]() ,
,
водорода ![]() ,
,
кислорода ![]() ,
,
паров воды ![]() .
.
4. Определим значение безразмерного коэффициента К для заданных веществ, воспользовавшись уравнением / = КсV , откуда ![]() :
:
для аргона ![]() ,
,
для водорода ![]() ,
,
для кислорода ![]() ,
,
для паров воды ![]() .
.
1.6.33. Коэффициент динамической вязкости воздуха, находящегося в нормальных условиях равен = 17,210 6 Пас. Определить коэффициент теплопроводности воздуха при тех же условиях.
Решение
1. Коэффициенты вязкости и теплопроводности связаны соотношением
![]() , (1)
, (1)
где К = (9 5)/4 = 1,74 постоянный безразмерный коэффициент, = (i 2)/i = 1,33 показатель адиабаты, i = 6 число степеней свободы молекулы воздуха, сV = iR/2 = 830 Дж/(кгК)
2. Выразим из уравнения (1) коэффициент теплопроводности и определим его величину
![]() . (2)
. (2)

1.6.34. Найти зависимость теплопроводности от температуры Т при изобарном процессе. Зависимость изобразить графически.
Решение
1. Запишем уравнение для коэффициента теплопроводности
![]() , (1)
, (1)
![]() . (2)
. (2)
2. Коэффициент теплопроводности, таким образом, прямо пропорционален корню квадратному из абсолютной температуры, на рисунке приведена качественная зависимость.
1.6.35.Найти зависимость теплопроводности от температуры Т при изохорном процессе. Зависимость изобразить графически.
Решение
1. При изохорном процессе, V = const концентрация молекул газа предполагается постоянной, поэтому уравнение коэффициента теплопроводности целесообразно следующим образом
![]() . (1)
. (1)
2. При изохорном процессе коэффициент, так же как и в предыдущей задаче прямо пропорционален корню квадратному из абсолютной температуры. Качественная зависимость = f(T) будет иметь такой же вид, как и в предыдущей задаче.
1.6.36
.
Найти зависимость теплопроводности от давления р при изотермическом процессе.
Решение
1. Для анализа зависимости = f(p) воспользуемся зависимостью (1) задачи 1.6.34
![]() . (1)
. (1)
Как видно из приведенного уравнения, коэффициент теплопроводности при постоянстве температуры не зависит от давления.

1.6.37. Найти зависимость теплопроводности от давления р при изохорном процессе. Зависимость изобразить графически.
Решение
1. При постоянном объёме концентрация молекул газа n и его плотность постоянны, уравнение коэффициента теплопроводности в этом случае можно представить следующим образом
![]() , (1)
, (1)
преобразуем в последнем уравнении комбинацию величин RT посредствам уравнения Клайперона Менделеева
![]() , (2)
, (2)
где плотность газа.
2. Подставим значение RT в уравнение (1)
![]() , (3)
, (3)
т.е. коэффициент теплопроводности при постоянном объёме пропорционален корню квадратному из величины давления ![]() .
.
1.6.38. Построить график зависимости коэффициента теплопроводности водорода от температуры в интервале температур 100 ≤ Т ≤ 600 К.
Решение
1. Запишем уравнение коэффициента теплопроводности в следующем виде

![]()
![]() , (1)
, (1)
![]() . (2)
. (2)
2. Подставим табличные значения величин в уравнение (2): = 210 3 кг/моль, d0 = 2,810 10 м, сV = iR/(2) = 10375 Дж/кгК
![]() . (3)
. (3)
3. Составим таблицу расчетных значений коэффициента теплопроводности водорода Н2 и построим график зависимости = f(T).
| Т, К | 100 | 300 | 500 | 700 | 900 | 1000 |
| , Вт/мК | 0,028 | 0,048 | 0,06 | 0,074 | 0,084 | 0,088 |
1.6.39. Углекислый газ СО2 и азот N2 находятся в одинаковых условиях. Определить отношение коэффициентов диффузии, коэффициентов динамической вязкости и коэффициентов теплопроводности, считая эффективные диаметры молекул одинаковыми.
Решение
1. Запишем уравнение для определения коэффициента диффузии
![]() , (2)
, (2)
как видно, при прочих равных условиях, отношение коэффициентов диффузии углекислого газа и азота будет определяться молярными массами
![]() . (3)
. (3)
2. Проанализируем далее уравнение коэффициента динамической вязкости (см. задачу 1.6.28)
![]() , (4)
, (4)
отношение коэффициентов динамической вязкости так же определяется молярными массами
![]() . (5)
. (5)
3. уравнение коэффициента теплопроводности можно представить следующим образом
![]() , (6)
, (6)
откуда очевидно, что
![]() . (7)
. (7)
1.6.40 Расстояние между внутренними зеркальными стенками термоса составляет h = 5 мм. До какой величины нужно довести давление во внутренней полости, чтобы теплопроводность воздуха начала уменьшаться?. Температура окружающей среды составляет 300 К, эффективный диаметр молекул воздуха принять равным d0 = 310 10м.
Решение
1. Термос представляет собой сосуд, теплоизолированный от внешней среды. Величина теплового потока через поверхность определяется законом Фурье
![]() , (1)
, (1)
где ![]() градиент температуры, s площадь, расположенная перпендикулярно направлению теплового потока, коэффициент теплопроводности прилегающей к стенке среды.
градиент температуры, s площадь, расположенная перпендикулярно направлению теплового потока, коэффициент теплопроводности прилегающей к стенке среды.
2. При прочих равных условиях величина теплового потока определяется коэффициентом теплопроводности и начнёт уменьшаться в том случае, когда средняя длина свободного пробега молекул станет равной расстоянию между стенками термоса, т.е. h ![]()
![]() . (2)
. (2)
3. Разрешим далее уравнение (2) относительно давления
![]() . (3)
. (3)
Формулы для коэффициента диффузии
В соответствии с кинетической теорией газов коэффициент диффузии можно вычислить как:
где ![]()
![]()

![]()
![]()

![]()
