§6.5 применение кислорода
§6.5 Применение кислорода.
Кислород необходим практически всем живым существам. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни. К счастью, атмосфера Земли пока не испытывает заметного недостатка кислорода, но такая опасность может возникнуть в будущем.
Вне земной атмосферы человек вынужден брать с собой запас кислорода. Мы уже говорили о его применении на подводных лодках. Точно так же полученный искусственно кислород используют для дыхания в любой чуждой среде, где приходится работать людям: в авиации при полетах на больших высотах, в пилотируемых космических аппаратах, при восхождении на высокие горные вершины, в экипировке пожарных, которым часто приходится действовать в задымленной и ядовитой атмосфере и т.д.
Во всех этих устройствах есть источники кислорода для автономного дыхания.
В медицине кислород используют для поддержания жизни больных с затрудненным дыханием и для лечения некоторых заболеваний. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
Но главными потребителями кислорода, конечно, являются энергетика, металлургия и химическая промышленность.
Электрические и тепловые станции, работающие на угле, нефти или природном газе используют атмосферный кислород для сжигания топлива. Если даже небольшой автомобиль является настоящим «пожирателем» кислорода (как мы выяснили в предыдущей главе), то гигантские тепловые и электрические станции расходуют кислорода неизмеримо больше. До сих пор они вырабатывают около 80 % всего электричества в нашей стране и только остальные 20 % электроэнергии дают гидростанции и атомные станции, не расходующие атмосферного кислорода.
Для металлургической и химической промышленности нужен уже не атмосферный, а чистый кислород. Ежегодно во всем мире получают свыше 80 млн. тонн кислорода. Для его производства требуется огромное количество электроэнергии, получение которой, как мы уже знаем, тоже связанос расходованием кислорода.
Чистый кислород расходуется главным образом на получение стали из чугуна и металлолома. С этим важным процессом вы познакомитесь в следующем классе.
В машиностроении, в строительстве кислород используют для сварки и резки металлов. Горючий газ ацетилен, сгорая в токе кислорода, позволяет получить температуру выше 3000°
С! Это приблизительно вдвое больше температуры плавления железа.
2 C2H2 | 5 O2 | = | 4 CO2 | 2 H2O | теплота | |||
ацетилен |
 Ацетиленовая горелка состоит из двух трубок, вставленных одна в другую. В одну трубку подается кислород, в другую – ацетилен, после чего смесь газов поджигается. Таким пламенем можно расплавить металлические детали в месте их соединения, то есть сварить их между собой.
Ацетиленовая горелка состоит из двух трубок, вставленных одна в другую. В одну трубку подается кислород, в другую – ацетилен, после чего смесь газов поджигается. Таким пламенем можно расплавить металлические детали в месте их соединения, то есть сварить их между собой.
Немного по-другому осуществляют резку металла. Если сначала сильно разогреть металл ацетиленовой горелкой, а затем уменьшить поток ацетилена и увеличить поток кислорода, то получается «кислородный резак». Железо, как мы знаем, горит в кислороде. Поэтому дальнейшее горение поддерживается уже без участия ацетилена, а струя кислорода прожигает металл, превращая его в оксиды железа. Сноп искр, вырывающихся из прожигаемого кислородом металла — это раскаленные частицы железной окалины.
_________________
Атом и молекула кислорода. формула кислорода. строение кислорода:
Кислород – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением О и атомным номером 8. Расположен в 16-й группе (по старой классификации — главной подгруппе шестой группы), втором периоде периодической системы.
Кислород самый лёгкий элемент периодической таблицы химических элементов Д. И. Менделеева из группы халькогенов.
Кислород – химически активный неметалл.
Кислород обозначается символом О.
Как простое вещество кислород (химическая формула O2) при нормальных условиях представляет собой двухатомный газ без цвета, вкуса и запаха. В жидком состоянии кислород имеет светло-голубой цвет, а в твёрдом – представляет собой кристаллы светло-синего цвета.
Молекула кислорода двухатомна. Также встречается аллотропная модификация кислорода – озон, молекула которого состоит из трёх атомов кислорода.
Химическая формула кислорода O2 (или O3 – озон).
Электронная конфигурация атома кислорода 1s2 2s2 2p4. Потенциал ионизации (первый электрон) атома кислорода равен 1313,94 кДж/моль (13,618055(7) эВ).
Строение атома кислорода. Атом кислорода (наиболее распространенный из трех изотопов кислорода (99,757 %) – 168О) состоит из положительно заряженного ядра ( 8), вокруг которого по атомным оболочкам движутся восемь электронов.
При этом 2 электрона находятся на внутреннем уровне, а 6 электронов – на внешнем. Поскольку кислород расположен во втором периоде, оболочки всего две. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внешняя оболочка представлена s- и р-орбиталями.
Два спаренных электрона находится на 1s-орбитали, вторая пара электронов – на 2s-орбитали. На 2р-орбитали находится два спаренных и два неспаренных электрона. Поэтому во всех своих соединениях кислород проявляет валентность II. В свою очередь ядро атома кислорода состоит из восьми протонов и восьми нейтронов. Кислород относится к элементам p-семейства.
Радиус атома кислорода (вычисленный) составляет 48 пм.
Атомная масса атома кислорода составляет 15,99903-15,99977 а. е. м.
Кислород – самый распространённый химический элемент на Земле. В земной коре на его долю в составе различных соединений приходится около 46 % массы. Морские и пресные воды содержат по массе 86 % кислорода (если быть точнее – 85,82 %). В человеке его содержание составляет по массе 61 %.
При высокой температуре молекула кислорода О2 обратимо диссоциирует на атомарный кислород. При 2000 °C на атомарный кислород диссоциирует 0,03 % молекулярного кислорода, при 2600 °C – 1 %, при 4000 °C – 59 %, при 6000 °C — 99,5 %.
Все тесты
- Тест на темуАнализ стихотворения «Не с теми я, кто бросил землю» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Перемена» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Стихи о Петербурге» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Стихи к Блоку» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «Клеветникам России» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Завещание» Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «Стихи о Москве» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «Молитва» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «И. И. Пущину!» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «День и ночь» Ф. Тютчева5 вопросов
- Тест на темуАнализ стихотворения «Весна в лесу» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Журавли» Р. Гамзатова5 вопросов
- Тест на темуАнализ стихотворения «Люблю» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения «Когда на меня навалилась беда» К. Кулиева5 вопросов
- Тест на темуАнализ стихотворения «Гамлет» Б. Пастернака5 вопросов
- Тест на темуАнализ стихотворения «Русь» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Ночь» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения К. Симонова «Ты помнишь, Алёша, дороги Смоленщины…»5 вопросов
- Тест на темуАнализ стихотворения Жуковского «Приход весны»5 вопросов
- Тест на темуАнализ стихотворения Анны Ахматовой «Сероглазый король»5 вопросов
- Тест на темуАнализ стихотворения «Июль – макушка лета…»5 вопросов
- Тест на темуАнализ стихотворения «Мелколесье. Степь и дали…» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Не позволяй душе лениться» Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «На дне моей жизни» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Нивы сжаты, рощи голы…» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Бабушкины сказки» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Снежок» Н. Некрасова1 вопрос
- Тест на темуАнализ стихотворения «По вечерам» Н. Рубцова5 вопросов
- Тест на темуАнализ стихотворения «Вчерашний день, часу в шестом…» Н. Некрасова5 вопросов
- Тест на темуАнализ стихотворения «Цветы последние милей…» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Я знаю, никакой моей вины…» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Я не ищу гармонии в природе»Н. Заболоцкого5 вопросов
- Тест на темуАнализ стихотворения «Разбуди меня завтра рано» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Снега потемнеют синие» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Осень» Н. Карамзина5 вопросов
- Тест на темуАнализ стихотворения «Молитва» А. Ахматовой5 вопросов
- Тест на темуАнализ стихотворения «Вечер» А. Фета5 вопросов
- Тест на темуАнализ стихотворения «Не жалею, не зову, не плачу» С. Есенина5 вопросов
- Тест на темуАнализ стихотворения «Тучи» М. Лермонтова5 вопросов
- Тест на темуАнализ стихотворения «Книга» Г. Тукая5 вопросов
- Тест на темуАнализ стихотворения «Необычайное приключение, бывшее с Владимиром Маяковским летом на даче» В. Маяковского5 вопросов
- Тест на темуАнализ стихотворения «Деревня» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Летний вечер» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Я убит подо Ржевом» А. Твардовского5 вопросов
- Тест на темуАнализ стихотворения «Элегия» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Зимнее утро» А. Пушкина5 вопросов
- Тест на темуАнализ стихотворения «Троица» И. Бунина5 вопросов
- Тест на темуАнализ стихотворения «Бабушке» М. Цветаевой5 вопросов
- Тест на темуАнализ стихотворения «О весна без конца и краю» А. Блока5 вопросов
- Тест на темуАнализ стихотворения «Море» В. Жуковского5 вопросов
История открытия
Что такое воздух? Древние народы глубоко задумывались над этим вопросом. И это не удивительно, когда понимаешь, насколько важен воздух для многих процессов. Объекты не могут гореть без воздуха. Человек не может выжить без воздуха. На самом деле, древние народы думали, что воздух должен быть «элементом».
Но они использовали слово «элемент» в несколько ином значении, нежели современные учёные. Для древних людей элемент был чем-то очень важным и основным. Воздух соответствует этому описанию, наряду с огнём, водой и землёй. Впоследствии многие учёные повлияли на открытие такого элемента, как кислород:
- Первым человеком в Западной Европе, который описал «части» воздуха, был итальянский художник и учёный Леонардо да Винчи (1452−1519). Леонардо отметил, что воздух не полностью расходуется, когда в нем что-то сжигается. Поэтому он сказал, что воздух должен состоять из двух частей: одной части, которая расходуется на горение, и одной части, которая не участвует в процессе. В течение многих лет идеи Леонардо были не очень популярны среди учёных. Проблема заключалась в том, что у первых химиков не было хорошего оборудования, как в современных лабораториях. Им было сложно собрать образцы воздуха, а затем изучить его.
- В начале 1700-х химики начали узнавать больше о воздухе, но несколько окольным путём. Например, в 1771 и 1772 годах Карл Вильельм Шееле изучал влияние тепла на ряд соединений. В одном эксперименте он использовал карбонат серебра (Ag 2 CO 3), карбонат ртути (HgCO 3) и нитрат магния (Mg (NO 3) 2). Когда он нагревал эти соединения, он обнаружил, что выделялся газ. Затем он изучил свойства этого газа и обнаружил, что пламя ярко горело в нём. Он также заметил, что животные в нём могут безболезненно находиться. Не зная этого, Шееле открыл кислород.
- Примерно через два года Джозеф Пристли провёл аналогичные эксперименты, нагревая оксид ртути (HgO) в пламени. Соединение распалось, в результате чего образовались жидкая металлическая ртуть и газ. Когда Пристли проверил новый газ, он обнаружил те же свойства и характеристики, что и Шееле. Пристли даже пытался вдохнуть тот газ, получение которого ему удалось осуществить.
- Антуана-Лорана Лавуазье (1743−94) часто называют отцом современной химии. Он получил это звание по ряду причин. Наиболее важной из них является объяснение, которое он открыл для процесса сгорания (горения). До исследования Лавуазье химики считали, что горящий объект выделяет вещество в воздух. Они назвали это вещество флогистоном. Например, когда горело дерево, химики говорили, что флогистон перешёл из дерева в воздух. Лавуазье показал, что эта идея неверна. Когда что-то горит, это на самом деле происходит реакция с кислородом в воздухе. Горение, сказал Лавуазье, — это просто окисление (процесс, при котором какое-либо вещество соединяется с О2). Это открытие дало химикам совершенно новый взгляд на химические изменения. Теория флогистона постепенно начала вымирать. Начали развитие многие идеи, которые сегодня используются в современной химии.
Некоторые люди думают, что Шееле следует отдать должное за открытие кислорода. Он завершил свои эксперименты раньше, чем Пристли. Но его издатель очень медленно печатал отчёты учёного. Они действительно вышли после отчётов Пристли. Таким образом, большинство историков сходится во мнении, что Шееле и Пристли должны разделить между собой право на открытие кислорода.
Ни Шееле, ни Пристли до конца не понимали важность их открытия. Этот шаг был предпринят французским химиком Антуаном-Лораном Лавуазье (1743−94). Лавуазье был первым человеком, который объявил, что новый газ является элементом. Он был также первым человеком, который объяснил, как кислород участвует в горении. Кроме того, он предложил название для газа.
Слово oxygenium («кислород») происходит от греческих слов, обозначающих «рождающий кислоту». Лавуазье выбрал такое название, потому что думал, что все кислоты содержат О2. Поэтому новый элемент отвечал за «образование кислот». Однако в этом отношении Лавуазье ошибся. Не все кислоты содержат кислород.
Получение кислорода в лаборатории
Лабораторные методы получения кислорода основаны на химических реакциях.
Дж. Пристли получал этот газ из соединения, название которого — меркурий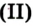
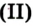 Рис. 54.Получение кислорода нагреванием меркурий
Рис. 54.Получение кислорода нагреванием меркурий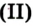 оксида
оксида
Соответствующее химическое уравнение:
Сейчас метод Пристли не используют, поскольку пары ртути токсичны. Кислород получают с помощью других реакций, подобных рассмотренной. Они, как правило, происходят при нагревании.
Реакции, при которых из одного вещества образуются несколько других, называют реакциями разложения.
Для получения кислорода в лаборатории используют такие оксигенсодержащие соединения:
Небольшое количество катализатора — манган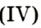
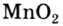
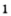 Получение кислорода разложением гидроген пероксида
Получение кислорода разложением гидроген пероксида 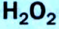 Налейте в пробирку 2 мл раствора гидроген пероксида (традиционное название этого вещества — перекись водорода). Зажгите длинную лучинку и погасите ее (как вы это делаете со спичкой), чтобы она едва тлела. Насыпьте в пробирку с раствором гидроген пероксида немного катализатора — черного порошка манган
Налейте в пробирку 2 мл раствора гидроген пероксида (традиционное название этого вещества — перекись водорода). Зажгите длинную лучинку и погасите ее (как вы это делаете со спичкой), чтобы она едва тлела. Насыпьте в пробирку с раствором гидроген пероксида немного катализатора — черного порошка манган
Составьте уравнение реакции разложения гидроген пероксида, если вторым продуктом реакции является вода
В лаборатории кислород можно также получить разложением натрий нитрата 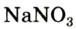

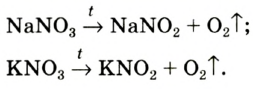
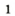
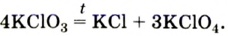
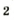 селитры.Кислород вместе с водородом являются продуктами разложения воды под действием электрического тока:
селитры.Кислород вместе с водородом являются продуктами разложения воды под действием электрического тока: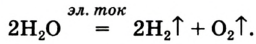
Применение кислорода:
Таблица химических элементов Д.И. Менделеева
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева
Распространённость в природе.
К. – самый распространённый химич. элемент на Земле: содержание химически связанного К. в гидросфере составляет 85,82% (гл. обр. в виде воды), в земной коре – 49% по массе. Известно более 1400 минералов, в состав которых входит К. Среди них преобладают минералы, образованные солями кислородсодержащих кислот (важнейшие классы – карбонаты природные, силикаты природные, сульфаты природные, фосфаты природные), и горные породы на их основе (напр., известняк, мрамор), а также разл. оксиды природные, гидроксиды природные и горные породы (напр., базальт). Молекулярный К. составляет 20,95% по объёму (23,10% по массе) земной атмосферы. К. атмосферы имеет биологич. происхождение и образуется в зелёных растениях, содержащих хлорофилл, из воды и диоксида углерода при фотосинтезе. Количество К., выделяемое растениями, компенсирует количество К., расходуемое в процессах гниения, горения, дыхания. К. – биогенный элемент – входит в состав важнейших классов природных органич. соединений (белков, жиров, нуклеиновых кислот, углеводов и др.) и в состав неорганич. соединений скелета.
Распространенность оксигена в природе
Оксиген — один из самых распространенных элементов на нашей планете. В земной коре его атомов больше, чем атомов любого другого элемента (§ 6). Атомы Оксигена содержатся в песке, глине, известняке, многих минералах. Оксиген — второй по распространенности в атмосфере (после Нитрогена) и в гидросфере (после Гидрогена).
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 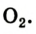
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 02. Это вещество содержит молекулы, состоящие из двух атомов Оксигена.
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
02 = 20.
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5 объема воздуха. Состав сухого воздуха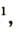
Организм взрослого мужчины ежесуточно потребляет приблизительно 900 г кислорода, а женщины — 600 г.
Состав воздуха:
Газ компонент воздуха Доля воздуха в%
| Название | Формула | объемная* | массовая |
| Азот | 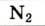 | 78,09 | 75,51 |
| Кислород | 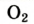 | 20,95 | 23,15 |
| Аргон | 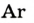 | 0,93 | 1,28 |
| углекислый газ | 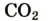 | 0,037 | 0,056 |
| Другие газы | менее 0,002 | менее 0,003 |
* Объемная доля вещества в смеси — отношение объема вещества к объему смеси. Объемную долю обозначают греческой буквой 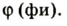
Определить объемную долю кислорода в воздухе можно экспериментально. Для этого нужны стеклянная бутылка без дна с пробкой и кристаллизатор с водой. В пробку вставляют ложку для сжигания, в которую набрано немного красного фосфора. Его поджигают, быстро вносят в бутылку и плотно I закрывают ее пробкой (рис. 52).
Кислород содержится не только в атмосфере. Небольшое его количество вместе с другими газами воздуха растворено в природной воде.
Существует еще одно простое вещество Оксигена — озон 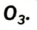 Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород:
Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород: 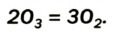
Озон содержится в атмосфере в незначительном количестве; его объемная доля не превышает
Определение объемной доли кислорода в воздухе сжиганием фосфора:
а — начало опыта;
б — окончание опыта
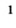
1 0,0004 %. Распадаясь, он поглощает часть ультрафиолетовых лучей солнечного света, вредную для растений и животных, и тем самым оберегает природу.
Свойства
Строение внешней электронной оболочки атома К. 2s22p4; в соединениях проявляет степени окисления –2, –1, редко 1, 2; электроотрицательность по Полингу 3,44 (наиболее электроотрицательный элемент после фтора); атомный радиус 60 пм; радиус иона О2– 121 пм (координац. число 2). В газообразном, жидком и твёрдом состояниях К. существует в виде двухатомных молекул О2. Молекулы О2 парамагнитны. Существует также аллотропная модификация К. – озон, состоящая из трёхатомных молекул О3.
В осн. состоянии атом К. имеет чётное число валентных электронов, два из которых не спарены. Поэтому К., не имеющий низкой по энергии вакантной d-орбитали, в большинстве химич. соединений двухвалентен. В зависимости от характера химич. связи и типа кристаллич. структуры соединения координац. число К. может быть разным: 0 (атомарный К.), 1 (напр., О2, СО2), 2 (напр., Н2О, Н2О2), 3 (напр., Н3О ), 4 (напр., оксоацетаты Ве и Zn), 6 (напр., MgO, CdO), 8 (напр., Na2O, Cs2O). За счёт небольшого радиуса атома К. способен образовывать прочные π-связи с др. атомами, напр. с атомами К. (О2, О3), углерода, азота, серы, фосфора. Поэтому для К. одна двойная связь (494 кДж/моль) энергетически более выгодна, чем две простые (146 кДж/моль).
Парамагнетизм молекул О2 объясняется наличием двух неспаренных электронов с параллельными спинами на дважды вырожденных разрыхляющих π*-орбиталях. Поскольку на связывающих орбиталях молекулы находится на четыре электрона больше, чем на разрыхляющих, порядок связи в О2 равен 2, т. е. связь между атомами К. двойная. Если при фотохимич. или химич. воздействии на одной π*-орбитали оказываются два электрона с противоположными спинами, возникает первое возбуждённое состояние, по энергии расположенное на 92 кДж/моль выше основного. Если при возбуждении атома К. два электрона занимают две разные π*-орбитали и имеют противоположные спины, возникает второе возбуждённое состояние, энергия которого на 155 кДж/моль больше, чем основного. Возбуждение сопровождается увеличением межатомных расстояний О–О: от 120,74 пм в осн. состоянии до 121,55 пм для первого и до 122,77 пм для второго возбуждённого состояния, что, в свою очередь, приводит к ослаблению связи О–О и к усилению химич. активности К. Оба возбуждённых состояния молекулы О2 играют важную роль в реакциях окисления в газовой фазе.
К. – газ без цвета, запаха и вкуса; tпл –218,3 °C, tкип –182,9 °C, плотность газообразного К. 1428,97 кг/дм3 (при 0 °C и нормальном давлении). Жидкий К. – бледно-голубая жидкость, твёрдый К. – синее кристаллич. вещество. При 0 °C теплопроводность 24,65·10—3 Вт/(м·К), молярная теплоёмкость при постоянном давлении 29,27 Дж/(моль·К), диэлектрич. проницаемость газообразного К. 1,000547, жидкого 1,491. К. плохо растворим в воде (3,1% К. по объёму при 20 °C), хорошо растворим в некоторых фторорганич. растворителях, напр. перфтордекалине (4500% К. по объёму при 0 °C). Значит. количество К. растворяют благородные металлы: серебро, золото и платина. Растворимость газа в расплавленном серебре (2200% по объёму при 962 °C) резко понижается с уменьшением темп-ры, поэтому при охлаждении на воздухе расплав серебра «закипает» и разбрызгивается вследствие интенсивного выделения растворённого кислорода.
К. обладает высокой реакционной способностью, сильный окислитель: взаимодействует с большинством простых веществ при нормальных условиях, в осн. с образованием соответствующих оксидов (мн. реакции, протекающие медленно при комнатной и более низких темп-рах, при нагревании сопровождаются взрывом и выделением большого количества теплоты). К. взаимодействует при нормальных условиях с водородом (образуется вода Н2О; смеси К. с водородом взрывоопасны – см. Гремучий газ), при нагревании – с серой (серы диоксид SO2 и серы триоксид SO3), углеродом (углерода оксид СО, углерода диоксид СО2), фосфором (фосфора оксиды), мн. металлами (оксиды металлов), особенно легко со щелочными и щёлочноземельными (в осн. пероксиды и надпероксиды металлов, напр. пероксид бария BaO2, надпероксид калия KO2). С азотом К. взаимодействует при темп-ре выше 1200 °C или при воздействии электрич. разряда (образуется монооксид азота NO). Соединения К. с ксеноном, криптоном, галогенами, золотом и платиной получают косвенным путём. К. не образует химич. соединений с гелием, неоном и аргоном. Жидкий К. также является сильным окислителем: пропитанная им вата при поджигании мгновенно сгорает, некоторые летучие органич. вещества способны самовоспламеняться, когда находятся на расстоянии нескольких метров от открытого сосуда с жидким кислородом.
К. образует три ионные формы, каждая из которых определяет свойства отд. класса химич. соединений: $ce{O2^-}$– супероксидов (формальная степень окисления атома К. –0,5), $ce{O2^2^-}$ – пероксидных соединений (степень окисления атома К. –1, напр. водорода пероксид Н2О2), О2– – оксидов (степень окисления атома К. –2). Положительные степени окисления 1 и 2 К. проявляет во фторидах O2F2 и ОF2 соответственно. Фториды К. неустойчивы, являются сильными окислителями и фторирующими реагентами.
Молекулярный К. является слабым лигандом и присоединяется к некоторым комплексам Fe, Co, Mn, Cu. Среди таких комплексов наиболее важен железопорфирин, входящий в состав гемоглобина – белка, который осуществляет перенос К. в организме теплокровных.

