Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Оксид серы — so2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).
Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 O2 = (t) FeO SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 H2SO4 = (t) K2SO4 H2O SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu H2SO4(конц.) = (t) CuSO4 SO2 H2O
Оксид серы vi — so3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия — Pr, V2O5).
SO2 O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Fe2(SO4)3 = (t) SO3 Fe2O3
Химические свойства
Понятие валентности. связь валентности со строением атома. конспект химия
Валентность — количество химических связей, которые может образовывать атом элемента с другими атомами за счет объединения неспаренных электронов в общую электронную пару (не зря ковалентная связь так названа). Валентность обозначают римской цифрой.
Валентность часто равна количеству неспаренных электронов у атома. Для элементов IV – VII А — групп валентность определить легко, задав вопрос: «Сколько электронов нужно данному элементу до завершения внешнего энергетического уровня?» или по формуле: 8 — № группы (действует только для элементов главных подгрупп IV – VII групп). Но не стоит забывать, что многие элементы в процессе возбуждения могут распаривать электроны, в таком состоянии валентность может достигать номера группы (это характерно для всех элементов, кроме азота, кислорода и фтора). Рассмотрим примеры.
Валентность азота и фосфора
Азот и фосфор, находящиеся в одной группе. Для них по формуле 8 – 5 = 3 мы можем найти низшую валентность (количество неспаренных электронов в основном состоянии), равную трем (III).
В таком случае азот образует аммиак (NH3) и оксид азота III (N2O3), а фосфор – фосфин (PH3) или оксид фосфора III (P2O3).
Но вспомним про возможность образовывать донорно-акцепторные связи некоторыми атомами. И азот, и фосфор имею такую возможность, поэтому кроме трех обычных ковалентных связей, они могут образовать дополнительную донорно-акцепторную. В таком случае, в основном состоянии оба могут иметь валентность IV, что соответствует катиону аммония и катиону фосфония (NH4 и PH4 ). Ковалентные связи обозначают черточкой («‒»).
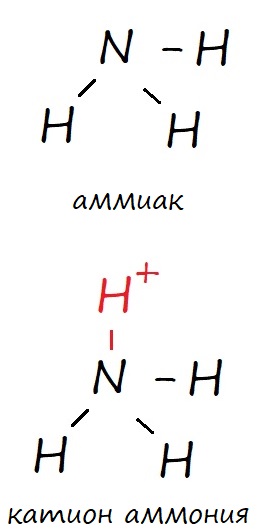
Рис. Образование ковалентных и донорно-акцепторных (выделено красным) связей атомом азота.
У фосфора, в отличие от азота, на внешнем уровне есть незаполненная d-орбиталь, на которую могут переходить электроны при возбуждении.
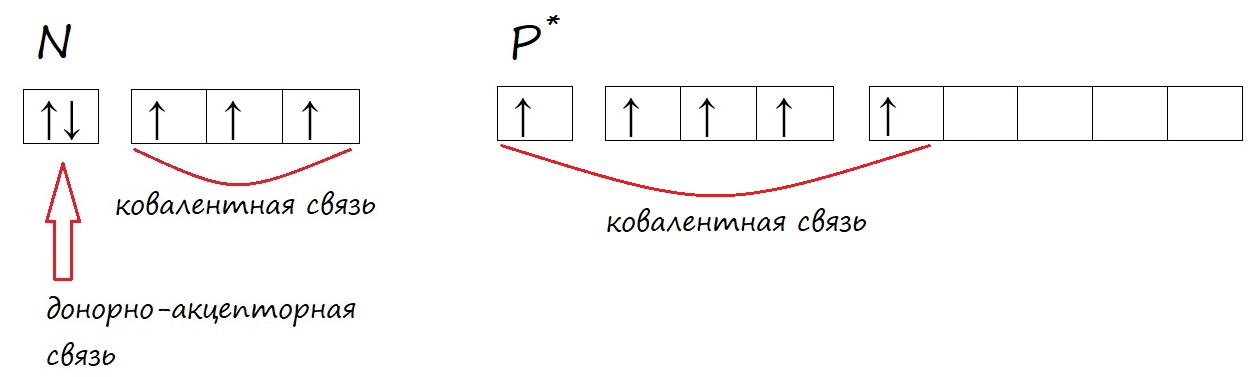
У фосфора в возбужденном состоянии появляется пять неспаренных электронов, поэтому он способен образовывать пять ковалентных связей, соответственно проявлять валентность V, например в ортофосфорной кислоте (H3PO4).
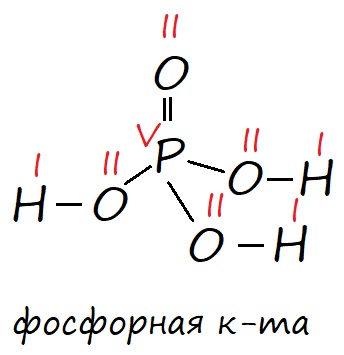
Рис. Строение фосфорной кислоты в соответствии с валентными состояниями атомов: фосфор в возбужденном состоянии имеет пять неспаренных электронов, его валентность равна V; кислород имеет два неспаренных электрона, поэтому его валентность равна II и он может образовывать две ковалентные связи; водород имеет один неспаренных электрон и его валентность равна I. Валентность обозначена красными римскими цифрами.
У азота нет свободной d-орбитали (она появляется с третьего энергетического уровня, а у азота всего два уровня), поэтому распарить электроны не может и высшую валентность, равную номеру группы, проявлять он не способен.
Валентность кислорода и серы
Аналогичную ситуацию можно наблюдать у атомов кислорода и серы. Кислород, находясь во втором периоде может иметь только два энергетических уровня, поэтому d-орбитали, появляющейся с третьего уровня, у него нет. Тогда как у серы три энергетических уровня, на внешнем уровне есть d-орбиталь и возможность распаривать на нее электроны в процессе возбуждения.
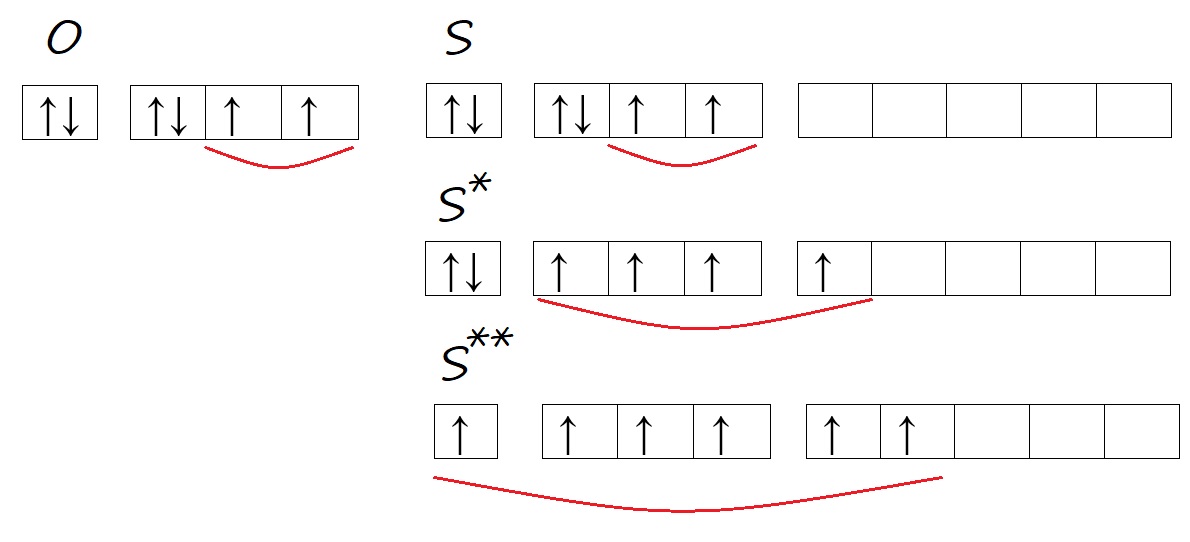
Рис. Количество неспаренных электронов у кислорода и серы в основном и возбужденном состоянии.
Таким образом, кислород способен проявлять валентность II, а сера – валентность II, IV, VI, например, в сероводороде (H2S) валентность равна двум; в сернистом газе и сернистой кислоте (SO2 и H2SO3) валентность равна четырём; в серном ангидриде и серной кислоте (SO3 и H2SO4) – шести.
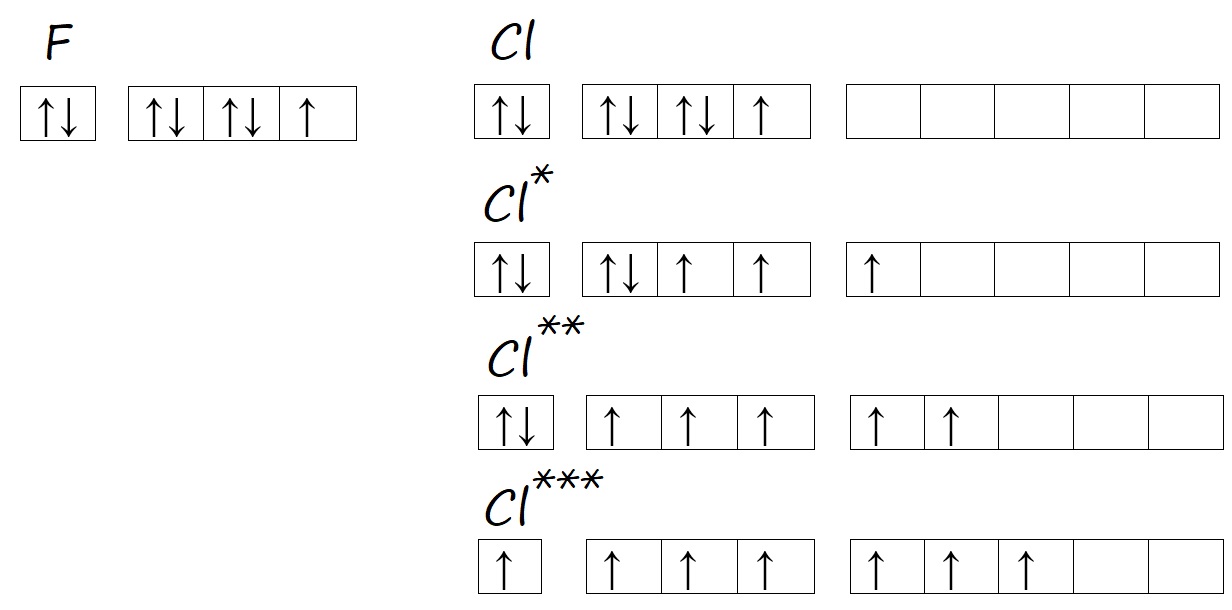
Валентность фтора и хлора
По причинам, описанным выше, фтор так же не способен распаривать свои электроны и переходить в возбужденное состояние, а хлор может. Поэтому у фтора есть одно валентное состояние (I), например, в HF (H ‒ F) и OF2 (F ‒ O ‒ F).
Хлор, как и другие нижестоящие галогены (элементы VIIА-подгруппы), может образовывать несколько возбужденных состояний, поэтому в разных соединениях имеет разную валентность. Например, валентность I хлор проявляет в хлороводороде HCl. Валентность III в хлористой кислоте HClO2. Валентность равную V – в хлорноватой кислоте HClO3. Равную VII – в хлорной кислоте HClO4.
Постоянная и непостоянная валентность
Как уже можно было заметить, некоторые элементы способны проявлять только одну валентность, тогда как другие могут иметь множество валентностей. По этой черте все элементы можно разделить на две группы: элементы с постоянной и непостоянной валентностью.
Таб. Классификация элементов по валентности
С постоянной валентностью | С непостоянной валентностью |
I: H и F II: O | Все остальные неметаллы. |
Иногда валентность определяют и у металлов, хотя для них характерна ионная, а не ковалентная связь, в таком случае таблица будет выглядеть следующим образом:
С постоянной валентностью | С непостоянной валентностью |
I: H, F, все металлы IА-подгруппы (Li, Na…). II: O и все металлы IIА-подгруппы, а также цинк. III: элементы IIIА-подгруппы. | Все остальные неметаллы и металлы. |
Низшая и высшая валентность
Высшая валентность равна номеру группы, в которой находится элемент (исключения: кислород, азот и фтор, как и было описано выше). Так, для брома высшей валентностью будет VII, для теллура – VI, для мышьяка V. Низшая валентность возможна для элементов четвёртой группы, она равна двум. Для элементов V – VII групп она определяется по описанной выше формуле (8 — №группы элемента). Поэтому у брома низшей валентностью будет I, у теллура II, а у мышьяка III.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.
Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S O2 = S H2O (недостаток кислорода)
SO2 C = (t) S CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S H2SO4 = S H2O (здесь может также выделяться SO2)
Химические свойства
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 H2O ⇄ H2SO3
Химические свойства
Сероводород — h2s
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).
Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 H2O = (t) Al(OH)3↓ H2S↑
FeS HCl = FeCl2 H2S↑
Химические свойства
Степень окисления
Степенью окисления (СО) называют условный показатель, который характеризует заряд атома в соединении и его поведение в ОВР (окислительно-восстановительной
реакции). В простых веществах СО всегда равна нулю, в сложных — ее определяют исходя из постоянных степеней окисления у некоторых элементов.
Численно степень окисления равна условному заряду, который можно приписать атому, руководствуясь предположением, что все электроны,
образующие связи, перешли к более электроотрицательному элементу.
Определяя степень окисления, одним элементам мы приписываем условный заряд » «, а другим «-«. Это связано с электроотрицательностью —
способностью атома притягивать к себе электроны. Знак » » означает недостаток электронов, а «-» — их избыток. Повторюсь, СО — условное
понятие.
Сумма всех степеней окисления в молекуле равна нулю — это важно помнить для самопроверки.
Кто более электроотрицательный, тот сильнее притягивает к себе электроны и «уходит в минус». Кто отдает свои электроны и испытывает их недостаток —
получает знак » «.
Самостоятельно определите степени окисления атомов в следующих веществах: RbOH, NaCl, BaO, NaClO3, SO2Cl2,
KMnO4, Li2SO3, O2, NaH2PO4. Ниже вы найдете решение этой задачи.
Сравнивайте значение электроотрицательности по таблице Менделеева, и, конечно, пользуйтесь интуицией 🙂 Однако по мере изучения химии, точное знание
степеней окисления должно заменить даже самую развитую интуицию 😉
Особо хочу выделить тему ионов. Ион — атом, или группа атомов, которые за счет потери или приобретения одного или нескольких
электронов приобрел(и) положительный или отрицательный заряд.
Определяя СО атомов в ионе, не следует стремиться привести общий заряд иона к «0», как в молекуле. Ионы даны в таблице растворимости, они имеют
разные заряды — к такому заряду и нужно в сумме привести ион. Объясню на примере.

