Нафталин
Ароматические углеводороды: Выделение, применение, рынок
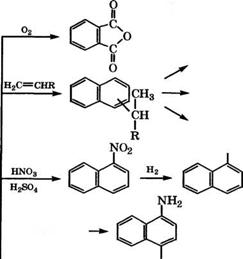
Основные направления применения нафталина представлены на схеме (рис. 16).
Одной из важнейших областей промышленного использования нафталина является окисление до фталевого ангидрида. Окисление нафталина проводится парофазным способом на вана — дий-калийсульфатном катализаторе в стационарном или псевдо — ожиженном слое [1]:
О
II
4-502 — а: > 2С02 2Н20
Н
Выход фталевого ангидрида на этом катализаторе составляет
86- 89 %, производительность по продукту 40 кг/ч на 1 м3 катализатора. Побочными продуктами процесса являются 1,4-наф — тохинон, малеиновый ангидрид, С02.
Модифицирование катализатора позволило повысить его производительность до 50-55 кг/(ч • м3) и выход фталевого ангидрида до 90-94 %. Процесс окисления происходит при массовом соотношении нафталин : воздух = 1 : 35 и температуре 360-370°С. Расход нафталина составляет 1.05-1.1 т на 1 т фталевого ангидрида.
Фирма «Badger» разработала процесс окисления нафталина при более высокой его концентрации (массовом соотношении нафталин : воздух — 1 : 12) в псевдоожиженном слое катализатора.
Парофазным окислением нафталина воздухом при 250-450°С в присутствии катализаторов V205, V205-A1203, Zr02, Si02-W03, B203, фосфатов щелочных металлов получают также 1,4-наф — тохинон [2]. В качестве катализатора возможно использование V205-K2S04, модифицированного оксидами Fe, Sn, Si, Ti, Al.
Теплоносители смазочные масла ПАВ |
![]()
![]()
![]()
![]()
ОН
ОН
![]() Н2о2
Н2о2
ХХУ
(СН3)2НС
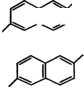
Рис. 16. Направления использования нафталина 278
Сн2=снсн
![]()
![]()
![]()
Три — тетрахлорнафталины, |
ГеС1з СОСНз На28х тиоиндигоидные |
![]()
![]()
![]()
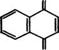
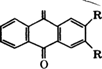
Рис. 16 (продолжение)
При температуре 430-480 °С окисление нафталина происходит с высокой конверсией, что позволяет исключить стадии отделения и рециркуляции сырья [3].
Возможно получение 1,4-нафтохинона окислением 1-нафтола кислородом с выходом 90 % в присутствии каталитического комплекса Со-салкомин в диметилформамиде [2].
1,4- Нафтохинон используется для синтеза антрахинона и его производных, красителей, антибактериальных препаратов и фунгицидов.
Алкилированием нафталина высшими линейными а-олефи — нами, содержащими 12-20 углеродных атомов, получают высшие алкилнафталины. В качестве катализаторов используются макропористые цеолиты типа Y с Н и NH4 обменными центрами [4], те же цеолиты, модифицированные рением [5], твердокислотные катализаторы на основе Zr02, модифицированного (NH4)6H4W1205. Полученные моноалкилнафталины используются в качестве смазочных масел и высокотемпературных теплоносителей с высокой теплопроводностью.
В качестве алкилирующего агента вместо оолефинов могут применяться спирты, алкилгалогениды. Фирма «Mobil Oil Corp.» запатентовала для алкилирования нафталина катализатор МСМ-49 состава Х203 • пУ02, где п < 35, X — трехвалентный элемент (А1, В, Fe, Ga или их смесь), Y — четырехвалентный элемент (Si, Ti, Ge или их смесь) [6].
В 1975 г. разработан высокотемпературный теплоноситель Термолан на основе высших алкилнафталинов, выпускаемый ПО «Оргсинтез» (г. Новомосковск). Это жидкий продукт с температурой плавления -30-ь-45°С, температурой кипения 450-500°С и температурным диапазоном устойчивой работы от -35 до 350°С. Теплоноситель отличается невысокой токсичностью (ПДК = = З0мг/м3), низким давлением насыщенного пара (0.05-0.1 МПа при максимальной температуре использования), сравнительно невысокой вязкостью (60 мм2/с при 20 °С), малой коррозионной активностью, высокой радиационной стойкостью [7, 8].
Алкилнафталины, полученные из нафталина и 1-эйкозена или 1-докозена, применяются в качестве рабочих жидкостей в вакуумных пароструйных насосах и обеспечивают создание ульт — равысокого вакуума (2.8-4.8) ■ 10“7 Па [9]. Вместо индивидуальных а-олефинов для алкилирования нафталина может использоваться фракция С18-С20 крекинг-дистиллята твердого парафина. Алкилирование нафталина проводится в присутствии катализатора BF3-H3P04-S03 при 100 °С в течение 1 ч, выход алкилнафталинов составляет 50-55 %. Полученная вакуумная жидкость, 280
названная Алкарен-1, позволяет создавать в диффузионных насосах вакуум около 10“7 Па [10].
На базе фракции 180-240 °С крекинг-дистиллята, содержащей а-олефины С8-С20, и нафталина получена также вакуумная рабочая жидкость Алкарен-24 [11]. Во избежание олигомеризации а-олефины предварительно гидрохлорировали в присутствии 1 % (мае.) гпС12 на силикагеле. Алкилирование нафталина алкилхлоридами проводилось в присутствии А1С13 при 20-100°С. Вакуумные масла получены также алкилированием дифенила алкилхлоридами С8-С12 (Алкарен Д24) и а-олефинами С12-С14 (Алкарен Д35). Технология получения вакуумных масел Алкарен отработана на опытно-промышленной установке ПО «Химпром» (г. Кемерово). Важное преимущество вакуумных масел на основе нафталина или дифенила и промышленных смесей а-олефинов по сравнению с зарубежными аналогами, полученными с использованием индивидуальных углеводородов, состоит в их значительно меньшей стоимости.
Алкилированием нафталина спиртами, например 2-бутано — лом, и одновременным сульфированием концентрированной Н2804 или слабым олеумом получают алкилнафталинсульфона — ты, применяющиеся в качестве ПАВ [12]. Алкилнафталинсуль — фонаты применяются также в качестве антикоррозионных и моюще-диспергирующих присадок к смазочным маслам [13].
Работы по применению алкилнафталинов, опубликованные до 1990 г., рассмотрены в обзорах [14, 15].
Нитрованием нафталина смесью концентрированных НЖ)3 и Н2в04 при 50-60°С получают 1-нитронафталин. Примеси 2-нитронафталина составляют 4-5 % (мае.) и динитронафталинов — около 3 % (мае.). При дальнейшем нитровании 1-нитронафталина образуется смесь 1,5- и 1,8-динитронафталинов [16].
Гидрированием 1-нитронафталина в присутствии № или Си получают 1-нафтиламин, сульфированием которого производится нафтионовая кислота [17]:
![]()
![]()
№
Перегруппировка гидросульфата 1-нафтиламина проводится в среде о-дихлорбензол а при 175-180 °С.
Сульфирование нафталина концентрированной H2S04 при температуре около 80 °С приводит к образованию 1-нафталин — сульфокислоты, а при температуре свыше 150 °С — к 2-нафта — линсульфокислоте [18].
Фирма «Chemie AG Bitterfeld-Wolfen» запатентовала способ получения нафтионовой кислоты взаимодействием 1 моль
1- нафтиламина и 1-1.2 моль 95-100 %-й H2S04 с образованием нафтиламингидросульфата и последующим его спеканием с
1- 1.3 моль мелкокристаллической амидосульфокислоты при 160-200 °С. Нафтионовую кислоту выделяют нагреванием реакционной смеси с 1 н. НС1 до кипения и очищают через нафтионат натрия с использованием активированного угля. Очищенная нафтионовая кислота пригодна для получения пищевых красителей [19].
Взаимодействием 1-нафтиламина с анилином в жидкой фазе при 230-250 °С в присутствии 12 или /г-толуолсульфокислоты или в паровой фазе при 800 °С над гелем А1203 получают N-фе — нил-1-нафтиламин (неозон А), применяющийся в производстве арилметановых красителей [16].
При нитровании 1-нафталинсульфокислоты получается смесь 5- и 8-нитронафталин-1-сульфокислот, восстановлением которых чугунными стружками получают соответствующие аминопроизводные [17]:
Аналогичным путем из 2-нафталинсульфокислоты получают кислоты Клеве — смесь 5- и 8-аминонафталин-2-сульфокислот. Нафтиламиносульфокислоты применяются в производстве красителей, а также в качестве реагентов для кинофотопромышленности.
При двухстадийном сульфировании нафталина сначала 20%-м олеумом при температуре не выше 35°С, затем 65 %-м олеумом 282
При 55 °С получают нафталин-1,5-дисульфокислоту (кислоту Армстронга) с примесью нафталин-1,6-дисульфокислоты [20].
Щелочным плавлением нафталин-2-сульфокислоты при 300- 315 °С получают 2-нафтол с выходом до 82 % [16, 21]. Возможно получение 2-нафтола гидроксилированием нафталина 28 % — м раствором Н202 сначала при 50 °С, затем при 80 °С в присутствии катализатора — тетракис(декахлор)фталоцианина меди. Конверсия нафталина составляет 22.3 %, селективность образования 2-нафтола — 90 % [22].
Алкилированием нафталина 2-пропанолом в присутствии мор — денита при 250 °С получают 2-изопропилнафталин [23], окислением которого до гидропероксида и кислотным разложением также возможно получение 2-нафтола и ацетона. Максимальный выход 2-нафтола — 61 % достигнут при использовании в качестве катализатора НС104 в растворе уксусной кислоты [24].
При алкилировании нафталина 2-пропанолом на цеолитах Н — У и ЬаН-У образуется в основном 1-изопропилнафталин [23], из которого может быть получен 1-нафтол. В промышленности 1- нафтол производится щелочным плавлением нафталин-1-сульфокислоты с КаОН при 300 °С с выходом около 93 % или гидролизом 1-нафтиламина под действием 20%-й Н2804 при 185- 240 °С [16].
Алкилирование нафталина пропиленом или 2-пропанолом в присутствии нанесенной на морденит Н-типа с мольным соотношением 8Ю2/А1203 свыше 15, при конверсии нафталина 95.2% сопровождается образованием 2,6-диизопропилнафтали — на с селективностью 61.9 % [25]. При алкилировании нафталина на том же морденитовом цеолите с 0.5 % (мае.) Р1 в присутствии добавок воды конверсия повышается до 97.5 % и селективность образования 2,6-диизопропилнафталина — до 67.3 % [26]. Пропитка Н-морденита нитратом церия (при 30 % (мае.) Се) приводит к повышению селективности по тому же изомеру до 70 %
[27] .
Компьютерный поиск оптимального катализатора синтеза
2,6- диизопропилнафталина также подтвердил выбор морденита
[28] .
При каталитическом взаимодействии нафталина с ди — и три — метилнафталинами в присутствии цеолитов протекают одновременно реакции трансметилирования и изомеризации с обогащением реакционной смеси 2,6-диметилнафталином [29, 30].
При алкилировании нафталина метанолом с использованием цеолита Н-гвМ-б происходит образование 2-метилнафталина. Механизм Р-селективного метилирования объясняется тем, что молекулы 1-метилнафталина, имеющие больший объем, не проникают в каналы цеолита [31]. При дальнейшем метилировании 2-метилнафталина на цеолите ZSM-5, особенно при отравлении его внешней поверхности с помощью 2,4-диметилхинолина, селективно образуется 2,6-диметилнафталин [32].
Аналогичные методы могут быть использованы и для получения 2,6-диэтилнафталина. Алкилированием нафталина этиленом или этилгалогенидом в присутствии цеолитов получают преимущественно 2,6-диэтилнафталин, который очищают кристаллизацией [33] или хроматографией на цеолите типа Y, модифицированном ионами Na, К или Ва [34].
Фирма «Nippon Steel Chemical Со.» запатентовала процесс получения 2,6-диэтилнафталина взаимодействием нафталина или 2-этилнафталина с полиэтилбензолами в присутствии цеолита У. Так, при взаимодействии 2-этилнафталина с тетраэтил — бензолами при 80 °С через 2 ч достигнута конверсия 2-этилнафталина 82.7 %, выход диэтилнафталинов 62.3 %, их состав, %:
2,6- 50.1; 2,7- 24.8; 1,6- 15; 1,7- 5.3; прочие изомеры 4.8 [35]. Окислением 2,6-диалкилнафталинов получают 2,6-нафталинди- карбоновую кислоту.
Гидрирование нафталина в присутствии никелевых катализаторов при 150°С приводит к образованию тетралина, а при 200 °С — к смеси цис — и транс-декалинов [16]. Выход декалинов составляет около 95 % при гидрировании тетралина на платино — алюмофосфатном катализаторе, нанесенном на А1203, при температуре процесса 220 °С и давлении 5.17 МПа [36]. Эффективный катализатор гидрирования нафталина до декалинов — 0.1 % (мае.) Ru на смешанных оксидах Mn203-Ni0 [37].
Гидрирование тетралина до цис — и mpawc-декалина проходит с высоким выходом в двухфазной системе, включающей катализатор — димер хлор(1,5-гексадиен)родия и водный буферный раствор с ПАВ. Катализатор сохраняет высокую активность после 8 циклов [38].
Тетралин и декалин рекомендуется использовать вместо 100-200 ароматических растворителей — опасных загрязнителей атмосферы. Они применяются в красках и чернилах, фармацевтических препаратах, в производстве агрохимикатов. Тетралин и декалин выпускает, в частности, американская фирма «Koch Specialty Chemicals» на заводе г. Корпус-Кристи, шт. Техас [39]. В России тетралин производит ОАО «Торжокский завод полиграфических красок» в Тверской области [40].
На основе алкилтетралинов получают среднещелочные сульфонатные присадки к моторным маслам [41].
Жидкофазным хлорированием нафталина в присутствии FeCl3 получают 1-хлорнафталин с примесями 2-хлор-, 1,4- и 1,5-ди — хлорнафталинов. Хлорированием расплавленного нафталина производится также смесь три — и тетрахлорнафталинов — гало — вакс. Галовакс применяется в качестве флегматизатора, заменителя воска и смол при пропитке тканей, изоляции проводов, изготовлении конденсаторов [42].
При ацетилировании нафталина уксусным ангидридом в среде дихлорэтана или хлорбензола получают с выходом 98 %
1- ацетилнафталин, а при проведении реакции в среде нитробензола — 2-ацетилнафталин с выходом около 70 % [16]. 2-Ацетил — нафталин применяется как душистое вещество и фиксатор запаха при составлении отдушек для мыла и парфюмерных композиций.
При взаимодействии 1-ацетилнафталина с полисульфидом натрия получают тиоиндигоидный краситель красно-коричневый Ж [43]:
Тиоиндигоидные красители более стойки, чем индигоидные, к действию окислителей, щелочей и применяются для печати по хлопку, льну, вискозе, для кубового крашения шерсти и меха, как пигменты в полиграфии.
Объем производства полибутилентерефталата в 1987 г. составлял всего 93 тыс. т/год, в том числе, тыс. т/год: США — 34, Япония — 32.5, Западная Европа — 26.5. Однако после кризисного 1993 …
Спрос в мире на полиэтилентерефталат уже в 1995 г. достиг 16.7 млн. т. При среднегодовых темпах роста в 8 % в 1997 г. он равнялся 20 млн. т, а в …
Производства чистой терефталевой кислоты и диметилтереф- талата относятся к наиболее динамично развивающимся в последние 20—25 лет. Так, мировой объем производства терефталевой кислоты и диметилтерефталата в 1976 г. составлял 1599 и …

