- Ангидрид — это что такое ангидрид
- Cпособы получения оксида серы (iv)
- Амидирование
- Гидролиз
- Глутаровый ангидрид
- Как образуются ангидриды?
- Номенклатура
- Окисление сернистого ангидрида до серного
- Оксид серы (vi), ангидрид серной кислоты
- Органические ангидриды
- Получение оксида серы
- Приложений
- Примеров
- Свойства ангидридов
- Химические свойства оксида серы (iv)
- Циклические ангидриды
- Чистый серный ангидрид
- Эстерификация
- Янтарный ангидрид
Ангидрид — это что такое ангидрид
1) Орфографическая запись слова: ангидрид
2) Ударение в слове: ангидр`ид
3) Деление слова на слоги (перенос слова): ангидрид
4) Фонетическая транскрипция слова ангидрид : [нг’др’`ит]
5) Характеристика всех звуков:
аа — гласный, безударный
н[н] — согласный, твердый, звонкий, непарный, сонорный
г[г’] — согласный, мягкий, звонкий, парный
ии — гласный, безударный
д[д] — согласный, твердый, звонкий, парный
р[р’] — согласный, мягкий, звонкий, непарный, сонорный
и[`и] — гласный, ударный
д[т] — согласный, твердый, глухой, парный
8 букв, 5 звук
Cпособы получения оксида серы (iv)
1.Сжигание серы на воздухе:
S O2 → SO2
2.Горение сульфидов и сероводорода:
2H2S 3O2 → 2SO2 2H2O
2CuS 3O2 → 2SO2 2CuO
3. Взаимодействие сульфитов с более сильными кислотами:
Например, сульфит натрия взаимодействует с серной кислотой:
Na2SO3 H2SO4 → Na2SO4 SO2 H2O
4.Обработка концентрированной серной кислотой неактивных металлов.
Например, взаимодействие меди с концентрированной серной кислотой:
Cu 2H2SO4 → CuSO4 SO2 2H2O
Амидирование
Кислотные ангидриды реагируют с аммиаком или с аминами (первичными и вторичными) с образованием амидов. Реакция очень похожа на только что описанную этерификацию, но ROH заменяется амином; например, вторичный амин, R2Нью-Гемпшир.
Опять реакция между (СН3СО)2О и диэтиламин, Et2NH:
(СН3СО)2O 2Et2NH => CH3CoNet2 СН3COO- Нью-Гемпшир2и др2
И диэтилацетамид, CH образуются3CoNet2, и карбоновая аммониевая соль, СН3COO- Нью-Гемпшир2и др2.
Хотя уравнение может показаться немного сложным для понимания, достаточно посмотреть, как группа -COCH3 заменить H эт2NH для образования амида:
и др2NH => Et2NCOCH3
Реакция — это больше, чем амидирование. Все суммировано в этом слове; на этот раз амин страдает ацилированием, а не алкоголем.
Гидролиз
Одной из самых простых реакций ангидридов является их гидролиз, который только что был показан для уксусного ангидрида. В дополнение к этому примеру, у нас есть ангидрид серной кислоты:
H2S2О7 H2О <=> 2H2SW4
Здесь у вас есть ангидрид неорганической кислоты. Обратите внимание, что для H2S2О7 (также называется дисульфуровой кислотой), сама реакция обратима, поэтому нагревание Н2SW4 Концентрат приводит к образованию его ангидрида. Если, с другой стороны, это разбавленный раствор H2SW4, ТАК выпущен3, серный ангидрид.
Глутаровый ангидрид
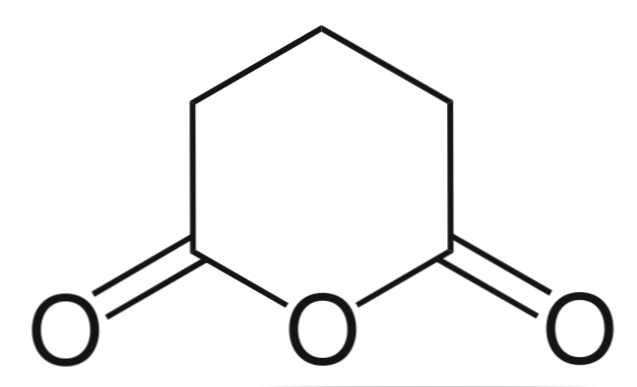
И, наконец, показан ангидрид глутаровой кислоты. Это конструктивно отличается от всех остальных тем, что состоит из гексагонального кольца. Опять же, три атома кислорода выделяются в структуре.
Другие ангидриды, более сложные, всегда могут быть подтверждены тремя атомами кислорода, находящимися очень близко друг к другу..
Как образуются ангидриды?
Неорганические ангидриды образуются путем взаимодействия элемента с кислородом. Таким образом, если элемент является металлическим, образуется основной оксид металла или ангидрид; и если он неметаллический, образуется неметаллический оксид или ангидрид кислоты.
Для органических ангидридов реакция другая. Две карбоновые кислоты не могут связываться напрямую, чтобы высвободить воду и образовать ангидрид кислоты; требуется участие соединения, которое еще не было упомянуто: ацилхлорид, RCOCl.
Карбоновая кислота вступает в реакцию с ацилхлоридом с образованием соответствующего ангидрида и хлористого водорода:
R1COCl R2COOH => (R1CO) O (COR2) HCl
СН3COCl CH3COOH => (CH3СО)2O HCl
A CH3 происходит от ацетильной группы, СН3CO-, а другой уже присутствует в уксусной кислоте. Выбор конкретного ацилхлорида, а также карбоновой кислоты может привести к синтезу ангидрида симметричной или асимметричной кислоты.
Номенклатура
Как называются ангидриды? Оставляя в стороне неорганические вещества, относящиеся к оксидам, названия органических ангидридов, которые до сих пор объяснялись, зависят от идентичности R1 и R2; то есть его ацильных групп.
Если два R одинаковы, достаточно заменить слово «кислота» на «ангидрид» в соответствующем названии карбоновой кислоты. И если, наоборот, два Rs разные, они названы в алфавитном порядке. Поэтому, чтобы узнать, как это назвать, необходимо сначала посмотреть, является ли это симметричным или асимметричным ангидридом кислоты..
(CH3СО)2Или это симметрично, так как R1= R2 = CH3. Производное уксусной или этановой кислоты, поэтому ее название, следуя предыдущему объяснению: ангидрид уксусной или этановой. То же самое касается только что упомянутого фталевого ангидрида.
Предположим, у вас есть следующий ангидрид:
СН3CO (O) COCH2СН2СН2СН2СН2СН3
Ацетильная группа слева происходит от уксусной кислоты, а справа — от гептановой кислоты. Чтобы назвать этот ангидрид, вы должны назвать свои группы R в алфавитном порядке. Итак, его зовут: гептановый уксусный ангидрид.
Окисление сернистого ангидрида до серного
ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ
Физико-химические основы процесса. Процесс окисления сернистого ангидрида до серного протекает по реакции
2S02 02^S03 A^, (45)
Где АН — тепловой эффект реакции.
Процентное отношение количества S02, окисленного до S03, к первоначальному общему количеству S02 называется степенью превращения (или степенью окисления).
Чтобы установить оптимальные условия для процесса окисления S02 на катализаторе в производстве серной кислоты, рассмотрим основные особенности обратимых экзотермических реакций на примере более простой реакции. Обозначим левую часть уравнения (45) буквой А, а продукт реакции буквой R:
A^1R LH. (46)
Общая скорость обратимой реакции равна разности скоростей прямой и обратной реакций, что в рассматриваемом случае можно выразить таким уравнением:
W=wl — w2=klCA — k2CR, (47)
Где w — общая скорость обратимой реакции; W, w2— скорости прямой и обратной реакций; klt k2 — константы
Л
Рис. 49. Зависимость равновесной х* и фактической Хф степени превращения от температуры Т для обратимой экзотермической реакции |
Скорости прямой и обратной реакций; СА, Си — концентрации исходного реагента А в реакционной смеси и продукта реакции R.
Из уравнения (47) следует, что общая скорость обратимой реакции с течением времени уменьшается, так как С а уменьшается, a CR увеличивается. Поэтому через некоторый промежуток времени т наступает равенство kiCA~k2CR, общая скорость реакции становится равной нулю (ш = 0) ив системе наступает равновесие. Достигаемую при этом степень превращения называют равно весной степенью превращения и обозначают х*. Для экзотермической реакции равновесная степень превращения понижается с повышением температуры (рис. 49). Фактическая степень превращения Хф в рассматриваемом случае с повышением температуры вначале увеличивается, достигает некоторого максимального значения, а затем снижается.
Показанная на рис. 49 кривая зависимости Хф от температуры соответствует некоторому времени ті соприкосновения газа с катализатором. Если это время уве
личить до Т2 (t2>Ti), то фактическая степень превращения увеличится и кривая зависимости от Т расположится выше первой кривой (рис. 50). Для тз, когда Тз>Т2, кривая будет еще выше.
Кривую АВ, соединяющую максимумы кривых, называют линией оптимальных температур (ЛОТ). По ней определяют температуру, которую необходимо поддерживать, чтобы обеспечить оптимальные результаты. Про-
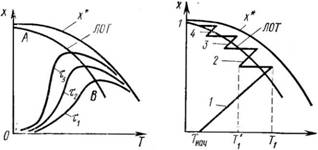
Рис. 50. Зависимость степени превращения х от температуры Т и времени соприкосновения газа с катализатором Т(Т8>Т2>Ті) |
Рис. 51. Изменение температуры Т и степени превращения в 1,2.3 и 4-м слоях катализатора; 7″нач = 7″зажиг |
Цесс следует начинать при максимальной температуре, а затем по мере повышения степени превращения, температуру следует понижать в соответствии с кривой ЛОТ. Таким образом, при проведении обратимой экзотермической реакции не существует одной какой-либо оптимальной температуры, должна соблюдаться оптимальная температурная последовательность — процесс необходимо начинать при высокой температуре, а затем ее понижать.
Приведенные закономерности по отношению к реакции (46) справедливы также и по отношению к реакции (45). Но так как процесс окисления SO2 на ванадиевом катализаторе проводится при высокой температуре, то нагревание газа до этой температуры связано с большими затратами топлива, поэтому на практике поступают так. Нагревают газ до температуры, при которой процесс начинает протекать с достаточной для практических целей скоростью (до температуры Твач> рис. 51), и направ
ляют его на первый слой катализатора. При окислении S02 по реакции (45) выделяется тепло, за счет которого температура газа повышается по прямолинейному закону в соответствии с уравнением
Т=Т0 а{х-х0), (48)
Где Т0, Т — температура в начале и в конце процесса; х0, х — степень превращения в начале и в конце процесса; а — коэффициент.
На первом слое катализатора процесс ведут так, чтобы температура газа на выходе из этого слоя Tt была несколько выше оптимальной, соответствующей ЛОТ (рис. 51). Затем процесс ведут вблизи ЛОТ. Для этого газ направляют в теплообменник, где он охлаждается до температуры Т , несколько более низкой, чем это следует из ЛОТ (см. рис. 51). После этого газ направляют на второй слой катализатора, где он вновь нагревается по прямолинейному закону за счет тепла реакции; затем газ охлаждают и направляют на третий слой катализатора; так поступают до тех пор, пока степень превращения не достигнет заданного значения.
Реакция окисления S02 до S03 идет в присутствии катализатора. Ранее в качестве катализатора при получении контактной серной кислоты применяли платину, теперь она полностью вытеснена ванадиевым катализатором, более дешевым и менее чувствительным к ядам (мышьяк, селен, хлор И др.).
Реакция (45) экзотермична. Тепловой эффект экзотермической реакции зависит от температуры, при которой она протекает:
Теплота Теплота
Температура, реакции[4], Температура, реакции*,
°С ккал/моль » С ккал/моль
25 22,393 500 22,506
100 22,975 550 22,399
200 22,949 600 22,285
300 22,879 650 22,165
400 22,698 700 22,039 450 22,606
Процесс окисления при использовании каждого типа катализатора начинается при определенной температуре (температура зажигания). Например, для платинового катализатора эта температура составляет 250° С, для ванадиевой контактной массы — около 400° С. Изменение температуры влияет на степень превращения (см. рис. 49—51). При этом для каждой температуры есть определенный предел степени превращения. Так как при реакции превращения SO2 в S03 выделяется тепло, понижение температуры приводит к повышению степени превращения.
Состав газа также влияет на реакцию окисления SO2 до S03, а именно: понижение концентрации сернистого ангидрида и увеличение концентрации кислорода повышает степень превращения SO2 в SO3. Состав газа меняется в зависимости от вида сжигаемого сырья и количества подводимого при обжиге воздуха.
Все перечисленные факторы (давление, температура, состав газа, тип катализатора) определяют скорость реакции превращения сернистого ангидрида в серный. От скорости реакции окисления зависит требуемый объем катализатора, а следовательно, и объем контактного аппарата. Чтобы процесс был экономичным, его стремятся вести при наибольшей скорости реакции.
Ванадиевая контактная масса. Она представляет собой пористое вещество, на которое нанесено активное комплексное соединение, содержащее пятиокись ванадия V205. Контактную массу формуют, придавая ей вид гранул, таблеток и т. д. (рис. 52).
В производстве контактной серной кислоты применяют в основном два вида катализатора: БАВ и СВД. Они получили такие названия по начальным буквам названий компонентов, входящих в их состав (барий, алюминий, ванадий и сульфованадат на диатомите).
Примерный состав контактной массы БАВ: V2Os — 12Si02-0,5Al203*2K20 • ЗВаО-2КС1. Перед вводом массы в эксплуатацию ее сушат горячим воздухом, а затем при 420—440° С насыщают сернистым ангидридом, вводя воздух с низкой концентрацией S02 (0,3—0,5%). При более высокой концентрации S02 неизбежен перегрев и, как следствие его, спекание массы. Насыщение проводится в промышленном контактном аппарате. При насыщении в газовую фазу выделяется хлор, а цвет массы меняется от белого (иногда розоватого) до желтого.
В сухой контактной массе содержится 7,5—8% ванадия (в пересчете на V2O5), насыпная плотность насыщенного катализатора составляет 600—700 г/л (свежего 500—550 г/л).
Примерный состав катализатор» СВД (сульфована- дат на диатомите): V205-3K20-6S03-35Si02. Масса СВД
Обладает высокой механической прочностью и в несколько раз дешевле массы БАВ. Гранулы СВД имеют светло-коричневый цвет, насыпная плотность 570—600 г/л, температура зажигания некоторых видов массы СВД несколько ниже температуры зажигания массы БАВ.
Для контактной массы СВД не требуется предварительного насыщения сернистым газом. Активность ее несколько ниже активности массы БАВ, поэтому следует загружать катализатора СВД в контактный аппарат больше, чем катализатора БАВ.
Средний диаметр гранул катализатора БАВ 5 мм, длина 7—15 мм. Кольцеобразную контактную массу БАВ готовят двух размеров (в мм): rfH= 10, с? вн=3, /г = 10 и dH=8, dBн=2,5, h=8 (dw dBn— наружный и внутренний диаметры колец, h — высота колец).
Средний диаметр гранул контактной массы СВД 4— 4,5 мм, длина гранул 10—15 мм; кольцеобразную массу готовят двух размеров (в мм): d„=8 и 12, dBн=3 и 6, ft = 8 и 12. Кольцеобразной массы загружают на 30% больше, чем гранулированной.
При температуре выше 620° С активность ванадиевой контактной массы быстро понижается. Предполагают, что при этом распадается активный комплекс, содержащий V2O5. Повышение температуры может привести к снижению активности катализатора также вследствие разрушения структуры массы и происходящего при этом уменьшения поверхности катализатора.
В настоящее время разработаны термически стойкие контактные массы (нагревание до 650—670° С не вызывает значительного уменьшения активности), а также катализаторы с низкой температурой зажигания, повышенной механической прочностью, для высокой концентрации S02 и др. Их марки: СВИТ, СВС, ИК-4, ИК-2, (КС) и др.
Температура зажигания контактной массы зависит не только от качества катализатора, но и от состава газовой смеси. С уменьшением кислорода в газе она повышается; так, при содержании в газе 7% S02 и 11% 02 температура зажигания массы БАВ 423° С. Уменьшение в этом же газе содержания кислорода до 6,7% повышает температуру зажигания до 437° С.
При эксплуатации активность контактной массы постепенно снижается, поэтому катализатор меняют через каждые 3—5 лет. При строгом соблюдении правил эксплуатации (например, поддержание постоянного температурного режима в аппарате, продувка его перед остановкой горячим сухим воздухом и т. д.) этот срок значительно увеличивается.
Сопротивление контактной массы составляет около половины гидравлического сопротивления всего контактного отделения. На сопротивление слоя контактной массы влияют размеры гранул и форма массы: укрупнение гранул способствует снижению сопротивления. Использование массы в виде крупных колец еще более снижает сопротивление слоя.
Наиболее сильным ядом для ванадиевой контактной массы является мышьяк (хотя ванадиевая масса в 5000 раз менее чувствительна к действию мышьяка, чем платиновая). Мышьяк поглощается контактной массой и накапливается в ней в виде AS2O5. При температуре ниже 550° С активность контактной массы вследствие отравления мышьяком понижается. При температуре выше
550° С образуется летучее соединение V205-As205, с которым теряется ванадий из первого слоя контактной массы, осаждаясь в виде корки на последующих слоях.
Соединения фтора HF и SiF4 также являются сильным ядом для ванадиевой контактной массы и значительно понижают ее активность.
Пары воды при температуре, превышающей температуру конденсации паров серной кислоты, не оказывают заметного влияния на ванадиевую контактную массу, что подтверждается многолетним опытом эксплуатации заводов мокрого катализа. При низкой температуре влага разрушает контактную массу.
Присутствие в газе С02, СО, H2S, CS2, NH3, NO, паров S, Se и других веществ при нормальном режиме работы контактного аппарата заметного понижения активности контактной массы не вызывает.
Сульфат железа, который может образоваться в результате коррозии аппаратуры, в верхних слоях контактной массы образует корки, мешающие нормальной работе катализатора.
Условия окисления S02 до S03 на ванадиевом катализаторе. Каждой степени окисления соответствует определенная температура, при которой наблюдается наивысшая скорость реакции окисления S02 до SO3 (оптимальная температура) (см. рис. 50). Однако скорость реакции зависит также от состава газа и поэтому при различном составе газовой смеси оптимальные температуры для одной и той же степени окисления различны. Таким образом, постоянной оптимальной температуры для процесса окисления сернистого ангидрида не существует.
На практике окисление проводят в несколько стадий (см. рис. 51). Газ нагревают примерно до температуры зажигания контактной массы (440° С) и направляют в первый слой контактной массы. Здесь в процессе окисления выделяется большое количество тепла, и температура газа сильно возрастает. Процесс ведется без отвода тепла (адиабатически) до достижения оптимальной температуры, а затем тепло отводят так, чтобы температура дальнейшего процесса окисления была возможно ближе к оптимальной. Таким образом, в первом слое катализатора температура возрастает от 440 примерно до 600° С. Степень превращения при этом составляет около 70%. В этих условиях скорость реакции наибольшая. Для Дальнейшего Окислення с максимальной скоростью не прореагировавшего S02 температуру газа следует понизить. Этого достигают отводом тепла в теплообменнике, расположенном между первым и вторым слоями катализатора. Температура здесь снижается от 600 до 525° С. Во втором слое, катализатора процесс снова идет без отвода тепла (адиабатически), и температура повышается за счет теплового эффекта реакции до 550° С. Степень окисления после второго слоя составляет уже 80%. Затем снова охлаждают газ между слоями до 500° С и т. д.
В каждом последующем слое общая степень окисления повышается.
Повышение температуры при адиабатическом процессе окисления S02 до SO3 приведено ниже:
Концентрация SO,) в газовой смеси, %
2 4 6 7
Повышение температуры при увеличении степени окисления иа 1%, «С
0,59 1,17 1,73 2,0 2,27 2,54
Концентрация SOs в газовой смеси, %
10
12 14 20
62,5
Повышение температуры при увеличении степени окисления иа 1%, °С
2,81 3,29 3,78 5,1 12,5
Пользуясь этими данными, можно рассчитать степень окисления в слое при определенном количестве выделившегося тепла, и наоборот, если исходить из определенной степени окисления, можно подсчитать, сколько тепла необходимо при этом отвести.
При окислении газ должен соприкасаться с контактной массой определенное время, только тогда можно получить заданную степень окисления. Время соприкосновения должно быть достаточным для получения желаемой степени окисления и в то же время минимальным. Иначе придется увеличивать количество контактной массы, что приведет к увеличению размеров аппарата и повышению капитальных затрат.
Количество контактной массы определяют из уравнения
V = Vx, (49)
Где w — объем контактной массы, м3; V — объем газа, приведенного к нормальным условиям, м3/с; т — время соприкосновения, с.
Время соприкосновения находят по определенным формулам в зависимости от состава газа, температурных условий, заданной степени превращения.
Для того чтобы учесть снижение активности катализатора во времени, обычно при расчетах количества контактной массы вводят коэффициенты запаса массы. Значения их принимают на основе практических данных.
Оптимальные условия работы контактного аппарата выбирают с учетом многих факторов. Всегда желательна высокая степень окисления. При этом в выхлопных газах содержится меньше SO2 (так, при степени превращения 99,5% в отходящих газах содержится 0,04% SO2, такие газы можно выбрасывать в атмосферу без дополнительной очистки). Однако с увеличением степени превращения (особенно выше 98%) сильно увеличивается необходимое количество контактной массы, так как процесс приближается к равновесию, когда скорость его снижается. Поэтому обычно ограничиваются степенью превращения около 98%, при этом достигается наиболее низкая себестоимость серной кислоты.
Большое значение в определении оптимального режима имеет гидравлическое сопротивление аппарата. С одной стороны, оно увеличивается с повышением концентрации S02, так как при этом необходимо повысить объем контактной массы, а с другой — уменьшается в результате уменьшения общего объема газа ( с повышением концентрации S02 общий объем газа уменьшается). Таким образом, очень важен правильный выбор концентрации S02. При этом следует учитывать, что повышение концентрации газа вызывает перегрев контактной массы. В связи с этим перспективны исследования по получению термостойкой контактной массы.
Двойное контактирование. Для достижения высокой степени окисления и уменьшения содержания сернистого ангидрида в отходящих газах без значительного увеличения количества контактной массы применяют так называемое двойное контактирование (или контактирование с промежуточной абсорбцией) — ДК/ДА.
Сущность двойного контактирования состоит в том, что процесс окисления S02 на катализаторе проходит в два этапа. На первом степень превращения составляет около 90%. Затем из газа выделяют серный ангидрид, направляя газ в дополнительный, промежуточный абсорбер. В результате в газе увеличивается соотношение
Ог : SO2, что позволяет на втором этапе увеличить степень превращения оставшегося сернистого ангидрида до 95—97%- Общая степень превращения достигает 99,5— 99,7%, а содержание SO2 в отходящих газах составляет около 0,03% (при одинарном контактировании — десятые доли процента).
При двойном контактировании сернистый газ дважды нагревается от начальной температуры около 50° С (после осушки в сушильной башне и выделения серного
Ангидрида в первой стадии абсорбции), поэтому для обеспечения автотермичности процесса концентрация SO2 в газе на входе в первую стадию контактирования должна поддерживаться 9—10%-
Схема контактного отделения с двойным контактированием изображена на рис. 53. Газ проходит теплообменники 1 и 2 и поступает на первый, а затем на второй и третий слои контактной массы аппарата 3. После третьего слоя газ подают в промежуточный абсорбер 6, из него в теплообменники 4 и 8, а затем в четвертый слой контактной массы. Охлажденный в теплообменнике 4 газ проходит абсорбер 7 и из него выводится в атмосферу. В случае возможных нарушений режима абсорбции очистка газа от сернокислотного тумана и брызг производится в волокнистом фильтре 5.
Окисление S02 на катализаторе в кипящем слое. Увеличение поверхности соприкосновения газа с катализатором при интенсивном перемешивании увеличивает ско*
рость процесса окисления SO2 до S03. При этом, как вытекает из экспериментальных исследований, расход катализатора снижается в два раза.
Интенсивность перемешивания увеличивает скорость процесса, позволяет полнее использовать поверхность контактной массы, значительно улучшает теплопередачу (а следовательно, и отвод тепла). Поэтому в аппаратах с кипящим слоем не только уменьшается объем катализатора, но газ может подаваться в аппарат с температурой ниже температуры зажигания и концентрация его может быть выше обычной (7—7,5%). Перечисленные преимущества делают процесс окисления в кипящем слое весьма перспективным.
Гидравлическое сопротивление кипящего слоя не зависит от размера зерен, поэтому для каталитического окисления SO2 в кипящем слое применяют очень мелкие сферические гранулы катализатора (радиус 0,5—2 мм), что обеспечивает практически полное использование внутренней его поверхности. Интенсивность процесса в кипящем слое повышается также вследствие постоянства температуры во всем слое.
Присутствие некоторого количества пыли в газе, поступающем в кипящий слой катализатора, не вызывает затруднений, так как вследствие большой скорости газа и интенсивного перемешивания пыль в кипящем слое не задерживается.
Заменять отработанный и загружать свежий катализатор в кипящий слой можно без остановки процесса, что важно при работе по упрощенным технологическим схемам, допускающим присутствие в газе контактных ядов.
Достоинства процесса окисления S02 в кипящем слое обусловили большой интерес к нему. На основании лабораторных исследований проведены полузаводские и опытно-промышленные испытания этого процесса и запроектированы промышленные установки с кипящим слоем катализатора.
Контактное отделение современного сернокислотного завода. Контактное отделение любой сернокислотной системы оборудуется подогревателем, контактными аппаратами и теплообменниками.
В период пуска системы, когда тепло реакции окисления SO2 до S03 еще не начало выделяться, газ нагревают до температуры зажигания в подогревателе. При вы
ходе контактного узла на обычный режим работы подогреватель отключают.
Разогрев контактного аппарата во время пуска (как и продувка контактной массы перед остановкой контактного аппарата) проводится сухим атмосферным воздухом, предварительно пропускаемым через сушильную башню. С этой целью на крупных системах устанавли-
Рис. 54. Контактные аппараты с промежуточным охлаждением газа между слоями контактной массы: а — охлаждение в теплообменниках, б — охлаждение введением холодного воздуха; 1 — слой контактной массы. 2 — теплообменники для охлаждения газа
Вают специальную небольшую сушильную башню и пусковой вентилятор. Разогрев и продувку аппарата можно проводить и влажным атмосферным воздухом. Однако при этом необходимо следить за тем, чтобы S03 из катализатора удалялся при высокой температуре (для предотвращения конденсации паров H2SO4).
Окисление S02 до S03 проводится в контактных аппаратах с промежуточным или внутренним теплообменом. В аппаратах с промежуточным теплообменом газ после каждого слоя катализатора охлаждается в теплообменнике (рис. 54, а), котле-утилизаторе или поддувом холодного газа (рис. 54, б). В аппарате с внутренним теплообменом газ из первого слоя поступает во второй, в котором расположены теплообменные трубы с циркулирующим в них более холодным газом.
Контактные аппараты с промежуточным теплообменом просты, удобны в регулировании и дают возможность использовать тепло реакции, поэтому их в последние годы применяют все чаще. Число слоев в этих аппаратах может быть от трех до пяти.
В контактном аппарате с кипящим слоем (рис. 55) холодильные элементы (змеевики) размещены в самом слое массы. Охлаждение проводится холодной водой или другим хладагентом.
При эксплуатации контактного отделения различают два периода его работы: 1) пусковой, когда тепло реакции еще не выделяется и газ нагревается в подогревателе за счет использования топлива или электроэнергии, 2) период нормальной работы, когда газ нагревается в теплообменниках вследствие выделения тепла реакции (подогреватель не работает). Для каждого из этих периодов существуют определенные схемы включения аппаратов: пусковая и рабочая.
Все аппараты контактного отделения соединены между собой стальными трубами (толщина стенок 4—5 мм) со стальными задвижками, при помощи которых регулируют расход газа и направление газовых потоков. Для лучшего сохранения тепла, выделяющегося при окислении, вся аппаратура контактного отделения покрыта слоем теплоизоляции (толщина слоя 150—250 мм).
Аппаратура контактного отделения. Контактные аппараты. Аппарат, приведенный на рис. 56, широко применяют в отечественной промышленности; его производительность 540 т/сут серной кислоты. Для охлаждения газа после первого слоя добавляют холодный сернистый газ.
Аппарат состоит из стального цилиндрического корпуса, в центре которого расположена опорная стойка, собранная из чугунных труб. Внутренний диаметр аппарата 8,5 м, общая высота 19,6 м. Контактная масса размещена на решетках, укрепленных в стенках аппарата и на опорной трубе. Газ после второго, третьего и четвертого слоев контактной массы охлаждается в промежуточных теплообменниках, вмонтированных в контактный аппарат. Теплообменные трубы расположены горизонтально и могут быть очищены и отремонтированы без выгрузки контактной массы.
При сжигании колчедана в печах КС получают высококонцентрированный обжиговый газ. В этом случае на
/—V _ слои контактной массы; 1—3 — промежуточные теплообменники. 4 — смесители, 5 — слои кварца (15—20 мм)
Первом слое контактной массы иногда окисляют газ с повышенной концентрацией S02 (10—12%), а перед вторым слоем снижают содержание S02 в газе и повышают концентрацию кислорода, добавляя атмосферный воздух (рис. 57). Одновременно с уменьшением концентрации S02 понижается температура газа, что исключает необходимость в теплообменнике после первого слоя контактной массы.
Расположение промежуточных теплообменников внутри контактного аппарата (см. рис. 54, а) значительно осложняет его конструкцию, поэтому в последние годы в высокопроизводительных контактных системах предусматриваются преимущественно контактные аппараты с выносными теплообменниками (см. рис. 57 и 58). Кроме простоты и надежной работы достоинство таких аппаратов еше и в том, что в них легко создаются оптимальные условия для осуществления процесса окисления сернистого ангидрида на катализаторе, а в выносных теплообменниках — оптимальные условия для процесса теплопередачи. Нецелесообразность совмещения этих процессов в одном аппарате проявляется особенно от
четливо с повышением производительности контактных аппаратов. Кроме того, в аппаратах с выносными теплообменниками газ после каждого слоя хорошо перемешивается по пути следования к теплообменникам и внутри них, что имеет большое значение для достижения высокой степени превращения.
Контактный аппарат с выносными теплообменниками производите льностью 1000 т/сут H2SO4 показан на рис. 58. Его диаметр 12 м, общая высота 22 м.
В контактном аппарате с кипящими слоями контактной массы (рис. 59) газ последовательно проходит снизу вверх через слои контактной массы, расположенные на газораспределительных решетках 2. Избыточное реакционное тепло отводится при помощи теплообмениых элементов 3. Верхняя часть аппарата расширена и снабжена отбойником 5 для уменьшения уноса Из слоя катализатора.
Газораспределительные решетки представляют собой колпачковые решетки, доля живого сечения в которых составляет 6%; на них расположена ванадиевая контактная масса с зернами размером 0,75—1 мм. Температура газа на входе в аппарат 300—350° С, гидравлическое сопротивление 800—900 мм вод. ст., общая степень превращения 95—98%. Потери контактной массы вследствие ее истирания в процессе интенсивного перемешивания в кипящем слое составляют 10% за 1 год (установлено на основании пятилетного опыта работы промышленного аппарата).
Рис. 59. Контактный аппарат с кипящими слоями контактной массы: |
1 — трубные решетки, 2 — перегородки, 3 — компенсатор, 4 — лазы, 5 — отверстие для слива кислоты |
IV — слон контактной массы; / — выравнивающие решетки. 2— газораспределительные решетки, 3 — теплообменные элементы, 4 — люки, 5 — отбойник |
Лодного газа или воздуха, добавляемых для понижения температуры газовой смеси после выхода из слоев контактной массы, и т. д. Обширные исследования в области усовершенствования конструкций контактных аппаратов непрерывно проводятся во многих странах, поскольку процесс окисления S02 до S03 — наиболее важная стадия контактного процесса. Аппаратурное оформление и технологический режим контактного отделения определя- |
С начала разработки контактного способа производства серной кислоты сконструировано большое число разнообразных контактных аппаратов. Они отличаются конструкцией, расположением полок с контактной массой, устройством теплообменников и их размещением, приспособлениями для распределения газа по сечению контактного аппарата, устройствами для смешивания хо — ются коэффициентом использования сырья (зависит от степени превращения), расходом электроэнергии (зависит от гидравлического сопротивления контактного аппарата) и другими технико-экономическими показателями сернокислотных систем.
Теплообменник — это стальной вертикальный цилиндр с верхней и нижней решетками 1 (рис. 60), в которые ввальцованы цельнотянутые стальные трубы. Внутри корпуса для более равномерного распределения газа по сечению межтрубного пространства и увеличения коэффициента теплопередачи горизонтально расположены перегородки 2 или решетки. Горячий газ (S03) из контактного аппарата проходит по трубам теплообменника сверху вниз противотоком сернистому газу, поступающему снизу в межтрубное пространство (или наоборот).
Если обжиговый газ, поступающий в контактное отделение, содержит туман серной кислоты, то он частично осаждается в межтрубном пространстве теплообменника, из-за чего стенки труб быстро разрушаются. Продукты коррозии понижают коэффициент теплопередачи. При высокой влажности газа, поступающего на контактирование, внутренняя поверхность труб также подвергается коррозии. Конденсата кислоты образуется тем больше, чем больше влажность газа и ниже температура стенки. Если влажность не превышает 0,01 %, конденсат кислоты в теплообменнике практически не образуется.
В теплообменнике газ охлаждается до 200° С; для того чтобы его можно было передать на абсорбцию, его дополнительно охлаждают в ангидридном холодильнике.
Ангидридный холодильник по своей конструкции принципиально не отличается от теплообменников. Обычно по трубам сверху вниз движется газ, поступающий из контактного отделения, в межтрубном пространстве — охлаждающий воздух или вода.
В ангидридном холодильнике с воздушным охлаждением газ поступает в приемную камеру / (рис. 61), опускается по трубам 2 вниз и выходит через штуцер 5 из нижней камеры 4. Атмосферный воздух, нагнетаемый вентилятором 3, проходит межтрубное пространство и выходит через кольцевое отверстие 6 возле верхней трубной решетки. Горячую воду (или воздух) из ангидридного холодильника используют для отопления помещений или для других целей.
І і I н -<и I я IIГЛ His Яз * 5 g и0 5 о В яё» ЈSS3| Sg«8s її t — о.» В ° e-cr Si 1 — ь ч a |
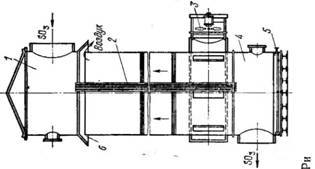
Подогреватель наиболее распространенного типа показан на рис. 62. Топка 4 сложена из огнеупорного кирпича и представляет собой прямоугольную камеру, в которую через отверстие 3 форсункой вдувается жидкое топливо или газ. Продукты горения смешиваются с воздухом, засасываемым через окна 2 и 5, и при 650—700° С поступают в шахту 1. Отсюда топочные газы через чугунную или стальную футерованную трубу 6 направляются в стальную приемную камеру 7 подогревателя, перекрытую чугунной крышкой 8 и футерованную огнеупорным кирпичом.
Теплообменник (подогреватель) 11— стальной цилиндр с верхней и нижней решетками, в которые вваль — цованы трубки; он установлен на кирпичном фундаменте. Иногда над верхней решеткой находится куполообразный свод 9 с отверстиями 80×80 мм, предназначенный для равномерного распределения газа по сечению подогревателя. Топочные газы проходят подогреватель сверху вниз, отдавая тепло сернистому газу, идущему противотоком в межтрубном пространстве, охлаждаются до 300—350° С и выходят в дымовую трубу. Сернистый газ при 50—60° С поступает снизу в межтрубное пространство подогревателя и, проходя снизу вверх противотоком топочным газам, движущимся по трубам, нагревается до 450—500° С.
Описанный подогреватель имеет малые размеры, быстро вводится в рабочий режим, процесс легко регулируется и т. д. Однако такой подогреватель может быть рекомендован только для непродолжительной работы, иначе в верхней трубной решетке под действием горячих топочных газов образуются трещины, через которые происходит утечка газа. Если по недосмотру топочные газы поступят в камеру 7 при чрезмерно высокой температуре, верхняя трубная решетка может перегореть, и подогреватель выйдет из строя.
При контактировании газа с низким содержанием S02 требуется постоянный подогрев. В этих случаях устанавливают подогреватели с чугунными трубами U-образной формы. Они помещаются в кирпичной камере, куда поступают горячие газы из топки подогревателя.
На некоторых заводах контактные аппараты разогреваются топочными газами, образующимися при сжигании газового топлива. Продукты его сгорания не оказывают вредного действия на контактную массу, если температура топочных газов достаточно высокая и обеспечена полнота сжигания топлива; для этого в топке необходимо автоматически поддерживать температуру 1100—1200° С. По выходе из топки газы разбавляют воздухом для снижения их температуры перед подачей в контактный аппарат.
На отдельных заводах применяют простые и дешевые электрические подогреватели, имеющие малые размеры; эти приборы быстро приводятся в рабочее состояние и легко регулируются. Несмотря на большой расход электроэнергии установка электрического подогревателя иногда экономически целесообразна, так как подогреватель на контактных заводах включается очень редко, обычно во время пуска, когда часть электрооборудования отключена или работает с недостаточной нагрузкой и в цехе есть резерв электрической мощности.
Технологический режим окисления S02 до S03. Показателем работы контактного отделения служит степень окисления и возможность па боты без подогревателя (ав — тотермичность процесса). Степень окисления определяется температурным режимом аппарата, который зависит от количества и концентрации поступающего газа. Чем выше концентрация S02, тем больше тепла выделяется при реакции окисления S02 до S03. Концентрация S02 должна быть постоянной, иначе температура в контактном аппарате будет неустойчивой, и режим работы нарушится.. Обычно концентрацию S02 поддерживают на уровне 7—7,5%. Тепло реакции расходуется в основном на нагревание поступающего газа.
Концентрацию газа и его температуру измеряют каждый час. Особенно тщательно следят за температурой на входе в первый слой, так как понижение ее может вызвать прекращен ие процесса окисления в первом слое контактной массы и нарушение баланса тепла в системе, что в конечном счете выведет контактный аппарат из строя.
На рис. 56 была показана схема контактного аппарата с вводом холодного газа после первого слоя и промежуточными теплообменниками после остальных слоев. Ниже приводятся данные об оптимальном режиме такого аппарата при концентрации в поступающем в него газе: S02 — 7%, 02—11,3% и температуре добавляемого газа 237° С (римскими цифрами обозначены слои катализатора) :
Температура газа, °С:
TOC o «1-3» h z на входе………………… 440
На выходе………………… 571
Степень окисления, % . . 0,655
Количество контактной лоты составляет около 300
II | Ill | IV | V |
476 | 460 | 437 | 431 |
548 | 482 | 444 | 433 |
0,827 | 0,938 | 0,973 | 0,980 |
Общие сведения. Для обжига колчедана существуют печи различных конструкций: механические полочные (многоподовые), вращающиеся цилиндрические, печи пылевидного обжига, печи для обжига в кипящем слое. В механических полочных печах обжиг колчедана ведут …
Амелин А. Г., Яшке Е. В. Как уже упоминалось, основная часть серной кислоты потребляется для изготовления удобрений. Для питания растений особенно нужны фосфор и азот. Природные фосфорные соединения (апатиты и …
Оксид серы (vi), ангидрид серной кислоты
Оксид серы (VI) – это кислотный оксид. При обычных условиях – бесцветная ядовитая жидкость. На воздухе «дымит», сильно поглощает влагу.
Способы получения. Оксид серы (VI) получают каталитическим окислением оксида серы (IV) кислородом.
2SO2 O2 ↔ 2SO3
Сернистый газ окисляют и другие окислители, например, озон или оксид азота (IV):
SO2 O3 → SO3 O2
SO2 NO2 → SO3 NO
Еще один способ получения оксида серы (VI) – разложение сульфата железа (III):
Fe2(SO4)3 → Fe2O3 3SO3
Органические ангидриды
Кислотные ангидриды реагируют путем ацилирования либо со спиртом, образуя сложный эфир, с амином, образуя амид или ароматическое кольцо.
Существуют миллионы каждого из этих соединений и сотни тысяч вариантов карбоновых кислот для приготовления ангидрида; следовательно, синтетические возможности резко возрастают.
Таким образом, одним из основных применений является включение ацильной группы в соединение, замещающее один из атомов или групп его структуры..
Каждый ангидрид в отдельности имеет свои приложения, но в общих чертах они все реагируют одинаково. По этой причине эти типы соединений используются для модификации полимерных структур, создания новых полимеров; то есть сополимеры, смолы, покрытия и т. д..
Например, уксусный ангидрид используется для ацетилирования всех ОН групп целлюлозы (нижнее изображение). При этом каждый Н ОН заменяется ацетильной группой COCH3.
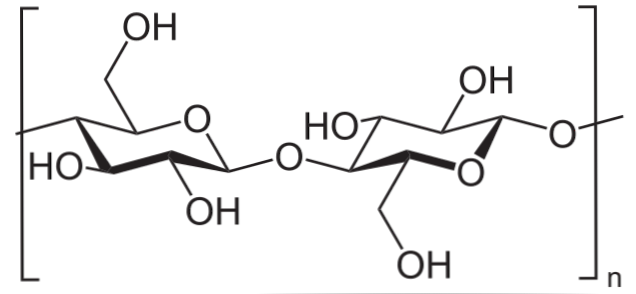
Таким способом получают полимер ацетата целлюлозы. Та же самая реакция может быть нарисована с другими полимерными структурами с группами NH2, также подвержен ацилированию.
Эти реакции ацилирования также полезны для синтеза лекарств, таких как аспирин (кислота ацетилсалициловая).
Получение оксида серы

Для получения небольшого количества серного ангидрида в лаборатории можно воспользоваться прибором, изображенным на рис.. Через трехгорлую склянку 1 с концентрированной серной кислотой пропускают для осушения кислород и сернистый газ.
Из склянки смесь обоих газов поступает в трубку 2,содержащую платинированный асбест (асбест с нанесенной на него мелко раздробленной платиной); трубка нагревается горелкой. Здесь происходит соединение кислорода с сернистым газом:
2SO2 O2 ⇄ 2SO3
Пары образующегося серного ангидрида вместе с избытком газов переходят в охлаждаемую льдом колбу 3. В колбе часть серного ангидрида сгущается, а не успевшие сгуститься пары попадают в склянку 4, где, соединяясь с водой, дают серную кислоту.
Приложений
Неорганические ангидриды имеют бесконечное количество применений, от синтеза и составления материалов, керамики, катализаторов, цементов, электродов, удобрений и т. Д. До покрытия земной коры тысячами минералов железа и алюминия и диоксида. углерода, выдыхаемого живыми организмами.
Они представляют собой источник отправления, точку, откуда происходит множество соединений, используемых в неорганическом синтезе. Одним из наиболее важных ангидридов является углекислый газ, СО2. Вместе с водой он необходим для фотосинтеза.
Возможно, ангидрид с большим количеством применений и имеющий (пока есть жизнь) является одним из фосфорной кислоты: трифосфат аденозина, более известный как АТФ, присутствующий в ДНК и «энергетическая валюта» метаболизма.
Примеров
Некоторые другие примеры органических ангидридов приведены к концу. Хотя о них не будет упоминаться, атомы кислорода могут быть заменены серой, давая серу или даже ангидриды фосфора.
-С6H5CO (O) COC6H5: бензойный ангидрид. Группа С6H5 представляет бензольное кольцо. Его гидролиз производит две бензойные кислоты.
-HCO (O) COH: муравьиный ангидрид. Его гидролиз производит две муравьиной кислоты.
— С6H5CO (O) COCH2СН3: бензойный пропановый ангидрид. Его гидролиз производит бензойную и пропановую кислоты.
-С6H11CO (O) COC6H11: циклогексанкарбоновый ангидрид. В отличие от ароматических колец, они насыщенные, без двойных связей.
-СН3СН2СН2CO (O) COCH2СН3: бутановый пропановый ангидрид.
Свойства ангидридов
Свойства ангидридов будут зависеть от того, на что вы ссылаетесь. Почти все имеют общее, что они реагируют с водой. Однако для так называемых основных ангидридов в неорганических, фактически некоторые из них даже нерастворимы в воде (MgO), поэтому это утверждение будет сосредоточено на ангидридах карбоновых кислот.
Точки плавления и кипения падают на молекулярную структуру и межмолекулярные взаимодействия для (RCO)2Или это общая химическая формула этих органических соединений.
Если молекулярная масса (RCO)2Или это низкий уровень, это, вероятно, бесцветная жидкость при комнатной температуре и давлении. Например, уксусный ангидрид (или этановый ангидрид), (СН3СО)2Или это жидкость, имеющая большое промышленное значение, так как ее производство очень велико..
Реакция между уксусным ангидридом и водой представлена следующим химическим уравнением:
(СН3СО)2O H2O => 2CH3COOH
Обратите внимание, что при добавлении молекулы воды выделяются две молекулы уксусной кислоты. Обратная реакция, однако, не может происходить для уксусной кислоты:
2CH3COOH => (CH3СО)2O H2O (не бывает)
Надо прибегнуть к другому синтетическому маршруту. С другой стороны, дикарбоновые кислоты могут нагреваться; но это будет объяснено в следующем разделе.
Химические свойства оксида серы (iv)
Оксид серы (IV) – это типичный кислотныйоксид. За счет серы в степени окисления 4 проявляет свойства окислителяи восстановителя.
1. Как кислотный оксид, сернистый газ реагирует с щелочамии оксидами щелочных и щелочноземельных металлов.
Например, оксид серы (IV) реагирует с гидроксидом натрия. При этом образуется либо кислая соль (при избытке сернистого газа), либо средняя соль (при избытке щелочи):
SO2 2NaOH(изб) → Na2SO3 H2O
SO2(изб) NaOH → NaHSO3
Еще пример: оксид серы (IV) реагирует с основным оксидом натрия:
SO2 Na2O → Na2SO3
2. При взаимодействии с водой SO2 образует сернистую кислоту. Реакция обратимая, т.к. сернистая кислота в водном растворе в значительной степени распадается на оксид и воду.
SO2 H2O ↔ H2SO3
3. Наиболее ярко выражены восстановительные свойства SO2. При взаимодействии с окислителями степень окисления серы повышается.
Например, оксид серы окисляется кислородом на катализаторе в жестких условиях. Реакция также сильно обратимая:
2SO2 O2 ↔ 2SO3
Сернистый ангидрид обесцвечивает бромную воду:
SO2 Br2 2H2O → H2SO4 2HBr
Азотная кислота очень легко окисляет сернистый газ:
SO2 2HNO3 → H2SO4 2NO2
Озон также окисляет оксид серы (IV):
SO2 O3 → SO3 O2
Качественная реакция на сернистый газ и на сульфит-ион – обесцвечивание раствора перманганата калия:
5SO2 2H2O 2KMnO4 → 2H2SO4 2MnSO4 K2SO4
Оксид свинца (IV) также окисляет сернистый газ:
SO2 PbO2 → PbSO4
4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
Например, при взаимодействии с сероводородом сернистый газ восстанавливается до молекулярной серы:
SO2 2Н2S → 3S 2H2O
Оксид серы (IV) окисляет угарный газ и углерод:
SO2 2CO → 2СО2 S
SO2 С → S СO2
Циклические ангидриды
В отличие от других карбоновых кислот, которые требуют ацилхлорида, дикарбоновые кислоты могут конденсироваться в их соответствующем ангидриде. Для этого необходимо нагреть их, чтобы способствовать высвобождению H2О. Например, показано образование фталевого ангидрида из фталевой кислоты.

Обратите внимание, как пятиугольное кольцо завершено, и кислород, который связывает обе группы C = O, является его частью; Это циклический ангидрид. Кроме того, можно видеть, что фталевый ангидрид является симметричным ангидридом, так как оба R1 как R2 Они идентичны: ароматическое кольцо.
Не все дикарбоновые кислоты способны образовывать их ангидриды, потому что, когда их группы COOH широко разделены, они вынуждены заканчивать большие и большие кольца. Самое большое кольцо, которое может быть образовано, является гексагональным, большее, чем реакция.
Чистый серный ангидрид
Чистый серный ангидрид представляет собой бесцветную легкоподвижную жидкость уд. веса 1,92, кипящую при 44,8° и застывающую при 16,8° в кристаллическую прозрачную массу. При хранении, особенно в присутствии следов влаги, это вещество видоизменяется, превращаясь в длинные шелковистые кристаллы, которые при 50°, не плавясь, возгоняются.
Серный ангидрид жадно соединяется с водой, выделяя большое количество тепла и образуя серную кислоту:
SO3 Н2О = H2SO4 21 ккал
124 125126
Вы читаете, статья на тему Серный ангидрид SO3
Эстерификация
Кислотные ангидриды реагируют со спиртами с пиридином в среде с образованием сложного эфира и карбоновой кислоты. Например, реакция между уксусным ангидридом и этанолом считается:
(СН3СО)2O CH3СН2ОН => СН3Колорадо2СН2СН3 СН3COOH
Таким образом образуется этиловый эфир этаноата, СН3Колорадо2СН2СН3, и этановая кислота (уксусная кислота).
Практически, то, что происходит, является замещением водорода гидроксильной группы ацильной группой:
R1-OH => R1-OCOR2
В случае (СН3СО)2Или ваша ацильная группа -COCH3. Поэтому говорят, что группа ОН страдает ацилированием. Однако ацилирование и этерификация не являются взаимозаменяемыми понятиями; Ацилирование может происходить непосредственно в ароматическом кольце, известном как ацилирование Фриделя-Крафтса..
Таким образом, спирты в присутствии ангидридов кислот этерифицируются путем ацилирования..
С другой стороны, только одна из двух ацильных групп реагирует со спиртом, другая остается с водородом, образуя карбоновую кислоту; что за случай (СН3СО)2Или это этановая кислота.
Янтарный ангидрид

Здесь у нас есть другая циклическая, полученная из янтарной кислоты, дикарбоновая кислота. Обратите внимание, как три атома кислорода выдают химическую природу этого типа соединения.
Малеиновый ангидрид очень похож на янтарный ангидрид, с той разницей, что между атомами углерода, образующими основание пятиугольника, существует двойная связь..

