Лекция 2 кислород и сера.
План.
- Общая характеристика подгруппы. Кислород как химический элемент.
- Кислород как простое вещество.
- Озон.
- Сера как химический элемент.
- Сера как простое вещество.
- Соединения серы с отрицательной степенью окисления.
- Оксиды серы.
- Серная кислота и ее соли.
Главную подгруппу 6 группы составляют кислород, сера, селен, теллур и полоний. Все эти элементы (их иногда называют халькогены) имеют на внешнем валентном слое конфигурацию типа s2p4 , т.е. близкую к завершению. Это обуславливает окислительные способности этих элементов. Следует отметить, что их ЭО при переходе от кислорода к теллуру резко снижается, т.к. появление новых электронных слоев ведет к увеличению радиуса атомов. Наибольшей окислительной способностью обладают типичные неметаллы — кислород и сера.
Кислород как химический элемент. Кислород или Оксиген №8. 2 период, 6 группа, главная подгруппа.
Состав атома:8р, 8е—, 8n.
Схема строения: заряд ядра 8, два электронных слоя (2 е—, 6 е—)
Электронная и графическая формулы: 1s22s22p4
Типичный неметалл, сильный окислитель. Практически единственная степени окисления: -2.
Практически единственная валентность: II.
 Самый распространенный элемент на Земле. На его долю приходится почти половина массы земной коры и около 90% массы мирового океана. Встречается в свободном состоянии в виде двух аллотропных модификаций: кислород О2 и озон О3. Эти газы входят в состав атмосферы, кислород в нем составляет около 21% по объему, озон – доли процента. Входит в состав неорганических соединений оксидов и гидроксидов, а также в состав многих солей. Содержится в важнейших органических соединениях: спиртах, альдегидах, кислотах и сложных эфирах. Является органогеном, входит в состав белков, жиров и углеводов, нуклеотидов и т.д.
Самый распространенный элемент на Земле. На его долю приходится почти половина массы земной коры и около 90% массы мирового океана. Встречается в свободном состоянии в виде двух аллотропных модификаций: кислород О2 и озон О3. Эти газы входят в состав атмосферы, кислород в нем составляет около 21% по объему, озон – доли процента. Входит в состав неорганических соединений оксидов и гидроксидов, а также в состав многих солей. Содержится в важнейших органических соединениях: спиртах, альдегидах, кислотах и сложных эфирах. Является органогеном, входит в состав белков, жиров и углеводов, нуклеотидов и т.д.
2. Физические свойства кислорода. При н.у. это бесцветный газ, не имеющий запаха. Температура кипения кислорода (-183оС). Немного тяжелее воздуха, немного растворим в воде (в 100 объемах воды — около 5 объемов кислорода при 0оС). Жидкий кислород притягивается магнитом.
Химические свойства кислорода. Кислород во всех химических реакциях проявляет сильные окислительные свойства. Его бинарные соединения с элементами называются оксидами. Кислород образует оксиды со всеми элементами, кроме гелия, неона и аргона. Оксиды образуются при окислении простых веществ (непосредственно не взаимодействуют с кислородом только галогены, золото и платина), при окислении сложных веществ. Реакции взаимодействия веществ с кислородом часто сопровождаются выделением тепла и света и поэтому их называют горением. При горении веществ на воздухе выделяется такое же тепла, но часть его тратится на нагревание азота, входящего в состав воздуха, поэтому температура пламени значительно снижается. Оксиды могут образовываться и при разложении сложных веществ (гидроксидов и солей), эти реакции, наоборот, обычно идут с поглощением энергии.
P0 O20 => P2 5 O5-2
S O2 => SO2
Mg O2 => MgO
Fe O2 => Fe2O3
CH4 O2 => CO2 H2O
ZnS O2 => ZnO SO2
Cu(OH)2 => CuO H2O
CaCO3 => CaO CO2
Роль в природе: процессы дыхания, гниения по химической сути являются процессами окисления сложных органических веществ.
Применение: Как сырье для получения различных соединений; для интенсификации процессов в химической и металлургической промышленности; для получения высоких температур (сварка и резка металла, ракетное топливо); жидкий кислород в смеси с опилками или другими горючими веществами используют как ВВ; газообразный кислород используют в медицине для лечения различных заболеваний (оксигенотерапия).
3. Озон. При н.у. это газ, обладающий характерным запахом. Температура кипения озона (-112оС). Он тяжелее воздуха, растворим в воде (в 100 объемах воды — около 50 объемов озона при 0оС). 
Озон образуется из кислорода при пропускании через него электрического разряда или жесткого УФ излучения.
О2 => O3
Обратная реакция – распад озона – протекает самопроизвольно, т.е. озон неустойчивое соединение. Озон – один из сильнейших окислителей, при его взаимодействии с веществами тоже образуются оксиды, но реакции протекают более энергично, чем с кислородом. Как сильный окислитель озон убивает бактерии и применяется для обеззараживания воды и помещений. Озон ядовит, ПДК в воздухе 10-5% , при этой концентрации хорошо ощущается его запах. В верхних слоях атмосферы концентрация озона обычно лежит в пределах 10-7-10-6.
Оксиды- один из важнейших классов неорганических веществ. Они делятся на основные, кислотные и амфотерные оксиды. Все они образуют гидроксиды и соответствующие соли. Кислород входит также в состав большого количества органических соединений.
Роль кислорода в организме и использование кислорода и озона в медицине. Содержание кислорода в организме 62,43%. Взрослый человек потребляет 264 см3 кислорода в мин. Оксиген имеет исключительное биологической значение, от него зависят важнейшие биохимические процессы, он участвует во всех видах обмена веществ. Наиболее известный физиологический процесс с участием кислорода – дыхание. Этот сложный физиологический процесс включает в себя не только процесс газообмена в легких, но и транспорт кислорода с током крови от легких к клеткам. Именно там в митохондриях происходит процесс тканевого дыхания, т.е. процесс окисления органических веществ. Продукты окисления (СО2) кровь уносит к легким. А энергия, которая выделяется в процессе реакции окисления тратится на образование молекул АТФ. При гидролизе АТФ энергия снова выделяется и расходуется на нужды организма. Т.е. с участием кислорода проходят все окислительные реакции в организме, за счет энергии этих реакций протекают все физиологические процессы. С кислородом связаны также фагоцитарные функции организма. Вспомните особенности строения атома кислорода. У него ярко выраженные неметаллические, окислительные свойства. В медицинской практике используются не только множество соединений кислорода (оксидов, гидроксидов, кислот, солей, органических и неорганических соединений) но и простые вещества – кислород и озон. Оксигенотерапия – кислородом лечат гельминтозы, сердечно-сосудистые и инфекционные заболевания, он стимулирует работу нервной системы, обладает снотворным действием и т.д. Оксигенотерапия лежит в основе климатолечения. Оксигенобаротерапия – метод лечения, в котором используется дыхание воздушной смесью с повышенным содержанием кислорода, в специальных герметичных помещениях барокамерах. В озонотерапии используют озон. Это сильнейший окислитель, в больших количествах он ядовит. Образуется из кислорода при электрическом разряде, под действием УФ. Озон обладает бактерицидным, дезодорирующим действием; используется для обработки питьевой воды, помещений, белья; в смеси с кислородом используется для лечения различных заболеваний.
4.Сера как химический элемент. Сульфур №16. 3 период,6 группа, главная подгруппа.
Состав атома: 16р, 16е—, 16n.
Схема строения: заряд ядра 16, три электронных слоя (2 е—, 8 е—, 6 е—)
Электронная и графическая формулы:
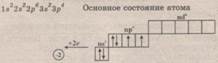
 Типичный неметалл. Характерные степени окисления: 6 и -2, возможна 4.
Типичный неметалл. Характерные степени окисления: 6 и -2, возможна 4.
Возможные валентности: II, IV, VI.

 Широко распространен в природе, содержание в земной коре 0,1%. Встречается в свободном состоянии (самородная сера) и в виде соединений. Например: сульфидов (железный колчедан FeS2, свинцовый блеск PbS) и сульфатов (гипс CaSO4∙2H2O, глауберова соль Na2SO4∙10H2O).Органоген, входит в состав белка
Широко распространен в природе, содержание в земной коре 0,1%. Встречается в свободном состоянии (самородная сера) и в виде соединений. Например: сульфидов (железный колчедан FeS2, свинцовый блеск PbS) и сульфатов (гипс CaSO4∙2H2O, глауберова соль Na2SO4∙10H2O).Органоген, входит в состав белка
.
5. Сера как простое вещество. Для серы характерна аллотропия. Три модификации. Сера ромбическая: твердое вещество желтого цвета, молекулярная кристаллическая решетка, S8, плавится при 112,8оС, плотность 2,07 г/см3. Нерастворима в воде, не смачивается. Растворяется в бензоле. Сера моноклинная: твердое вещество темно-желтого цвета, молекулярная кристаллическая решетка, S8, плавится при 119,3оС, плотность 1,96г/см3 . При н.у. неустойчива, превращается в ромбическую. Сера пластическая: резиноподобная коричневая масса, аморфное строение, S∞. При н.у. неустойчива, превращается в ромбическую.
 Химические свойства: типичный неметалл, может быть и окислителем и восстановителем.
Химические свойства: типичный неметалл, может быть и окислителем и восстановителем.
Как окислитель взаимодействует с металлами и водородом:
Al S→ Al2S3
Na S → Na2S
H2 S → H2S
Как восстановитель – с активными неметаллами:
S O2 →SO2


Получение:
1). Самородная сера. Перегретым водяным паром обрабатывают породу.
2). Разложение пирита без доступа воздуха: FeS2 → FeS S
3). Неполное сгорание сероводорода: H2S O2 → S H2O
Применение:
1). Получение серной кислоты и сульфатов.
2). Получение сульфитов.
3). Производство красителей, резины, черного пороха, спичек, лекарств.
Сера в организме человека и ее использование в медицине.
Содержание в организме 0,16%, суточная потребность 4-5 грамм. Больше всего серы содержится в кератине волос, костях, нервной ткани; входит в состав белков (аминокислоты цистеин и метионин), гормонов, витаминов. В организме серная кислота, образующаяся в процессе метаболизма, обезвреживает ядовитые продукты метаболизма (фенол, скатол, крезол) и чужеродные токсины (тяжелые металлы). Простое вещество сера оказывает противомикробное и противопаразитарное действие, серные мази и суспензии используют для лечения кожных заболеваний, гельминтозов. 1% раствор серы в персиковом масле (сульфозин) используют при лечении шизофрении и алкоголизма. Тиосульфат натрия обладает противовоспалительным и противоаллергическим действием.
Дата добавления: 2022-02-09; просмотров: 82; Нарушение авторских прав
§

 H2S — сероводород, бесцветный газ с характерным запахом гниющего белка. Кристаллизуется при -85,7оС, кипит при -60,8оС. Немного тяжелее воздуха, при н.у. в 1л воды растворяется 2,5 л сероводорода.
H2S — сероводород, бесцветный газ с характерным запахом гниющего белка. Кристаллизуется при -85,7оС, кипит при -60,8оС. Немного тяжелее воздуха, при н.у. в 1л воды растворяется 2,5 л сероводорода.
Восстановитель, окисляется кислородом воздуха (горение)
H2S O2 →SO2 H2O, при недостатке кислорода или низкой температуре H2S O2 →S H2O
Водный раствор называют сероводородной водой, на воздухе, на свету она становится мутной (опалесцирует) в результате образования коллоидного раствора серы в воде (см. предыдущую реакцию). Кроме того раствор сероводорода обладает свойствами кислоты, поэтому его называют сероводородной кислотой, это слабая кислота. Образуется при гниении белков, встречается в водах минеральных источников и вулканических газах. Такие источники могут быть причиной гибели человека ( Сероводород очень ядовит!), но могут использоваться и для лечения желудка, почек, кожи. Соли сероводородной кислоты называют сульфидами. Большинство из них нерастворимо в воде. В природе эти соли образуют минералы, которые используют как руды цветных металлов: ZnS, CuS, PbS…Многие сульфиды имеют переменный состав. В легкой промышленности используют сульфиды натрия и кальция для очистка кожи от шерсти. Сульфиды щелочноземельных металлов служат основой люминофоров. А в лабораториях реакции образования сульфидов используют для определения многих металлов, т.к. эти соли имеют характерный цвет.


Дата добавления: 2022-02-09; просмотров: 17; Нарушение авторских прав
§
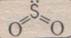 SO2 — оксид серы (IV), сернистый газ. Бесцветный газ с резким запахом, на воздухе не горит, легко растворяется в воде, ядовит.
SO2 — оксид серы (IV), сернистый газ. Бесцветный газ с резким запахом, на воздухе не горит, легко растворяется в воде, ядовит.
Химические свойства: кислотный оксид, характерны восстановительные свойства.
Как восстановитель:
SO2 O2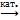 SO3, катализатор V2O5
SO3, катализатор V2O5
Как кислотный оксид сернистый газ взаимодействует со щелочами:
SO2 NaОН →NaНSO3 и Na2SO3 H2O (соли гидросульфиты и сульфиты).
С водою образуется сернистая (сульфитная) кислота.
SO2 H2O ↔ H2 SO3 Это слабый электролит. Нестойкая, существует только в водных растворах, легко окисляется кислородом воздуха до серной кислоты: H2 SO3 O2 → H2 SO4.
 Обесцвечивает органические красители.
Обесцвечивает органические красители.
Получение:
1). Горение серы: S O2 →SO2
2). Обжиг сульфидов: ZnS O2 → ZnO SO2 и т.д.
Большое количество сернистого газа образуется при горении органических соединений (каменный уголь).
Применение:
1). Производство серной кислоты.
2). Производство сульфитов и гидросульфитов.
3). В с/х для уничтожения насекомых и микроорганизмов.
4). В текстильной промышленности для отбеливания тканей, соломки и т.д.
5). При консервировании фруктов и ягод.
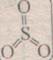 SO3 – оксид серы (VI), серный ангидрид. Молекула существует только в парах, при понижении температуры полимеризуется. При н.у. это бесцветная жидкость, летучая, «дымит» на воздухе, кристаллизуется при 17оС, кипит при 66оС. Легко растворяется в воде, токсичен.
SO3 – оксид серы (VI), серный ангидрид. Молекула существует только в парах, при понижении температуры полимеризуется. При н.у. это бесцветная жидкость, летучая, «дымит» на воздухе, кристаллизуется при 17оС, кипит при 66оС. Легко растворяется в воде, токсичен.
Химические свойства: сильный окислитель, кислотный оксид.
Как кислотный оксид:
SO3 H2O →H2 SO4 Q, взаимодействует с водой, образуя серную кислоту, при этом выделяется большое количества тепла.
SO3 NaОН →NaНSO4 и Na2SO4 H2O, т.е. образует гидросульфаты и сульфаты
Получение: в промышленности SO2 O2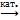 SO3, катализатор V2O5
SO3, катализатор V2O5
Применение: как промежуточный продукт при производстве серной кислоты, в лаборатории как сильное водопоглощающее средство.
Дата добавления: 2022-02-09; просмотров: 13; Нарушение авторских прав
§
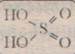 H2 SO4 –ббесцветная маслянистая жидкость, плотность 98% раствора 1,84 г/см,— нелетучая и запаха не имеет. Чрезвычайно гигроскопична, легко поглощает воду. При растворении выделяется большое количество тепла.
H2 SO4 –ббесцветная маслянистая жидкость, плотность 98% раствора 1,84 г/см,— нелетучая и запаха не имеет. Чрезвычайно гигроскопична, легко поглощает воду. При растворении выделяется большое количество тепла.
Химические свойства: 1. Сильная кислота, распадается на ионы по двум ступеням практически на 100%, образует два ряда солей.
H2SO4 ↔ H HSO4— — гидросульфат –ион
HSO4— ↔ H SO4 2- — сульфат- ион
Разбавленная кислота H2 SO4 обладает всеми общими свойствами кислот: изменяет окраску растворов индикаторов); взаимодействует с основаниями, основными оксидами и солями (реакции ионного обмена, не ОВР!):
H2SO4 2 KOH → K2SO4 2H2O;
2H SO42- 2K 2OH— = 2K SO42- 2H2O; H OH— = H2O
H2SO4 KOH → KНSO4 H2O
3H2SO4 Al2O3 → Al2(SO4)3 3H2O;
2H 3SO42- Al2O3 → 2Al3 3SO42- H2O ; 2H Al2O3 → 2Al3 H2O
H2SO4 Na2CO3→ Na2SO4 H2CO3 → Na2SO4 H2O CO2↑;
2H SO42- 2Na CO3→ 2Na SO42- H2O CO2↑; 2H CO3→ H2O CO2↑;
Во всех этих реакциях главную роль играют ионы водорода, а SO42- просто присутствует в растворе. Специфической реакцией иона SO42- (т.е. серной кислоты и всех ее солей) является реакция с солями бария.
H2SO4 BaCl2 → 2HCl BaSO4↓
2H SO42- Ba2 2Cl— → 2H 2Cl— BaSO4↓
SO42- Ba2 → BaSO4↓
Na2SO4 Ba(NO3)2 → 2NaNO3 BaSO4↓
2Na SO42- Ba2 2NO3— → 2Na 2NO3— BaSO4↓
SO42- Ba2 → BaSO4↓
Эту реакцию называют «качественной реакцией» на серную кислоту и ее соли, потому что в ней образуется характерный мелкокристаллический белый осадок BaSO4. Реакцию используют в лабораторной практике для определения наличия в растворе иона SO42-.
При взаимодействии с металлами серная кислота может вести себя по-разному, в зависимости от концентрации и активности металла.
В разбавленной H2SO4 окислителем является ион Н , поэтому разбавленная серная кислота взаимодействует только с металлами стоящими в ряду напряжений до водорода, причем, одним из продуктов реакции будет газ водород.
H2SO4(разб.) Zn → H2 ↑ ZnSO4
Zn0 – 2e— → Zn 2 H e— → H0
Но если мы возьмем концентрированную кислоту, то в роли окислителя выступит S 6 , и вместо водорода мы получим продукт ее восстановления – какое-то соединение серы. Какое? Это зависит от активности металла, температуры, концентрации кислоты. Обычно образуется смесь таких веществ. Но, упрощая, можно считать, что чем активнее металл, тем более глубоко идет процесс восстановления, и степень окисления серы в продукте реакции будет ниже. Следует также отметить, что с концентрированной H2SO4 взаимодействуют все металлы, кроме золота и платины, но на холоду железо, алюминий и хром пассивируются (не реагируют из-за образования прочной пленки на поверхности металла), а некоторые металлы не реагируют и с разбавленной серной кислотой (если при этом образуется нерастворимая соль).
H2SO4(конц.) Zn → ZnSO4 H2О S Zn0 – 2e— → Zn2 S 6 6e— → S0
H2SO4(конц.) Cu → ZnSO4 H2О SO2 Cu0 – 2e— → Cu2 S 6 2e— → S 4
H2SO4(конц.) Ca → CaSO4 H2О CaS Ca0 – 2e— → Ca2 S 6 8e— → S-2
H2SO4(конц.)– сильный окислитель, и может окислять не только металлы, но и неметаллы и даже их соединения, обугливает органические вещества (т.к. забирает воду, например, у углеводов)
H2SO4(конц.) C → СО2↑ H2О SO2↑
C0 – 4e— → C4 S 6 2e— → S 4
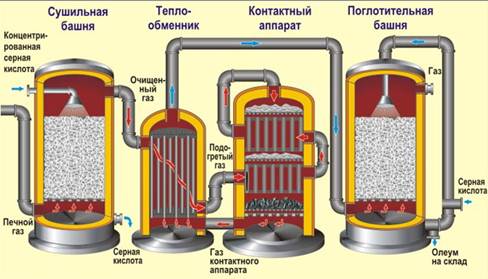
 Получение серной кислоты. В промышленности процесс получения серной кислоты обычно включает в себя три стадии. Сырьем является FeS2 (пирит, железный колчедан).
Получение серной кислоты. В промышленности процесс получения серной кислоты обычно включает в себя три стадии. Сырьем является FeS2 (пирит, железный колчедан).
1) обжиг колчедана (принцип теплообмена, в «кипящем слое», воздух обогащен кислородом):
FeS2 O2 → Fe2O3 SO2 13746кДж
2) каталитическое окисление сернистого газа (4500С, катализатор V2O5 оксид ванадия (V), принцип противотока):
SO2 O2 ↔ SO3 197,9кДж
 3) гидратация оксида серы (VI) (принцип противотока, принцип теплообмена, орошение концентрированной серной кислотой)
3) гидратация оксида серы (VI) (принцип противотока, принцип теплообмена, орошение концентрированной серной кислотой)
SO3 H2O →H2 SO4 130,6 кДж
Конечным продуктом является «олеум» — раствор SO3 в концентрированной H2 SO4.
В производстве серной кислоты часто используют сернистый газ, получаемый при обжиге цветных руд, горении топлива или свободной серы. Т.е. первая стадия может быть немного другой, а вот две последние – всегда одинаковы.
Применение. Серная кислота – «хлеб» химической промышленности.
 1) получение сульфатов, которые широко используются в народном хозяйстве, например:
1) получение сульфатов, которые широко используются в народном хозяйстве, например:
— K2SO4 и (NH4)2 SO4 — сульфаты калия и аммония, в с/х как минеральные удобрения
— CuSO4∙5H2O – медный купорос, в с/х как средство борьбы с болезнями растений, в легкой промышленности как краситель, в строительстве как противогрибковое средство, в гальванопластике (покрытие слоем меди)
FeSO4∙ 7H2O – железный купорос, в с/х средство борьбы с вредителями растений, в легкой промышленности при крашении тканей.
CaSO4∙ 2H2O – минерал гипс, в строительстве используют «жженый гипс» 2CaSO4∙ H2O под названием «алебастр» в состав шпаклевок, в медицине — слепки, шины, в художественно- прикладном творчестве.
Na2SO4∙ 10H2O – глауберова соль, в медицине как слабительное, в производстве стекла
BaSO4 –в медицине, (рентген желудка), в производстве бумаги, резины как наполнитель
2) в цветной металлургии (гидрометаллургия, получение меди, никеля и т.д.) и обработке металлов (печатные платы, гальваника, аккумуляторы и т.д.)
3) неорганический синтез (производство минеральных удобрений, пигментов, кислот…) и органический синтез (производство красителей, ВВ, полимеров…)
4) производство бумаги
5) производство соды (стекло, СМС)
Соли серной кислоты не обладают окислительными свойствами, вступают в обычные реакции ионного обмена.
Дата добавления: 2022-02-09; просмотров: 38; Нарушение авторских прав
Оксиды серы. общая характеристика, химические свойства ✎

Большинство школьников знают два оксида серы — SO2 и SO3.
Однако, это не все соединения, которые сера образует с кислородом.
Рассмотрим их все.
Монооксид серы — SO

- Встречается только в виде разбавленной газовой фазы;
- после концентрирования превращается в S2O2 (диоксид дисульфита);
Дисульфид серы — SO2

- эндогенный диоксид серы играет важную физиологическую роль в регуляции работы сердца и кровеносных сосудов, а нарушение его метаболизма может привести к артериальной гипертензии, атеросклерозу, стенокардии.
Триоксид серы, серный ангидрид — SO3

- Является значительным загрязнителем, основной компонент кислотных дождей;
- имеет большое значение в промышленности, так как является прекурсором серной кислоты;
- в сухой атмосфере обильно дымит, без запаха, но едкий;
- на воздухе образуется прямым окислением сернистого газа;
- в лаборатории триоксид серы можно получить путем двухстадийного пиролиза бисульфата натрия:
- серный ангидрид агрессивно гигроскопичен — теплота гидратации достаточна, чтобы смесь этого газа и древесины (или хлопка) могла воспламениться;
- при вдыхании вызывает ожоги, обладает высокой коррозионной активностью.
Тетроксид серы — SO4
- Этот оксид серы представляет собой группу химических соединений с формулой SO3 Х, где Х лежит между 0 и 1;
- здесь содержатся пероксогруппы (О-О), а степень окисления серы как в триоксиде серы, 6;
- может быть выделен при низких температурах (78 К), после реакции SO3 с атомарным кислородом или фотолиза смесей SO3 — озон.

Монооксид дисеры, субоксид серы — S2O
- Представляет собой бесцветный газ, который при конденсации образует твердое вещество бледного цвета, нестабильное при комнатной температуре;
- был обнаружен Питером Шенком в 1933 году.
Пoсле краткого обзора оксидов серы прилагаю таблицу двух важнейших оксидов серы — сернистого газа и серного ангидрида, так как именно они по большей части встречаются в заданиях ЕГЭ и ОГЭ по Химии.
Реагент | Оксид серы IV – SO2 — Диоксид серы; — газ с резким запахом; — кислотный оксид; — гибридизация серы – sp2; — валентный угол — 120 | Оксид серы VI – SO3 — Триоксид серы; — бесцветная летучая жидкость; — кислотный оксид; — гибридизация серы — sp3; — валентный угол 120 |
Получение | 1) В промышленности: S O2 = SO2 (360 C) 4FeS 7O2 = 2Fe2O3 4SO2 (t) 2) В лаборатории: Na2SO3 H2SO4 = Na2SO4 SO2 H2O (t) Me 2H2SO4 (k) = MeSO4 SO2 2H2O (Me = Cu, Hg, Bi, Ag) 2HBr 2H2SO4 (k) = Br2 SO2 2H2O | 1) В промышленности: 2SO2 O2 = 2SO3 (500 C, V2O5) SO2 O3 = SO3 O2 2) В лаборатории: 2CaSO4 = 2CaO 2SO3 (450 C) 2CuSO4 = 2CuO 2SO3 Na2S2O7 = Na2SO4 2SO3 |
O2 | 2SO2 O2 = 2SO3 Q | ≠ |
H2O | SO2 H2O = H2SO3 | SO3 H2O = H2SO4 |
H2O2 | SO2 H2O2 = H2SO4 | ≠ |
Основные оксиды | SO2 CaO = CaSO3 SO2 Na2O = Na2SO3 | SO3 Na2O = Na2SO4 SO3 CaO = CaSO4 |
Кислотные оксиды | SO2 CO = S 2CO2 (Al2O3, 500 C) SO2 NO2 = SO3 NO (нитрозный способ получения серной кислоты) | ≠ |
Амфотерные оксиды | SO2 Al2O3, BeO, ZnO ≠ | SO3 Fe2O3 = Fe2(SO4)3 |
Основания | SO2 2NaOH = Na2SO3 H2O SO2 Me(OH)x ≠ (Me = Fe, Cr, Al, Sn) SO2 2KOH (расплав) = 3K2SO4 K2S 4H2O (t) | SO3 2NaOH (разб.) = Na2SO4 H2O SO3 Ca(OH)2 = CaSO4 H2O |
Кислоты | SO2 4HI = S↓ 2I2 2H2O SO2 2H2S = 3S 2H2O SO2 2HNO3 (k) = H2SO4 2NO2 SO2 2HNO2 (p) = H2SO4 2NO | SO3 HF = HSO3F (45 C) SO3 HCl = HSO3Cl (20 C, в олеуме) SO3 H2SO4 CaF2 = 2HSO3F CaSO4 SO3 H2SO4 (безводн.) = H2S2O7 3SO3 H2S = 4SO2 H2O |
Соли | SO2 Na2CO3 = Na2SO3 CO2 (20 С) SO2 Na2SO3 = Na2S2O5 (в этаноле) SO2 PCl5 = PClO3 SCl2O (50 — 60 C) | SO3 MeF = MeSO3F (Me = Li, K, NH4) SO3 2KI = K2SO3 I2 SO3 Na2S = Na2SO4 |
Комплексные соли | 3SO2 Na3[Al(OH)6] (P) = Al(OH)3 3NaHSO3 | ≠ |
Неметалл | SO2 O3 = SO3 O2 SO2 2C = S↓ 2CO2 (600 С) SO2 Cl2 = SO2Cl2 (солнечный свет) SO2 F2 = SO2F2 (20 С, Pt) SO2 3F2 = SF6 O2 (650 C) SO2 2H2 = S↓ 2H2O SO2 3S = 2S2O (вакуум, эл. разряд) | 2SO3 C = 2SO2 CO2 10SO3 P4 = P4O10 10SO2 |
Металл | SO2 Me H2O = MeSO3 H2 (активные Ме) SO2 Me = MeS2O4 (Me = Zn, Co; в смеси этанола иводы) | SO3 Mg = MgO SO2 |
ОВР | SO2 Cl2 2H2O = 2HCl H2SO4 SO2 I2 2H2O = 2HI H2SO4 5SO2 2KMnO4 2H2O = K2SO4 2MnSO4 2H2SO4 5SO2 2K2Cr2O7 H2SO4 = K2SO4 Cr2(SO4)3 H2O SO2 2FeCl3 2H2O = 2FeCl2 H2SO4 2HCl SO2 2CuCl2 2H2O = 2CuCl 2HCl H2SO4 | SO3 2HCl = SO2 Cl2 H2O (t) SO3 2HBr = SO2 Br2 H2O (0 C) SO3 8HI = H2S 4I2 3H2O (0 C) |
Сера, химические свойства, получение
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Соли серной кислоты
Серная кислота, будучи двухосновной, образует два ряда солей: средние, называемые сульфатами, и кислые, называемые гидросульфатами. Сульфаты образуются при полной нейтрализации кислоты щелочью (на один моль кислоты приходится два моля щелочи), а гидросульфаты — при недостатке щелочи (на один моль кислоты — один моль щелочи):
Многие соли серной кислоты имеют большое практическое значение.
Качественная реакция на сульфат-ион. Большинство солей серной кислоты растворимо в воде. Соли CaSO4 и PbSO4 мало растворимы в воде, a BaSO4 практически нерастворима как в воде, так и в кислотах. Это свойство позволяет использовать любую растворимую соль бария, например ВаСl2, как реагент на серную кислоту и ее соли (точнее, на ион 
или в ионной форме:
При этом выпадает белый нерастворимый в воде и кислотах осадок сульфата бария.
Услуги по химии:
- Заказать химию
- Заказать контрольную работу по химии
- Помощь по химии
Лекции по химии:
- Основные понятия и законы химии
- Атомно-молекулярное учение
- Периодический закон Д. И. Менделеева
- Химическая связь
- Скорость химических реакций
- Растворы
- Окислительно-восстановительные реакции
- Дисперсные системы
- Атомно-молекулярная теория
- Строение атома в химии
- Простые вещества
- Химические соединения
- Электролитическая диссоциация
- Химия и электрический ток
- Чистые вещества и смеси
- Изменения состояния вещества
- Атомы. Молекулы. Вещества
- Воздух
- Химические реакции
- Закономерности химических реакций
- Периодическая таблица химических элементов
- Относительная атомная масса химических элементов
- Химические формулы
- Движение электронов в атомах
- Формулы веществ и уравнения химических реакций
- Химическая активность металлов
- Количество вещества
- Стехиометрические расчёты
- Энергия в химических реакциях
- Вода
- Необратимые реакции
- Кинетика
- Химическое равновесие
- Разработка новых веществ и материалов
- Зеленая химия
- Термохимия
- Правило фаз Гиббса
- Диаграммы растворимости
- Законы Рауля
- Растворы электролитов
- Гидролиз солей и нейтрализация
- Растворимость электролитов
- Электрохимические процессы
- Электрохимия
- Кинетика химических реакций
- Катализ
- Строение вещества в химии
- Строение твердого тела и жидкости
- Протекание химических реакций
- Комплексные соединения
Лекции по неорганической химии:
- Важнейшие классы неорганических соединений
- Водород и галогены
- Подгруппа азота
- Подгруппа углерода
- Общие свойства металлов
- Металлы главных подгрупп
- Металлы побочных подгрупп
- Свойства элементов первых трёх периодов периодической системы
- Классификация неорганических веществ
- Углерод
- Качественный анализ неорганических соединений
- Металлы и сплавы
- Металлы и неметаллы
- Производство металлов
- Переходные металлы
- Элементы 1 (1А), 2 IIA и 13 IIIA групп и соединения
- Элементы 17(VIIA), 16(VIA) 15(VA), 14(IVA) групп и их соединения
- Важнейшие S -элементы и их соединения
- Важнейшие d элементы и их соединения
- Важнейшие р-элементы и их соединения
- Производство неорганических соединений и сплавов
- Главная подгруппа шестой группы
- Главная подгруппа пятой группы
- Главная подгруппа четвертой группы
- Первая группа периодической системы
- Вторая группа периодической системы
- Третья группа периодической системы
- Побочные подгруппы четвертой, пятой, шестой и седьмой групп
- Восьмая группа периодической системы
- Водород
- Кислород
- Озон
- Водород
- Галогены
- Естественные семейства химических элементов и их свойства
- Химические элементы и соединения в организме человека
- Геологические химические соединения
Лекции по органической химии:
- Органическая химия
- Углеводороды
- Кислородсодержащие органические соединения
- Азотсодержащие органические соединения
- Теория А. М. Бутлерова
- Соединения ароматического ряда
- Циклические соединения
- Карбонильные соединения
- Амины и аминокислоты
- Химия живого вещества
- Синтетические полимеры
- Органический синтез
- Элементы 14(IVA) группы
- Азот и сера
- Растворы кислот и оснований

