- Введение
- .1 получение изопрена из изобутена и формальдегида
- Реакции присоединения
- 1. Гидрирование
- 2 Способы производства изопрена
- 2. Галогенирование алкадиенов
- 2.1 Синтез изопрена из ацетона и ацетилена
- 2.2 Синтез изопрена из пропилена
- 3. Гидрогалогенирование алкадиенов
- 5. Полимеризация
- Окисление алкадиенов
- 1. Мягкое окисление алкадиенов
- 2. Жесткое окисление
- 3. Горение алкадиенов
- Техника безопасности
- Безопасность
- Биологическая роль
- Изопрен
- Изопрен легко присоединяет по двойным связям водород, галогены, галогеноводороды, первичные и вторичные амины и др. его главное свойство — способность легко полимеризоваться и сополимеризоваться, например с бутадиеном, стиролом, акрилонитрилом, пропиленом [4, с.67].
- Литература
- Получение из фракции c5
- Помогите пожалуйста. какой объем co2 получится при горении 13.6 г изопрена в 78.4 л кислорода — спрашивалка
- Примечания
- Процессы дегидрирования
- Синтез полимеров
- Синтез терпенов
- Синтетические методы
- Список использованных источников
- Ссылки
- Устаревшие методы
- Физические свойства
- Химические свойства
- Экономические факторы
- Заключение
Введение
Основная особенность изопрена, заключается в том, что при полимеризации
он образует транс- и цис-полиизопреновые (аналог натуральному) изопреновые
каучуки. То, что натуральный каучук является полимером изопрена, было известно
уже в 1860 году. Только после открытия катализатора Циглера-Натта были получены
искусственные каучуки, практически равноценные по эластическим свойствам
натуральному [10, с.378].
Натуральный каучук получают из млечного сока некоторых тропических
деревьев. Выделенный из млечного сока каучук вулканизируют, т.е. обрабатывают
серой или хлористой серой, при этом каучук поглощает некоторое количество серы,
что значительно улучшает его качества: он становится эластичнее, сохраняет эти
свойства при значительных колебаниях температуры; становится также более
устойчивым к химическим воздействиям.
Полиизопреновые каучуки — каучуки общего назначения, которые используются
в таких изделиях: автомобильных, самолетных, велосипедных камер и покрышек [10,
с.356].
Задачами данной работы являются:
Определение основных способов как промышленного, так и лабораторного
получения изопрена;
Рассмотрение аппаратурного оформления и технологии получения продукта для
каждого способа;
Выявление наиболее эффективного в настоящее время промышленного способа
получения изопрена.
.1
получение изопрена из изобутена и формальдегида
При взаимодействии изобутена с формальдегидом (реакция Принса) при более
высокой температуре в жидкой фазе наблюдается постепенное разложение
4,4-диметил-1,3-диоксана (ДМД), ненасыщенных спиртов и диола с образованием
изопрена. Это видно из рисунка 2, на котором представлена зависимость выхода
продуктов от времени реакции при 160 °С.
— формальдегид; 2 — 4,4-диметилдиоксан-1,3; 3 — изопрен;
4-3-метилбутен-3-ол-1; 5 — 3-метилбутен-2-ол-1; 6 — 5-метилдигидропиран-5,6; 7
— трет-бутилметиловый эфир; 8 — 3-метилбутандиол-1,3.
Рисунок 2 — График зависимости выхода продуктов рекции формальдегида с
изобутеном от времени реакции
На этой основе разработан одностадийный синтез изопрена в жидкой фазе при
150-160°С, ≈ 3 МПа и катализе водорастворимыми кислотами Льюиса. Кроме
снижения числа аппаратов и капитальных затрат при одностадийном процессе легче
решается проблема утилизации побочных продуктов, в том числе и трет-бутанола,
который можно возвращать на реакцию, где он находится в равновесии с изобутеном
[7, с.348].
Предложено даже вместо изобутена использовать в качестве сырья
трет-бутанол (полученный при извлечении изобутена из С4-фракции или при
изобутеновом варианте эпоксидирования пропилена):
Упрощенная технологическая схема получения изопрена из изобутеновой
фракции и формальдегида изображена на рисунке 3:
, 2 — реакторы I стадии; 3, 7, 10-13, 18, 19 — ректификационные колонны;
4 — дефлегматор; 5 — кипятильник; 6 — дроссельные вентили; 8 — насосы; 9
-нейтрализатор; 14 — теплообменник; 15 — реактор II стадии; 16 — холодильник;
17 — сепаратор.
Рисунок 3 — Принципиальная технологическая схема получения изопрена из
изобутена и формальдегида
Первую стадию проводят в двух трубчатых реакторах 1 и 2, охлаждаемых
водой. Изобутеновая фракция и разбавленный рециркулятом водный раствор
формальдегида движутся в них противотоком: более тяжелый, водный слой
опускается вниз, а легкий, углеводородный поднимается вверх, причем
диспергирование жидкостей позволяет создать большую поверхность контакта фаз.
Верхние и нижние части этих реакторов работают как сепараторы, в которых
отделяются соответственно углеводородный и водный слои. В первый переходят
почти полностью диоксан и ненасыщенные спирты, во втором слое остаются
непревращенный формальдегид, часть метанола и диола [17, с.59].
Водный слой из нижней части реактора 2 нейтрализуют щелочью и отгоняют из
него в колонне 3 все летучие вещества, которые объединяют с углеводородным
слоем. Затем в колонне 7 из кубового остатка колонны 3 и рециркулирующего
формалина со второй стадии процесса отгоняют разбавленный водный раствор
формальдегида, отделяя его от тяжелых остатков.
Этот раствор возвращают на
реакцию, добавляя к нему свежий формалин [17, с.35]. Углеводородный слой с
верха реактора 1 и легкий погон ректификации водного слоя объединяют и
обрабатывают в нейтрализаторе 9 движущимся противотоком водным раствором
щелочи, который после этого смешивают с водным слоем, выходящим из реактора 2,
подавая на совместную переработку, описанную выше.
Из промытого углеводородного
слоя в колонне 10 отгоняют непревращенный изобутен, возвращая его на реакцию
(при использовании фракции, содержащей бутаны и н-бутены, во избежание их
накопления в рециркуляте необходима дополнительная ректификация для
«укрепления» изобутена).
Затем в колонне 11 из продуктов реакции отгоняют более
летучие метанол и метилаль, а в колонне 12 — трет-бутанол. Диоксан (вместе с
ненасыщенными спиртами) отделяют в колонне 13 от тяжелого остатка и направляют
на вторую стадию процесса [16, с.34].
Диоксан нагревают и испаряют в теплообменнике 14 за счет тепла горячей
реакционной массы, смешивают с перегретым паром и подают в реактор 15 второй
стадии (адиабатического типа со стационарным слоем гетерогенного катализатора).
Реакционная смесь проходит через теплообменник 14, охлаждается и конденсируется
в холодильнике 16 органический слой отделяется от водного в сепараторе 17.
— колонна обезметаноливания формальдегида; 2, 3 — реакторы; 4
-экстракционная колонна; 5 — колонна отгонки легколетучих углеводородов; 6 —
колонна упаривания водного слоя; 7 — колонна концентрирования формальдегида; 8
— узел очистки водного слоя; 9 — колонна отмывки непрореагировавшего
формальдегида; 10 — колонна отгонки легкой фракции С4; II — колонна
выделения ДМД и ТМК.
Рисунок 4 — Принципиальная технологическая схема синтеза ДМД
Органический слой с верха сепаратора 17 подают последовательно в две
ректификационные колонны. В первой (18) отгоняют образовавшийся при разложении
диоксана изобутен, который возвращают на первую стадию синтеза. Затем в колонне
19 отделяют изопрен от более высококипящего остатка (непревращенный диоксан и
побочные продукты).
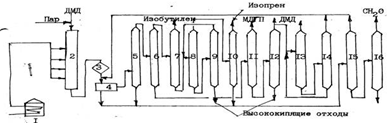 4 и С5;
4 и С5;
7 — колонна отгонки изобутилена; 8,9 — колонны выделения изопрена —
ректификата; II — колонна отгонки МДГП; II2 — колонна выделения возвратного
ДМД; I3 — абсорбер; I4 — десорбер; I5 — колонна отгонки летучих органических
веществ из водного слоя; I6 — колонна рекуперации СН2О.
Рисунок 5 — Принципиальная технологическая схема каталитического
разложения ДМД и получение изопрена
Сообщается о высокой селективности (до 80% по формальдегиду и 90% по
изобутену), снижении коррозии аппаратуры и высоком качестве получаемого
изопрена [10, с.396].
2.2
Получение изопрена из изоамиленов и изопентана
Способы каталитического дегидрирования применяются в производстве
изопрена из изосоединений С5 — изопентана и изоамиленов. Если в
качестве исходного продукта применять изопентан, то процесс каталитического
дегидрирования будет протекать в две стадии: изопентан- изоамилены-изопрен.
Получение изопрена из изоамиленов и из изопентана схематически может быть
представлено уравнениями:
Методом каталитического дегидрирования изопентана при нормальном давлении
и 525-535% °C можно получить изоамилены с выходом 33-37% на пропущенный и
83-87% на разложенный изопентан. Реакции каталитического дегидрирования
углеводородов С5 протекают, как правило, при температурах на 25-30
°C более низких, чем при дегидрировании углеводородов С4.
Получение изопрена из изопентана усложняется тем, что при дегидрировании
изопентана образуется значительное большое количество изомеров. Кроме этого,
дегидрирование в большей мере сопутствуют реакции изомеризации.
При дегидрировании изопентана образуются три изомера изоамиленов:
2-метилбутилен-1; 2-метилбутилен-2 и 3-метилбутилен-1, кипящие соответственно
при 31,05, 38,49 и 20 °C; преимущественно образуется 2-метилбутилен-2 в
количестве около 65% от всех изоамиленов.
Вследствие реакций изомеризации, происходящих при каталитическом
дегидрировании изопентана, и наличия в техническом изопентане некоторого
количества н-пентана фракция С5, выделенная из продуктов
дегидрирования, содержит сложную смесь продуктов, состоящую из изопентана, н-пентана,
трех изоамиленов, трех н-амиленов (пентен-1, пентен-2, цис- и транс-),
пиперилена (цис- и транс-), изопрена, циклопентадиена.
Реакция дегидрирования изоамиленов в изопрен может быть выражена
уравнением:
Теплота этой реакции Q зависит от структуры исходного изоамилена: для дегидрирования
2-метилбутилена-2 она составит 32,895 ккал/моль, для 3-метилбутилена-1 —
29,478 ккал/моль и для 2-метилбутилена-1 — 31,324 ккал/моль. Все
три изоамилена образуют изопрен.
Проведение этой реакций требует низких парциальных давлений и высокой температуры.
Изоамилены при дегидрировании в присутствии водяного пара и катализатора
образуют 75-85% изопрена.
Метод получения изопрена из изоамиленов и изопентана требует жесткого
режима и сложного фракционирования как сырья, так и готового продукта. На пути
осуществления этого метода стоят еще и другие трудности, обусловленные
чувствительностью реакции полимеризации к примесям, содержащимся в мономерном
изопрене, полученным этим способом.
Недостатками этого процесса являются также
трудность обеспечения производства фракциями с высоким содержанием изопентана и
большое количество побочного продукта-пиперилена, для которого в настоящее
время не удается найти промышленного применения [20, с.90].
2.3
Получение изопрена жидкофазным окислением углеводородов
Получение изопрена жидкофазным окислением изопентена основано на реакции
эпоксидирования его органическими гидропероксидами.
Процесс включает в себя четыре стадии:
Окисление изопентана кислородом воздуха до трет-пентилгидропероксида:
Взаимодействие гидропероксида с 2-метилбутеном-2, который является
промежуточным продуктом синтеза, с образованием оксида 2-метилбутена-2:
Изомеризация оксида 2-метилбутена-2 в ненасыщенный спирт 2-метилбутен-1-ол-3:
Дегидратация спирта в изопрен:
Принципиальная блок-схема процесса приведена ниже на рисунке 6:
Рисунок 6 — Принципиальная технологическая схема получения изопрена
жидкофазным окислением углеводородов
Реакции присоединения
Для алкадиенов характерны реакции присоединения по одной из двойных связей С=С, либо по обоим связям. Реакции с водой, галогенами и галогеноводородами протекают по механизму электрофильного присоединения. При присоединении одной молекулы реагента к алкадиену рвется только одна двойная связь. При присоединении двух молекул реагента к алкадиену разрываются обе двойные связи.
| Помимо присоединения по одной из двух двойных связей (1,2-присоединение), для сопряженных диенов характерно так называемое 1,4-присоединение, когда в реакции участвует вся делокализованная система из двух двойных связей, реагент присоединяется к 1 и 4 атому углерода сопряженной системы, а двойная связь образуется между 2 и 3 атомами углерода. |
1. Гидрирование
Гидрирование алкадиенов протекает в присутствии металлических катализаторов, при нагревании и под давлением.
При присоединении одной молекулы водорода к дивинилу образуется смесь продуктов (бутен-1 и бутен-2):
Соотношение продуктов 1,2- и 1,4- присоединения зависит от условий реакции.
| При комнатной и повышенной температуре основным продуктом реакции является 1,4-продукт (бутен-2). |
При полном гидрировании дивинила образуется бутан:
2
Способы производства изопрена
Известны следующие промышленные методы получения изопрнена:
Синтез изопрена из ацетона и ацетилена;
Синтез изопрена из пропилена (димеризация пропилена);
Метатезис бутена.
2. Галогенирование алкадиенов
Присоединение галогенов к алкадиенам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
| При взаимодействии с алкадиенами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на двойную связь. |
| Например, при взаимодействии бутадиена-1,3 с бромной водой преимущественно протекает 1,4 присоединение и образуется 1,4-дибромбутен-2: |
Побочным продуктом бромирования дивинила является 3,4-дибромбутен-1:
При полном бромировании дивинила образуется 1,2,3,4-тетрабромбутан:
2.1
Синтез изопрена из ацетона и ацетилена
Процесс разрабатывался академиком А.Е.Фаворским, а затем И.Н. Назаровым и
протекает в три стадии. Этот способ малоприменим из-за дорогого сырья. изопрен изобутен
формальдегид пропилен
Синтез диметилацетиленилкарбинола (метилбутинола) из ацетона и ацетилена
в присутствии щелочного катализатора-порошкообразного КОН и растворителе —
диэтилового эфира:
В целях предупреждения образования побочных продуктов на первой стадии
применяется избыток ацетилена. В качестве катализатора используется ацетиленид
щелочного или щелочноземельного металла. Выход метилбутинола составляет 50-60
моль на 1 моль катализатора.
Гидрирование метилбутинола (МБИ) в диметилвинилкарбинол (метилбутенол):
Гидрирование МБИ осуществляется под давлением водорода 0,5-1 МПа и
температуре 30-80°С. Катализатор — коллоидный палладий на носителе.
Каталитическая дегидратация метилбутенола в изопрен:
Дегидратация диметилвинилкарбинола осуществляется путем пропускания паров
ДМВК с водой над технической окисью алюминия при 260-3000 С.
На рисунке 1 приведена принципиальная техническая схема производство
изопрена реакцией ацетилена с ацетоном:
— реактор этилирования; 2 — аппарат для обрыва реакции; 3 — сепаратор; 4
— колонна регенерации ацетона; 5 — колонна выделения тяжелого остатка; 6 —
реактор гидрирования; 7-сепаратор катализатора;8 — испаритель метилбутенола; 9
— ректор дегидратации; 10 — скруббер водной отмывки; 11 — ректификационная
колонна.
Рисунок 1 — Принципиальная технологическая схема получения изопрена из ацетилена
и ацетона
Аммиачно-ацетиленовая смесь компримируется до рабочего давления,
сжижается и вместе с ацетоном и катализатором вводится в реактор 1. Продукт
реакции направляется затем в реактор 2 для разложения катализатора. После
реактора 2 давление снижается до атмосферного и происходит испарение аммиака и
избытка ацетилена, который возвращается в ре-цикл.
Испаренная жидкость
подвергается ректификации в двух колоннах 4 и 5. Первая, из которых
предназначена для выделения небольшого количества непрореагировавшего ацетона,
а вторая — для удаления тяжелых побочных продуктов и соли, оставшейся после
разложения катализатора, в виде раствора.
С верха колонны 5 отбирается азеотроп
МБИ (метилбутинол — вода), который вместе с катализатором и избытком водорода, направляется
в реактор 6 для селективного гидрирования. Непрореагировавший водород
возвращается в рецикл, давление гидрированного продукта снижается до
атмосферного, затем на центрифуге от него отделяется катализатор, который в
свою очередь возвращается в ре-цикл [3, с.290].
Полученная по вышеописанной схеме смесь метилбутенола и воды испаряется в
аппарате 8 и направляется в реактор 9. Выделенные здесь пары изопрена
промываются в скруббере 10 водой от небольшого количества непрореагировавшего
метилбутенола и других побочных продуктов.
2.2 Синтез
изопрена из пропилена
Процесс получения изопрена проводится в три стадии.
Димеризация пропилена в 2-метилпентен-1 на металлорганических
катализаторах:
В результате реакции получается нестабильный алюминийалкил, который
впоследствии, взаимодействуя с пропиленом, распадается по схеме:
Изомеризация 2-метилпентена-1 в 2-метилпентен-2 на кислотных
катализаторах:
Пиролиз 2-метилпентена -2 в присутствии бромистого водорода:
Применение бромистого водорода в качестве инициатора пиролиза
2-метилпентена-2 требует изготовление печи из специальных жаро- и
коррозионностойких сталей. Достоинством метода является использование в
качестве сырья доступного и дешевого пропилена.
3. Гидрогалогенирование алкадиенов
Алкадиены взаимодействуют с галогеноводородами. При присоединении хлороводорода к бутадиену-1,3 преимущественно образуется 1-хлорбутен-2:
3-Хлорбутен-1 образуется в небольшом количестве.
При присоединении полярных молекул к алкадиенам образуется смесь изомеров. При этом выполняется правило Марковникова.
| Правило Марковникова: при присоединении полярных молекул типа НХ к алкадиенам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода при двойной связи. |
5. Полимеризация
Полимеризация — это процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
nM → Mn (M – это молекула мономера)
| Полимеризация алкадиенов протекает преимущественно по 1,4-механизму, при этом образуется полимер с кратными связями, называемый каучуком. |
Продукт полимеризации дивинила (бутадиена) называется искусственным каучуком:
При полимеризации изопрена образуется природный (натуральный) каучук:
Окисление алкадиенов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на мягкое и жесткое.
1. Мягкое окисление алкадиенов
Мягкое окисление алкадиенов протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкадиена разрываются только π-связи и окисляются атомы углерода при двойных связях. При этом образуются четырехатомные спирты.
| Обесцвечивание алкадиенами водного раствора перманганата калия, как и в случае алкенов – качественная реакция на двойную связь. |
2. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) происходит полный разрыв двойных связей С=С и связей С-Н у атомов углерода при двойных связях. При этом у окисляемых атомов углерода образуются связи с атомами кислорода.
Так, если у атома углерода окисляется одна связь, то образуется группа С-О-Н (спирт). При окислении двух связей образуется двойная связь с атомом углерода: С=О, при окислении трех связей — карбоксильная группа СООН, четырех — углекислый газ СО2.
Можно составить таблицу соответствия окисляемого фрагмента молекулы и продукта:
| Окисляемый фрагмент | KMnO4, кислая среда | KMnO4, H2O, t |
| >C= | >C=O | >C=O |
| -CH= | -COOH | -COOK |
| CH2= | CO2 | K2CO3 |
При окислении бутадиена-1,3 перманганатом калия в среде серной кислоты возможно образование щавелевой кислоты и углекислого газа:
3. Горение алкадиенов
Алкадиены, как и прочие углеводороды, горят в присутствии кислорода с образованием углекислого газа и воды.
В общем виде уравнение сгорания алкадиенов выглядит так:
CnH2n-2 (3n-1)/2O2 → nCO2 (n-1)H2O Q
| Например, уравнение сгорания бутадиена: |
2C4H6 11O2 → 8CO2 6H2O
Техника безопасности
По степени воздействия на организм человека каучук относится к
малоопасным веществам: 4-й класс по ГОСТ 12.1.007. При непосредственном
контакте местное раздражающее действие на кожу и слизистые оболочки глаз
отсутствует. Кожно-резорбтивное и сенсибилизирующие действия отсутствуют.
Кумулятивные свойства не выявлены [17, с.120].
Производственные помещения должны быть оборудованы общеобменной
приточно-вытяжной вентиляцией, местными отсосами. Кратность обмена воздуха
должна быть не менее 3. При производстве и применении каучука должно
использоваться оборудование в антистатическом пожаро- и взрывозащищенном
герметичном исполнении.
При пожаре опасность представляют продукты сгорания полимера, оксиды
углерода, сажа. При температуре переработки каучук невзрывоопасен и горит
только при внесении в источник огня. Температура воспламенения каучука — 290°С,
температура самовоспламенения — 340°С.
Обслуживающий персонал при производстве и переработке каучука должен
соблюдать нормы промышленной гигиены и промышленной санитарии, проходить
предварительный (при приеме на работу) и периодические профилактические
осмотры. Он должен проводить все работы, связанные с производством и
переработкой каучука, в специальной одежде и специальной обуви в соответствии с
требованиями ГОСТ 12.4.103 и ГОСТ 12.4.011 и типовых норм бесплатной выдачи
рабочим и служащим специальной одежды, обуви и др. [17, с.86].
Транспортная маркировка — по ГОСТ 14192. На каждое грузовое место наносят
манипуляционные знаки «Беречь от влаги» и «Беречь от солнечных лучей» по ГОСТ
14192, а также следующие данные:
а) наименование или товарный знак предприятия-изготовителя;
б) наименование и марку каучука;
в) номер партии;
г) номер места;
д) массу нетто;
е) месяц и год изготовления;
ж) обозначение настоящего стандарта и документа, по которому выпускают
каучук.
Безопасность
В высоких концентрациях в отношении животных изопрен проявляет анестетические свойства с последующим параличом и летальным исходом. Изопрен не вызывает точечных мутаций в тесте Эймса. Метаболизм происходит, в основном, в дыхательной системе: при этом происходит превращение изопрена в соответствующие эпоксиды и затем диолы.
Насыщение происходит при атмосферных концентрациях, равных 300—500 м д.[прояснить]; при более низких концентрациях скорость метаболизма прямо пропорциональна концентрации.
В высоких концентрациях изопрен оказывает на человека наркотическое действие, а также может вызывать раздражение кожи, глаз, слизистых оболочек и дыхательной системы. Предельно допустимая концентрация, установленная для изопрена в СССР, составляет 40 мг/м3[20].
Изопрен взрывоопасен и легко воспламеняется[7].
Биологическая роль
Изопрен в том числе в составе молекул других терпенов, встречается в разнообразных живых организмах: животных, растениях и микроорганизмах. В зависимости от организма число изопреновых фрагментов в молекуле терпена может составлять 1 (гемитерпены), 2 (монотерпены)
, 3 (сесквитерпены), 4 (дитерпены), 6 (тритерпены) или 8 (тетратерпены). В некоторых растениях обнаружены очень длинные терпены (каучук, гуттаперча), число звеньев изопрена в которых варьируется от нескольких тысяч до одного миллиона.
Изопрен может также входить в состав других природных соединений неизопреноидного строения (например, прениллипидов), повышая их липофильность. Известно, что синтез изопреноидов в растениях осуществляется двумя независимыми путями: ацетат/мевалонатным путём (ацетат/MVA) (образуются полипренолы) и дезоксиксилозафосфат/метилэритритфосфатным путём (DOXP/MEP).
Оба пути приводят к изопрену в виде так называемого «активного изопрена» — изопентенилпирофосфата (IPP), который под действием изомеразы может превращаться в изомерный 3,3-диметилаллилдифосфат (DMAPP). Сам изопрен получается из DMAPP при действии изопренсинтазы[21].
В середине XX века было обнаружено, что растения выделяют в атмосферу пары изопрена. Мировые объёмы выбросов фитогенного изопрена оцениваются в (180—450)⋅1012 г приведённого к массе углерода, содержащегося в соединении в год.
Эмиссия изопрена листьями растений ускоряется при температуре выше 28 °C и при высокой интенсивности солнечного излучения, когда процесс фотосинтеза полностью насыщен. Подтвердить это явление или проверить, способно ли растение выделять изопрен, можно при помощи спектроскопии в ультрафиолетовой области или путём анализа газов в газовом хроматографе, комбинированном с масс-спектрометром.
Физиологическая роль выделения растениями изопрена до конца не выяснена. Изопрен обеспечивает растениям повышенную устойчивость к перегреванию. Кроме того, как потенциальный уловитель радикалов, он может защищать растения от разрушающего воздействия озона и активных форм кислорода.
Предполагается также, что поскольку синтез изопрена требует постоянной затраты молекул АТФ и НАДФН, образующихся в процессе фотосинтеза, он таким образом сохраняет фотосистемы от перевосстановления и фотоокислительного разрушения в условиях чрезмерного освещения.
Из гомологического рядадиеновых углеводородов изопрен является наиболее часто встречающимся диеновым углеводородом в организме человека. По некоторым оценкам, скорость синтеза изопрена в организме человека составляет около 0,15 мкмоль/(кг·ч), что соответствует приблизительно 17 мг в час для человека массой 70 кг.
Изопрен также присутствует в ничтожных концентрациях во многих пищевых продуктах[источник не указан 2962 дня].
Изопрен
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
СТЕРЛИТАМАКСКИЙ
ФИЛИАЛ
ФЕДЕРАЛЬНОГО
ГОСУДАРСТВЕННОГО БЮДЖЕТНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ
ВЫСШЕГО
ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Естественнонаучный
факультет
Кафедра химии
и химической технологии
КУРСОВАЯ
РАБОТА
Изопрен
Стерлитамак
2022
Содержание
Введение
1 Литературный
обзор
1.1 Физико-химические характеристики изопрена
1.2 Способы производства изопрена
1.2.1 Синтез
изопрена из ацетона и ацетилена
1.2.2 Синтез
изопрена из пропилена
.2.3 Метатезис бутена
1.3 Применение изопрена
2
Технологическая часть
2.1 Получение
изопрена из изобутена и формальдегида
2.2 Получение изопрена из изоамиленов и
изопентана
.3 Получение изопрена
жидкофазным окислением углеводородов
3 Техника
безопасности.
Заключение
Список использованных
источников.
Изопрен легко присоединяет по двойным связям водород,
галогены, галогеноводороды, первичные и вторичные амины и др. его главное
свойство — способность легко полимеризоваться и сополимеризоваться, например с
бутадиеном, стиролом, акрилонитрилом, пропиленом [4, с.67].
Для получения изопрена в промышленности могут быть использованы шесть
способов. При взаимодействии ацетона и ацетилена получения изопрена
первоначально получается метилбутинол, который затем подвергается гидрированию,
а затем дегидратируется. Вторым методом получения изопрена является димеризация
пропилена.
В присутствии определенных видов катализаторов в реакции кроме
изопрена также образуется метан, который используется для моторного топлива для
автомобилей, в быту, а в промышленности в метан обычно добавляют одоранты
(обычно тиолы) со специфическим «запахом газа».
Литература
- Химическая энциклопедия / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 191—192.
- The Chemistry and Biology of Volatiles / Edited by A. Herrmann. — Wiley, 2022. — ISBN 9780470777787.
- Weissermel K., Arpe H.-J.1,3-Diolefins // Industrial Organic Chemistry. — 4th ed.. — Wiley, 2008. — P. 107—126. — ISBN 9783527619191. — doi:10.1002/9783527619191.ch5.
- Weitz H. M., Loser E. Isoprene (англ.) // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2000. — doi:10.1002/14356007.a14_627.
- Каримов Э. Х., Касьянова Л. З., Мовсумзаде Э. М., Даминев Р. Р., Каримов О. Х., Ялалов М. Р. Совмещение процессов окисления и дегидрирования изоамиленов в производстве изопрена на железокалиевом катализаторе // Теоретические основы химической технологии. 2022. Т. 50. № 1. С. 95.
- Karimov E. K., Kas’yanova L. Z., Movsumzade E. M., Daminev R. R., Karimov O. K., Yalalov M. R. Combination of oxidation and dehydrogenation processes of isoamylenes in the production of isoprene on iron potassium catalyst // Theoretical Foundations of Chemical Engineering. 2022. Т. 50. № 1. С. 92—96.
Получение из фракции c5
Фракция C5 является побочным продуктом крекинга углеводородов в процессе получения этилена. Она содержит небольшое количество изопрена, другие углеводороды с пятью атомами углерода в молекуле, а также ароматические углеводороды C6—C8.
Такая смесь может быть перегнана с выделением изопрена, обычно в количестве 2—5 массовых % в пересчёте на этилен. Однако выход может быть увеличен, если в качестве исходного сырья использовать более тяжёлую фракцию. Если крекинг проводится в более жёстких условиях (при повышенной температуре и в течение более долгого времени), то выход изопрена уменьшается.
Тем не менее такое ужесточение условий приводит к увеличению концентрации изопрена во фракции C5. Такое обогащение коммерчески выгодно, поскольку оно уменьшает затраты на транспортировку и получение чистого изопрена[12].
Перегонка фракции C5 не позволяет получить чистый изопрен, поскольку в смеси присутствуют некоторые компоненты, которые мало отличаются по температуре кипения. Для выделения чистого изопрена были предложены методы, основанные на отгонке азеотропной смеси с пентаном, а также методы с использованием экстракции селективными органическими растворителями (<i>N</i>-метилпирролидоном, диметилформамидом и ацетонитрилом)[14].
В целом, с точки зрения энергозатрат, выделение изопрена подобным способом гораздо выгоднее, нежели его химический синтез[15].
Помогите пожалуйста. какой объем co2 получится при горении 13.6 г изопрена в 78.4 л кислорода — спрашивалка

Георгий
Реакция горения: C5H8 7O2 = 5CO2 4H2O
Количество изопрена: n(C5H8) = m/M = 13,6 г/68 г/моль =0,2 моль
По уравнению, кислорода потребуется 5 7 раз больше, т. е. 1,4 моль
Количество кислорода: n(O2) = V/Vм = 78,4 л/22,4 л/моль = 3,5 моль
Изопрен в недостатке, количество СО2 — в 5 раз больше, т. е. 1 моль
Объём газа: V(CO2) = n*Vм = 1 моль*22,4 л/моль = 22,4 л
Примечания
- ↑ 12Ullmann, 2000, p. 84.
- ↑C. G. Williams Proceedings of the Royal Society (1860) 10.
- ↑ 12M. J. Loadman.Analysis of Rubber and Rubber-like Polymers (неопр.). — Springer, 2022. — С. 10. — ISBN 9789401144353.
- ↑Winfried R. Pötsch (Federführung); Annelore Fischer; Wolfgang Müller. Lexikon bedeutender Chemiker. Unter Mitarb. von Heinz Cassebaum. Frankfurt am Main, Deutsch, 1989, 470 S. ISBN 3-8171-1055-3.
- ↑Ullmann, 2000, p. 83—84.
- ↑Ullmann, 2000, p. 85—86.
- ↑ 12Химическая энциклопедия, 1990.
- ↑ 12Industrial Organic Chemistry, 2008, p. 120.
- ↑Ullmann, 2000, p. 86—87.
- ↑ 12Ullmann, 2000, p. 87.
- ↑Ullmann, 2000, p. 87—88.
- ↑ 123Ullmann, 2000, p. 88.
- ↑Industrial Organic Chemistry, 2008, p. 118.
- ↑Ullmann, 2000, p. 90.
- ↑ 12Industrial Organic Chemistry, 2008, p. 117.
- ↑ 123Ullmann, 2000, p. 94—95.
- ↑ 12Ullmann, 2000, p. 85.
- ↑ 12Ullmann, 2000, p. 92—93.
- ↑Ullmann, 2000, p. 93—94.
- ↑ 12Ullmann, 2000, p. 98.
- ↑Herrmann, 2022, p. 12—17.
- ↑Herrmann, 2022, p. 22—27.
- ↑Herrmann, 2022, p. 31—33.
Процессы дегидрирования
Реакции дегидрирования изопентана и изопентенов с образованием изопрена широко исследованы и напоминают аналогичные реакции получения бутадиена[12].
Одностадийный процесс дегидрирования изопентана под действием катализатора на основе Cr2O3/Al2O3 при 600 °C и 7 кПа даёт изопрен с выходом 52 %. Этот метод применялся в СССР.
Дегидрирование изопентенов (метилбутенов) протекает под действием катализатора Shell (Fe2O3/K2CO3/Cr2O3) при 600 °C с выходом 85 %.
Исходные углеводороды можно выделить из соответствующих перегонных фракций путём растворения в серной кислоте с последующим разложением эфира серной кислоты при 35 °C и обратной экстрацией изопентенов насыщенными углеводородами[12].
Синтез полимеров
Бо́льшая часть производимого изопрена используется в синтезе цис-1,4-полиизопрена — изопренового каучука, который по свойствам и строению похож на природный каучук и широко применяется в производстве автомобильных шин. Другой продукт полимеризации изопрена — транс-1,4-полиизопрен — имеет свойства гуттаперчи и не находит широкого использования в промышленности, кроме изготовления шаров для гольфа и изоляции проводов[18].
Важную область применения изопрена составляет синтез блок-сополимеров типа стирол-изопрен-стирол. Подобные продукты используются как термопластические полимеры и адгезивы, чувствительные к давлению. Изопрен также используется в синтезе бутилового каучука — продукта сополимеризации изопрена с изобутиленом, где мольная доля изопрена составляет от 0,5 до 3,0 %[18].
Синтез терпенов
С 1972 года компанией Rhodia Incorporated (США) была начата разработка методов промышленного синтеза терпенов из изопрена, ацетона и ацетилена. Синтетическая схема включала в себя присоединение хлороводорода к изопрену с образованием пренилхлорида, который затем в две стадии превращали в дегидролиналоол.
Последний служил в качестве исходного соединения для синтеза различных терпенов, например, линалоола, гераниола, цитраля, β-ионона и их производных. Позже завод был закрыт, однако японский производитель Kuraray продолжил выпускать по этой схеме не только указанные продукты, но также сквалан и другие соединения.
Природные терпены состоят из фрагментов изопрена, соединённых друг с другом по принципу «голова — хвост». Синтетические аналоги также должны иметь такую структуру, а также содержать двойные связи в определённых положениях. В связи с этим, промышленный синтез терпенов методами олигомеризации и теломеризации затруднён, и обычно пользуются другими подходами.
Тем не менее предложен способ синтеза мирцена димеризацией изопрена на катализаторе (натрий/диалкиламин). Этот способ реализуется в промышленном масштабе компанией Nissan Chemical Industries. Теломеризация изопрена под действием диэтиламина и бутиллития в качестве катализатора приводит к N,N-диэтилнериламину, который далее может быть превращён в линалоол, гераниол, нерол, цитронеллаль, гидроксицитранеллаль и ментол[16].
Синтетические методы
Промышленные методы получения изопрена могут быть разделены на группы в зависимости от исходных реагентов для сборки пятиуглеродного скелета молекулы:
- C1 C4⟶C5{displaystyle {ce {C1 C4 -> C5}}};
- C2 C3⟶C5{displaystyle {ce {C2 C3 -> C5}}};
- C3 C3⟶C6⟶C5 C1{displaystyle {ce {C3 C3 -> C6 -> C5 C1}}};
- C4 C4⟶C8⟶C5 C3{displaystyle {ce {C4 C4 -> C8 -> C5 C3}}}.
Основным блоком C4 для синтеза изопрена является изобутилен, к которому в кислой среде (серная кислота или ионообменные смолы) присоединяют формальдегид с образованием 4,4-диметил-1,3-диоксана с выходом 74—80 % (реакция Принса), который далее разлагают при нагревании (200—300 °C) в присутствии ортофосфорной кислоты, что даёт изопрен с выходом 43—46 %.
Метод был предложен в 1938 году и стал известен благодаря работам сотрудников Французского института нефти. Предпринимались попытки улучшения данного синтеза, связанные преимущественно с технологическими особенностями и использованием различных катализаторов.
Существенной чертой метода является выделение формальдегида при разложении 1,3-диоксана и связанное с этим образование смолы в установках по синтезу изопрена. Чтобы избежать подобных побочных процессов, предлагалось использовать различные химические аналоги формальдегида (метилаль, метилхлорметиловый эфир, диоксолан), а также генерировать его непосредственно при синтезе целевого продукта[6][7][8].
Также в качестве блока C4 может использоваться бутен-2. Его гидроформилирование в присутствии родиевогокатализатора приводит к 2-метилбутаналю, который затем подвергается каталитической дегидратации под действием фосфата магния-аммония, молекулярных сит либо цеолитов, что приводит к изопрену.
Синтез изопрена из блоков C2 и C3 был предложен Снампроджетти и использовался в Италии, давая 30 тыс. тонн изопрена в год. На первой стадии данного процесса происходит реакция между ацетоном и ацетиленом в присутствии KOH в жидком аммиаке при 10—40 °C и 20 бар.
Продукт присоединения селективно гидрируется до алкена, после чего дегидратируется при 250—300 °C на оксиде алюминия, давая изопрен. Общая селективность в расчёте на ацетон и ацетилен составляет 85 %. Метод позволяет получать очень чистый изопрен, однако такое производство является относительно затратным[10][8].
Промышленное получение изопрена путём димеризации пропилена, последующей изомеризации получаемого 2-метилпентена-1 в 2-метилпентен-2 и крекинга последнего в присутствии HBr с образованием метана и изопрена было воплощено на заводе в городе Бомонт (Техас), однако в 1975 году прекращено после пожара по причине роста цены на пропилен[10].
Интересным подходом к синтезу изопрена является метатезис бутена-2 с образованием пропилена и 2-метилбутена-2. Последний может быть дегидрирован различными известными способами. Недостаток данного подхода заключается в том, что поскольку в реакцию метатезиса могут вступать любые алкены, происходит образование разнообразных побочных продуктов.
Особенно эта ситуация усугубляется при промышленных масштабах производства, когда в качестве исходного реагента используется более дешёвый технический бутен-2, содержащий примесь бутена-1[11].
Список
использованных источников
1. Ахметов, Б.В., Задачи и упражнения по физической и
коллоидной химии. — Л.: Химия, 1989. — 239 с.
2. Платэ, Н.А., Сливинский, Е.Ф., Основы химии и
технологии полимеров. 2002. — 696 с.
3. Соколов, Р. С. Химическая технология. — М.: Владос,
2000. — 1.2 т.
4. Аверко-Антонович, Ю. О., Омельченко, Р. Я., Охотина,
Н. А., Эбич, Ю. Р. Технология резиновых изделий: учебное пособие для вузов. —
JL: Химия, 1991. — 352 с.
. Кирпичников, П. А., Авереко-Антонович, Л. А.,
Авереко-Антонович, Ю. О. Химия и технология синтитичёского каучука. — Л.:
Химия,1998. — 424 с.
6. Гармонова, И. В. Синтетический каучук — 2-е изд. —
Л.: Химия, 1994.
. Хананашвили, Л. М., Андрианов, К. А. Технология
элементорганических мономеров и полимеров. — М.: Химия, 1998.
. Чаушеский, Е. А. Новые исследования в области
высокомолекулярных соединений. — М.: Химия, 2005.
. Болдырев, А. П., Подвальный, С. Л. Управление
технологическими процессами в производстве стереорегулярного полиизопренового
каучука СКИ-3. — М.: ЦНИИТЭнефтехим, 1995.
. Кирпичников, П. А., Береснев, В. В., Попова, Л. М.
Альбом технологических схем основных производств промышленности синтетического
каучука. — Л.: Химия, 1996. — 224 с.
. Романова, Р. Г., Ламберов, А. А., Шайхутдинова, З.
И., Гильманов, Х. Х., Гильмуллин, Р. Р. Журнал прикладной химии. — Т. 81. Вып.
9., 2008.
. Рейсфельд, В. О., Шеин, B. C., Ермаков, В. И.
Реакционная аппаратура и машины заводов основного органического синтеза и
синтетического каучука. — Л.: Химия, 1995. — 392 с.
. Рейсфельд, В. О., Еркова, Л. Н. Оборудование
производств основного органического синтеза и синтитических каучуков. — Л.:
Химия, 1994. — 440 с.
. Будтов, В. П., Консетов В. В. Тепломассоперенос в
полимеризационных процессах. — Л.: Химия, 1993.
. Елисеева, В. И., Иванчев, С. С., Кучанов, С. И.,
Лебедев, А. В. Эмульсионная полимеризация и ее применение в промышленности.
-М.: Химия, 1996.
. Гончаров, А. И., Корнилов, М. Ю. Справочник по
химии. — М.: Высшая школа, 1977. — 304 с.
. Бочкарев, В. В., Ляпков, А. А., Основы
проектирования предприятий органического синтеза. Методические указания к
выполнению дипломного проекта. — Томск: ТПУ, 2002. — 52 с.
. Кузнецов, В. И., Волонский, Е. В. Развитие химии
высокомолекулярных соединений. — М.: Высшая школа, 2008.
. Огородников, С.К., Справочник нефтехимика. — Л.:
Химия, 1998.- 592 с.
20. Соколов,
Р.С. Химическая технология. — М.: ВЛАДОС, 2000. — 443 с.
Ссылки
Как только страница обновилась в Википедии она обновляется в Вики 2.Обычно почти сразу, изредка в течении часа.
Устаревшие методы
Изопрен был впервые получен английским химиком Чарльзом Уильямсом в 1860 году путём пиролиза натурального каучука и он же указал его верную эмпирическую химическую формулу C5H8[2][3] и дал веществу название без какого-либо объяснения значения[3][4].
Наиболее распространённым способом получения изопрена в лабораторных условиях было термическое разложение скипидарного масла в так называемой изопреновой лампе — специальном приборе с нагреваемой электрическим током спиралью. Во время Второй мировой войны в США изопрен получали пиролизом лимонена в промышленных масштабах.
До окончания войны изопрен был слишком дорог для производства синтетического каучука, однако ситуация изменилась с появлением методов его получения из нефти, а также с развитием технологии его полимеризации[5].
Физические свойства
При стандартных условиях изопрен представляет собой бесцветную летучую жидкость. Изопрен практически не растворяется в воде (0,029 мол. %), но смешивается во всех соотношениях с этанолом, диэтиловым эфиром, ацетоном и бензолом.
Химические свойства
Согласно данным спектроскопических исследований, при 50 °C большинство молекул изопрена находится в более устойчивой s-транс-конформации, и только 15 % молекул имеют s-цис-конформацию. Разность энергий между этими состояниями составляет 6,3 кДж/моль[17].
По химическим свойствам изопрен представляет собой типичный сопряжённый диен, вступающий в реакции присоединения, замещения, циклизации, комплексообразования и теломеризации. По сравнению с бутадиеном, он более активно реагирует с электрофилами и диенофилами за счёт донорного индуктивного эффектаметильной группы[17].
Экономические факторы
Ключевым фактором при планировании промышленного производства изопрена является месторасположение завода по разделению фракции C5, поскольку прибыльность зависит от возможности доставить эти фракции к месту разделения из нескольких заводов, на которых производится крекинг.
По состоянию на 1987 год в Западной Европе производилось 83 000 тонн диенов C5, из них 44 000 тонн приходилось на димеризованный циклопентадиен и 23 000 тонн на изопрен. Остальные 15 000 тонн составляли пиперилены[16].
К 1997 году мировые объёмы производства изопрена возросли до 850 000 тонн в год, из них 180 тыс., 130 тыс. и 30 тыс. тонн производились в США, Японии и Западной Европе соответственно. Крупнейшим производителем изопрена является Goodyear (США, 61 тыс. тонн в год)[15].
Заключение
В данной курсовой работе представлены основные способы получения
изопрена, физико-химические свойства, технология, схемы производства и
применение изопрена.
Было изучено, что в промышленности существует шесть способов получения
изопрена:
из пропилена;
метатезисом бутена;
из изобутена и формальдегида;
из изоамиленов и изопентана;
жидкофазным окислением углеводородов.
Промышленную реализацию получили 3 способа:
из ацетона и ацетилена;
из изобутена и формальдегида;
из изоамиленов и изопентана;
Достоинством первого способа получения изопрена из ацетона и ацетилена
является то, что выход изопрена составляет — 98,5%, но при этом способ
малоприменим из-за дорогого сырья. При изучении способа получения изопрена из
изобутилена и формальдегида выяснилось то, что селективность достигает до 90%,
что говорит о высоком качестве получаемого изопрена, а также о снижении
коррозии аппаратуры.
Достоинством способа получения изопрена из изоамиленов и изопентана
являются то, что выход изопрена — 85%, недостатками — требует жесткого режима и
сложного фракционирования как сырья, так и готового продукта. Наиболее
перспективным и экономичным способом получения изопрена является реакция из
изобутилена и формальдегида, а также реакцией изоамиленов и изопентана.





