- Биологическая роль кислорода
- История открытия
- Кислород – простое вещество o2
- Нахождение в природе
- Примечания
- Ракетное топливо
- Распространённость в природе.
- Распространенность оксигена в природе
- Реакции бензольного кольца
- Свойства
- Строение и физические свойства простых веществ
- Физические и химические свойства
- Физические свойства
Биологическая роль кислорода
Аварийный запас кислорода в бомбоубежище
Большинство живых существ (аэробы) дышат кислородом воздуха.
Широко используется кислород в медицине.
При сердечно-сосудистых заболеваниях, для улучшения обменных процессов, в желудок вводят кислородную пену («кислородный коктейль»).
Подкожное введение кислорода используют при трофических язвах, слоновости, гангрене и других серьёзных заболеваниях.
Для обеззараживания и дезодорации воздуха и очистки питьевой воды применяют искусственное обогащение озоном.
Радиоактивный изотоп кислорода 15O применяется для исследований скорости кровотока, лёгочной вентиляции.
История открытия
Официально считается[2][3], что кислород был открыт английским химиком Джозефом Пристли1 августа1774 года путём разложения оксида ртути в герметично закрытом сосуде (Пристли направлял на это соединение солнечные лучи с помощью мощной линзы).
Однако Пристли первоначально не понял, что открыл новое простое вещество, он считал, что выделил одну из составных частей воздуха (и назвал этот газ «дефлогистированным воздухом»).
О своём открытии Пристли сообщил выдающемуся французскому химику Антуану Лавуазье.
Несколькими годами ранее (в 1771 году) кислород получил шведский химик Карл Шееле.
Он прокаливал селитру с серной кислотой и затем разлагал получившийся оксид азота. Шееле назвал этот газ «огненным воздухом» и описал своё открытие в изданной в 1777 году книге (именно потому, что книга опубликована позже, чем сообщил о своём открытии Пристли, последний и считается первооткрывателем кислорода). Шееле также сообщил о своём опыте Лавуазье.
Важным этапом, который способствовал открытию кислорода, были работы французского химика Пьера Байена, который опубликовал работы по окислению ртути и последующему разложению её оксида.
Наконец, окончательно разобрался в природе полученного газа А. Лавуазье, воспользовавшийся информацией от Пристли и Шееле. Его работа имела громадное значение, потому что благодаря ей была ниспровергнута господствовавшая в то время и тормозившая развитие химии флогистонная теория.
Лавуазье провёл опыт по сжиганию различных веществ и опроверг теорию флогистона, опубликовав результаты по весу сожженных элементов. Вес золы превышал первоначальный вес элемента, что дало Лавуазье право утверждать, что при горении происходит химическая реакция (окисление) вещества, в связи с этим масса исходного вещества увеличивается, что опровергает теорию флогистона.
Таким образом, заслугу открытия кислорода фактически делят между собой Пристли, Шееле и Лавуазье.
Кислород – простое вещество o2
Кислород является молекулярным веществом, молекула двухатомна. В молекуле кислорода связь ковалентная неполярная.
При обычных условиях кислoрoд – газ без цвета и запаха, тяжелее воздуха, плохо растворим в воде (несколько лучше, чем азот). В жидком состоянии кислород светло-голубого, в твёрдом – синего цвета.
Кислород является хорошим окислителем. Реагирует практически со всеми простыми веществами (кроме инертных газов, галогенов, благородных металлов). Так, например, киcлород окисляет металлы:
O2 2Zn = 2ZnO3O2 4Al = 2Al2O3O2 2Cu = 2CuO2O2 3Fe = Fe3O4
Кислорoд является также окислителем многих неметаллов. В некоторых случаях, для того чтобы началась реакция, требуется нагревание:
O2 C = CO2O2 S = SO25O2 4Р = 2Р2O5O2 2Н2 = 2Н2O
Кислoрод реагирует с азотом в электрической дуге (реакция обратима, идёт с небольшим выходом NO):
В кислороде сгорают многие горючие вещества, практически все органические вещества:
2O2 СН4 = СO2 2Н202Н2S 3O2 = 2SO2 2Н20
Кислoрoд окисляет многие сложные вещества – как неорганические, так и органические:
O2 4Fe(OH)2 2Н20 = 4Fe(OH)3O2 2СН3СНО = СН3СООН.
В промышленности кислород получают перегонкой воздуха. Способ основан на том, что у азота и кислорода разные температуры кипения. В лаборатории киcлорoд получают:
а) электролизом воды:![]()



![]()
Нахождение в природе

Накопление O
2
в атмосфере Земли. Зелёный график — нижняя оценка уровня кислорода, красный — верхняя оценка.
1
. (3,85—2,45 млрд лет назад) — O
2
не производился
2
. (2,45—1,85 млрд лет назад) O
2
производился, но поглощался океаном и породами морского дна
3
. (1,85—0,85 млрд лет назад) O
2
выходит из океана, но расходуется при окислении горных пород на суше и при образовании озонового слоя
4
. (0,85—0,54 млрд лет назад) все горные породы на суше окислены, начинается накопление O
2
в атмосфере
5
. (0,54 млрд лет назад — по настоящее время) современный период, содержание O
2
в атмосфере стабилизировалось
Кислород — самый распространённый в земной коре элемент, на его долю (в составе различных соединений, главным образом силикатов) приходится около 47 % массы твёрдой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе). Более 1500 соединений земной коры в своём составе содержат кислород.
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе (около 1015 тонн). Однако до появления первых фотосинтезирующих микробов в архее 3,5 млрд лет назад, в атмосфере его практически не было. Свободный кислород в больших количествах начал появляться в палеопротерозое (3—2,3 млрд лет назад) в результате глобального изменения состава атмосферы (кислородной катастрофы).
Наличие большого количества растворённого и свободного кислорода в океанах и атмосфере привело к вымиранию большинства анаэробных организмов. Тем не менее, клеточное дыхание с помощью кислорода позволило аэробным организмам производить гораздо больше АТФ, чем анаэробным, сделав их доминирующими.
С начала кембрия 540 млн лет назад содержание кислорода колебалось от 15 % до 30 % по объёму. К концу каменноугольного периода (около 300 миллионов лет назад) его уровень достиг максимума в 35 % по объёму, который, возможно, способствовал большому размеру насекомых и земноводных в это время.
Основная часть кислорода на Земле выделяется фитопланктоном Мирового океана. Около 60 % кислорода от используемого живыми существами расходуется на процессы гниения и разложения, 80 % кислорода, производимого лесами, уходит на гниение и разложение растительности лесов.
Деятельность человека очень мало влияет на количество свободного кислорода в атмосфере. При нынешних темпах фотосинтеза понадобится около 2000 лет, чтобы восстановить весь кислород в атмосфере.
Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет около 25 %, по массовой доле — около 65 %.
В 2022 году датские учёные доказали, что свободный кислород входил в состав атмосферы уже 3,8 млрд лет назад.
Примечания
- ↑Дикислород // Большая Энциклопедия Нефти Газа
- ↑J. Priestley, Experiments and Observations on Different Kinds of Air, 1776.
- ↑W. Ramsay, The Gases of the Atmosphere (the History of Their Discovery), Macmillan and Co, London, 1896.
- ↑ 4,04,14,2Inorganic Crystal Structure Database
- ↑Margaret-Jane Crawford и Thomas M. Klapötke The trifluorooxonium cation, OF3 // Journal of Fluorine Chemistry. — 1999. — Т. 99. — С. 151-156.
- ↑Curie P., Curie M. (1899). «Effets chimiques produits par les rayons de Becquerel«. Comptes rendus de l’Académie des Sciences129: 823-825.
- ↑Радиационная химия // Энциклопедический словарь юного химика. 2-е изд.. — М.: 1990. — С. 200.
- ↑Руководство для врачей скорой помощи / Михайлович В. А. — 2-е изд., перераб. и доп. — Л.: Медицина, 1990. — С. 28-33. — 544 с. — 120 000 экз. — ISBN 5-225-01503-4. (см. ISBN )
- ↑Food-Info.net : E-numbers : E948 : Oxygen.
Ракетное топливо
В качестве окислителя для ракетноготоплива применяется жидкий кислород, пероксид водорода, азотная кислота и другие богатые кислородом соединения.
Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива (удельный импульс смеси водород — озон превышает удельный импульс для пары водород-фтор и водород-фторид кислорода).
Медицинский кислород хранится в металлических газовых баллонах высокого давления (для сжатых или сжиженных газов) голубого цвета различной ёмкости от 1,2 до 10,0 литров под давлением до 15 МПа (150 атм) и используется для обогащения дыхательных газовых смесей в наркозной аппаратуре, при нарушении дыхания, для купирования приступа бронхиальной астмы, устранения гипоксии любого генеза, при декомпрессионной болезни, для лечения патологии желудочно-кишечного тракта в виде кислородных коктейлей.
Для индивидуального применения медицинским кислородом из баллонов заполняют специальные прорезиненные ёмкости — кислородные подушки.
Для подачи кислорода или кислородо-воздушной смеси одновременно одному или двум пострадавшим в полевых условиях или в условиях стационара применяются кислородные ингаляторы различных моделей и модификаций. Достоинством кислородного ингалятора является наличие конденсатора-увлажнителя газовой смеси, использующего влагу выдыхаемого воздуха.
Для расчёта оставшегося в баллоне количества кислорода в литрах обычно величину давления в баллоне в атмосферах (по манометруредуктора) умножают на величину ёмкости баллона в литрах.
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавкиE948[9], как пропеллент и упаковочный газ.
Распространённость в природе.
К. – самый распространённый химич. элемент на Земле: содержание химически связанного К. в гидросфере составляет 85,82% (гл. обр. в виде воды), в земной коре – 49% по массе. Известно более 1400 минералов, в состав которых входит К. Среди них преобладают минералы, образованные солями кислородсодержащих кислот (важнейшие классы – карбонаты природные, силикаты природные, сульфаты природные, фосфаты природные), и горные породы на их основе (напр., известняк, мрамор), а также разл. оксиды природные, гидроксиды природные и горные породы (напр., базальт). Молекулярный К. составляет 20,95% по объёму (23,10% по массе) земной атмосферы. К. атмосферы имеет биологич. происхождение и образуется в зелёных растениях, содержащих хлорофилл, из воды и диоксида углерода при фотосинтезе. Количество К., выделяемое растениями, компенсирует количество К., расходуемое в процессах гниения, горения, дыхания. К. – биогенный элемент – входит в состав важнейших классов природных органич. соединений (белков, жиров, нуклеиновых кислот, углеводов и др.) и в состав неорганич. соединений скелета.
Распространенность оксигена в природе
Оксиген — один из самых распространенных элементов на нашей планете. В земной коре его атомов больше, чем атомов любого другого элемента (§ 6). Атомы Оксигена содержатся в песке, глине, известняке, многих минералах. Оксиген — второй по распространенности в атмосфере (после Нитрогена) и в гидросфере (после Гидрогена).
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 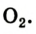
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 02. Это вещество содержит молекулы, состоящие из двух атомов Оксигена.
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
02 = 20.
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5 объема воздуха. Состав сухого воздуха
Организм взрослого мужчины ежесуточно потребляет приблизительно 900 г кислорода, а женщины — 600 г.
Состав воздуха:
Газ компонент воздуха Доля воздуха в%
| Название | Формула | объемная* | массовая |
| Азот | 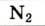 | 78,09 | 75,51 |
| Кислород | 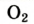 | 20,95 | 23,15 |
| Аргон | 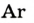 | 0,93 | 1,28 |
| углекислый газ | 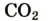 | 0,037 | 0,056 |
| Другие газы | менее 0,002 | менее 0,003 |
* Объемная доля вещества в смеси — отношение объема вещества к объему смеси. Объемную долю обозначают греческой буквой 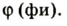
Определить объемную долю кислорода в воздухе можно экспериментально. Для этого нужны стеклянная бутылка без дна с пробкой и кристаллизатор с водой. В пробку вставляют ложку для сжигания, в которую набрано немного красного фосфора. Его поджигают, быстро вносят в бутылку и плотно I закрывают ее пробкой (рис. 52).
Кислород содержится не только в атмосфере. Небольшое его количество вместе с другими газами воздуха растворено в природной воде.
Существует еще одно простое вещество Оксигена — озон 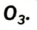 Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород:
Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород: 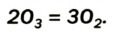
Озон содержится в атмосфере в незначительном количестве; его объемная доля не превышает
Определение объемной доли кислорода в воздухе сжиганием фосфора:
а — начало опыта;
б — окончание опыта
1 0,0004 %. Распадаясь, он поглощает часть ультрафиолетовых лучей солнечного света, вредную для растений и животных, и тем самым оберегает природу.
Реакции бензольного кольца
Наличие гидроксильного заместителя значительно облегчает протекание реакций электрофильного замещения в бензольном кольце.
1. Бромирование фенола. В отличие от бензола, для бромирования фенола не требуется добавления катализатора (бромида железа (III)).
Кроме того, взаимодействие с фенолом протекает селективно (избирательно): атомы брома направляются в орто- и параположения, замещая находящиеся там атомы водорода. Селективность замещения объясняется рассмотренными выше особенностями электронного строения молекулы фенола.
Так, при взаимодействии фенола с бромной водой образуется белый осадок 2,4,6-трибромфенола:
Эта реакция, так же, как и реакция с хлоридом железа (III), служит для качественного обнаружения фенола.
2. Нитрование фенола также происходит легче, чем нитрование бензола. Реакция с разбавленной азотной кислотой идет при комнатной температуре. В результате образуется смесь орто- и пара-изомеров нитрофенола:
При использовании концентрированной азотной кислоты образуется взрывчатое вещество — 2,4,6-тринитрофенол (пикриновая кислота):
3. Гидрирование ароматического ядра фенола в присутствии катализатора происходит легко:
4. Поликонденсация фенола с альдегидами, в частности с формальдегидом, происходит с образованием продуктов реакции — фенолформальдегидных смол и твердых полимеров.
Взаимодействие фенола с формальдегидом можно описать схемой:
Вы, наверное, заметили, что в молекуле димера сохраняются «подвижные» атомы водорода, а значит, возможно дальнейшее продолжение реакции при достаточном количестве реагентов:
Реакция поликонденсации, т.е. реакция получения полимера, протекающая с выделением побочного низкомолекулярного продукта (воды), может продолжаться и далее (до полного израсходования одного из реагентов) с образованием огромных макромолекул. Процесс можно описать суммарным уравнением:
Образование линейных молекул происходит при обычной температуре. Проведение же этой реакции при нагревании приводит к тому, что образующийся продукт имеет разветвленное строение, он твердый и нерастворим в воде. В результате нагревания фенолформальдегидной смолы линейного строения с избытком альдегида получаются твердые пластические массы с уникальными свойствами.
Полимеры на основе фенолформальдегидных смол применяют для изготовления лаков и красок, пластмассовых изделий, устойчивых к нагреванию, охлаждению, действию воды, щелочей и кислот, обладающих высокими диэлектрическими свойствами. Из полимеров на основе фенолформальдегидных смол изготавливают наиболее ответственные и важные детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиоприборов.
Клеи на основе фенолформальдегидных смол способны надежно соединять детали самой различной природы, сохраняя высочайшую прочность соединения в очень широком диапазоне температур. Такой клей применяется для крепления металлического цоколя ламп освещения к стеклянной колбе. Теперь вам понятно, почему фенол и продукты на его основе находят широкое применение.
Свойства
Строение внешней электронной оболочки атома К. 2s22p4; в соединениях проявляет степени окисления –2, –1, редко 1, 2; электроотрицательность по Полингу 3,44 (наиболее электроотрицательный элемент после фтора); атомный радиус 60 пм; радиус иона О2– 121 пм (координац. число 2). В газообразном, жидком и твёрдом состояниях К. существует в виде двухатомных молекул О2. Молекулы О2 парамагнитны. Существует также аллотропная модификация К. – озон, состоящая из трёхатомных молекул О3.
В осн. состоянии атом К. имеет чётное число валентных электронов, два из которых не спарены. Поэтому К., не имеющий низкой по энергии вакантной d-орбитали, в большинстве химич. соединений двухвалентен. В зависимости от характера химич. связи и типа кристаллич. структуры соединения координац. число К. может быть разным: 0 (атомарный К.), 1 (напр., О2, СО2), 2 (напр., Н2О, Н2О2), 3 (напр., Н3О ), 4 (напр., оксоацетаты Ве и Zn), 6 (напр., MgO, CdO), 8 (напр., Na2O, Cs2O). За счёт небольшого радиуса атома К. способен образовывать прочные π-связи с др. атомами, напр. с атомами К. (О2, О3), углерода, азота, серы, фосфора. Поэтому для К. одна двойная связь (494 кДж/моль) энергетически более выгодна, чем две простые (146 кДж/моль).
Парамагнетизм молекул О2 объясняется наличием двух неспаренных электронов с параллельными спинами на дважды вырожденных разрыхляющих π*-орбиталях. Поскольку на связывающих орбиталях молекулы находится на четыре электрона больше, чем на разрыхляющих, порядок связи в О2 равен 2, т. е. связь между атомами К. двойная. Если при фотохимич. или химич. воздействии на одной π*-орбитали оказываются два электрона с противоположными спинами, возникает первое возбуждённое состояние, по энергии расположенное на 92 кДж/моль выше основного. Если при возбуждении атома К. два электрона занимают две разные π*-орбитали и имеют противоположные спины, возникает второе возбуждённое состояние, энергия которого на 155 кДж/моль больше, чем основного. Возбуждение сопровождается увеличением межатомных расстояний О–О: от 120,74 пм в осн. состоянии до 121,55 пм для первого и до 122,77 пм для второго возбуждённого состояния, что, в свою очередь, приводит к ослаблению связи О–О и к усилению химич. активности К. Оба возбуждённых состояния молекулы О2 играют важную роль в реакциях окисления в газовой фазе.
К. – газ без цвета, запаха и вкуса; tпл –218,3 °C, tкип –182,9 °C, плотность газообразного К. 1428,97 кг/дм3 (при 0 °C и нормальном давлении). Жидкий К. – бледно-голубая жидкость, твёрдый К. – синее кристаллич. вещество. При 0 °C теплопроводность 24,65·10—3 Вт/(м·К), молярная теплоёмкость при постоянном давлении 29,27 Дж/(моль·К), диэлектрич. проницаемость газообразного К. 1,000547, жидкого 1,491. К. плохо растворим в воде (3,1% К. по объёму при 20 °C), хорошо растворим в некоторых фторорганич. растворителях, напр. перфтордекалине (4500% К. по объёму при 0 °C). Значит. количество К. растворяют благородные металлы: серебро, золото и платина. Растворимость газа в расплавленном серебре (2200% по объёму при 962 °C) резко понижается с уменьшением темп-ры, поэтому при охлаждении на воздухе расплав серебра «закипает» и разбрызгивается вследствие интенсивного выделения растворённого кислорода.
К. обладает высокой реакционной способностью, сильный окислитель: взаимодействует с большинством простых веществ при нормальных условиях, в осн. с образованием соответствующих оксидов (мн. реакции, протекающие медленно при комнатной и более низких темп-рах, при нагревании сопровождаются взрывом и выделением большого количества теплоты). К. взаимодействует при нормальных условиях с водородом (образуется вода Н2О; смеси К. с водородом взрывоопасны – см. Гремучий газ), при нагревании – с серой (серы диоксид SO2 и серы триоксид SO3), углеродом (углерода оксид СО, углерода диоксид СО2), фосфором (фосфора оксиды), мн. металлами (оксиды металлов), особенно легко со щелочными и щёлочноземельными (в осн. пероксиды и надпероксиды металлов, напр. пероксид бария BaO2, надпероксид калия KO2). С азотом К. взаимодействует при темп-ре выше 1200 °C или при воздействии электрич. разряда (образуется монооксид азота NO). Соединения К. с ксеноном, криптоном, галогенами, золотом и платиной получают косвенным путём. К. не образует химич. соединений с гелием, неоном и аргоном. Жидкий К. также является сильным окислителем: пропитанная им вата при поджигании мгновенно сгорает, некоторые летучие органич. вещества способны самовоспламеняться, когда находятся на расстоянии нескольких метров от открытого сосуда с жидким кислородом.
К. образует три ионные формы, каждая из которых определяет свойства отд. класса химич. соединений: $ce{O2^-}$– супероксидов (формальная степень окисления атома К. –0,5), $ce{O2^2^-}$ – пероксидных соединений (степень окисления атома К. –1, напр. водорода пероксид Н2О2), О2– – оксидов (степень окисления атома К. –2). Положительные степени окисления 1 и 2 К. проявляет во фторидах O2F2 и ОF2 соответственно. Фториды К. неустойчивы, являются сильными окислителями и фторирующими реагентами.
Молекулярный К. является слабым лигандом и присоединяется к некоторым комплексам Fe, Co, Mn, Cu. Среди таких комплексов наиболее важен железопорфирин, входящий в состав гемоглобина – белка, который осуществляет перенос К. в организме теплокровных.
Строение и физические свойства простых веществ
С простым веществом кислородом вы уже познакомились в курсе химии 7-го класса. Напомним, что простое вещество кислород в природе существует в виде двух аллотропных модификаций — обычного кислорода 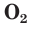 озона
озона 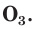
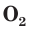
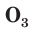
В природе озон образуется при грозовых разрядах и при окислении смолы хвойных деревьев. Небольшие количества озона в воздухе оказывают целебное действие на людей. Однако сильное обогащение воздуха озоном может стать опасным для здоровья. Увеличение содержания озона в воздухе выше предельно допустимой концентрации приводит к появлению головных болей, раздражению дыхательных путей и глаз, а затем к ослаблению сердечной деятельности.
Источниками озона являются работающие приборы, в которых происходит высоковольтный электрический разряд — копировальные установки и лазерные принтеры, а также источники ультрафиолетового и рентгеновского излучения. Поэтому помещения, в которых находятся такие приборы, необходимо часто проветривать.
Озон сосредоточен в верхних слоях атмосферы, образуя озоновый слой, который защищает Землю и ее обитателей от жесткого ультрафиолетового излучения Солнца. Поверхности Земли достигают только те ультрафиолетовые лучи, которые не опасны для живых организмов.
Кислород и озон в воде мало растворимы. При 20 °С в 100 объемах 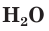
Физические и химические свойства
Физические свойства.
Низшие кислоты, т.е. кислоты с относительно небольшой молекулярной массой, содержащие в молекуле до четырех атомов углерода, — жидкости с характерным резким запахом (вспомните запах уксусной кислоты). Кислоты, содержащие от $4$ до $9$ атомов углерода, — вязкие маслянистые жидкости с неприятным запахом; содержащие более $9$ атомов углерода в молекуле — твердые вещества, не растворяющиеся в воде.
Температуры кипения предельных одноосновных карбоновых кислот увеличиваются с ростом числа атомов углерода в молекуле и, следовательно, с ростом относительной молекулярной массы. Так, например, температура кипения муравьиной кислоты равна $100,8°С$, уксусной — $118°С$, пропионовой — $141°С$.
Простейшая карбоновая кислота — муравьиная $НСООН$, имея небольшую относительную молекулярную массу $(M_r(HCOOH)=46)$, при обычных условиях является жидкостью с температурой кипения $100,8°С$. В то же время бутан $(M_r(C_4H_{10})=58)$ в тех же условиях газообразен и имеет температуру кипения $–0,5°С$.
Возникновение водородных связей становится понятным при рассмотрении строения молекул карбоновых кислот.
Молекулы предельных одноосновных карбоновых кислот содержат полярную группу атомов — карбоксил 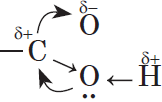
Муравьиная и уксусная кислоты растворимы в воде неограниченно. Очевидно, что с увеличением числа атомов в углеводородном радикале растворимость карбоновых кислот снижается.
Химические свойства.
Общие свойства, характерные для класса кислот (как органических, так и неорганических), обусловлены наличием в молекулах гидроксильной группы, содержащей сильную полярную связь между атомами водорода и кислорода. Рассмотрим эти свойства на примере растворимых в воде органических кислот.
1. Диссоциация с образованием катионов водорода и анионов кислотного остатка:
$CH_3-COOH⇄CH_3-COO^{-} H^ $
Более точно этот процесс описывает уравнение, учитывающее участие в нем молекул воды:
$CH_3-COOH H_2O⇄CH_3COO^{-} H_3O^ $
Равновесие диссоциации карбоновых кислот смещено влево; подавляющее большинство их — слабые электролиты. Тем не менее, кислый вкус, например, уксусной и муравьиной кислот объясняется диссоциацией на катионы водорода и анионы кислотных остатков.
Очевидно, что присутствием в молекулах карбоновых кислот «кислого» водорода, т.е. водорода карбоксильной группы, обусловлены и другие характерные свойства.
2. Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений до водорода: $nR-COOH M→(RCOO)_{n}M {n}/{2}H_2↑$
Так, железо восстанавливает водород из уксусной кислоты:
$2CH_3-COOH Fe→(CH_3COO)_{2}Fe H_2↑$
3. Взаимодействие с основными оксидами с образованием соли и воды:
$2R-COOH CaO→(R-COO)_{2}Ca H_2O$
4. Взаимодействие с гидроксидами металлов с образованием соли и воды (реакция нейтрализации):
$R—COOH NaOH→R—COONa H_2O$,
$2R—COOH Ca(OH)_2→(R—COO)_{2}Ca 2H_2O$.
5. Взаимодействие с солями более слабых кислот с образованием последних. Так, уксусная кислота вытесняет стеариновую из стеарата натрия и угольную из карбоната калия:
$CH_3COOH C_{17}H_{35}COONa→CH_3COONa C_{17}H_{35}COOH↓$,
$2CH_3COOH K_2CO_3→2CH_3COOK H_2O CO_2↑$.
6. Взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров — реакция этерификации (одна из наиболее важных реакций, характерных для карбоновых кислот):
Взаимодействие карбоновых кислот со спиртами катализируется катионами водорода.
Реакция этерификации обратима. Равновесие смещается в сторону образования сложного эфира в присутствии водоотнимающих средств и при удалении эфира из реакционной смеси.
В реакции, обратной этерификации, которая называется гидролизом сложного эфира (взаимодействие сложного эфира с водой), образуются кислота и спирт:
Очевидно, что реагировать с карбоновыми кислотами, т.е. вступать в реакцию этерификации, могут и многоатомные спирты, например глицерин:
Все карбоновые кислоты (кроме муравьиной) наряду с карбоксильной группой содержат в молекулах углеводородный остаток. Безусловно, это не может не сказаться на свойствах кислот, которые определяются характером углеводородного остатка.
7. Реакции присоединения по кратной связи — в них вступают непредельные карбоновые кислоты. Например, реакция присоединения водорода — гидрирование. Для кислоты, содержащей в радикале одну $π$-связь, можно записать уравнение в общем виде:
$C_{n}H_{2n-1}COOH H_2{→}↖{катализатор}C_{n}H_{2n 1}COOH.$
Так, при гидрировании олеиновой кислоты образуется предельная стеариновая кислота:
${C_{17}H_{33}COOH H_2}↙{text»олеиновая кислота»}{→}↖{катализатор}{C_{17}H_{35}COOH}↙{text»стеариновая кислота»}$
Непредельные карбоновые кислоты, как и другие ненасыщенные соединения, присоединяют галогены по двойной связи. Так, например, акриловая кислота обесцвечивает бромную воду:
${CH_2=CH—COOH Br_2}↙{text»акриловая(пропеновая)кислота»}→{CH_2Br—CHBr—COOH}↙{text»2,3-дибромпропановая кислота»}.$
8. Реакции замещения (с галогенами) — в них способны вступать предельные карбоновые кислоты. Например, при взаимодействии уксусной кислоты с хлором могут быть получены различные хлорпроизводные кислоты:
$CH_3COOH Cl_2{→}↖{Р(красный)}{CH_2Cl-COOH HCl}↙{text»хлоруксусная кислота»}$,
$CH_2Cl-COOH Cl_2{→}↖{Р(красный)}{CHCl_2-COOH HCl}↙{text»дихлоруксусная кислота»}$,
$CHCl_2-COOH Cl_2{→}↖{Р(красный)}{CCl_3-COOH HCl}↙{text»трихлоруксусная кислота»}$
Физические свойства
В мировом океане содержание растворённого O2 больше в холодной воде, а меньше — в тёплой.
При нормальных условиях кислород — это газ без цвета, вкуса и запаха.
1 л его имеет массу 1,429 г. Немного тяжелее воздуха. Слабо растворяется в воде (4,9 мл/100 г при 0 °C, 2,09 мл/100 г при 50 °C) и спирте (2,78 мл/100 г при 25 °C).
Хорошо растворяется в расплавленном серебре (22 объёма O2 в 1 объёме Ag при 961 °C).
Межатомное расстояние — 0,12074 нм. Является парамагнетиком.
При нагревании газообразного кислорода происходит его обратимая диссоциация на атомы: при 2000 °C — 0,03 %, при 2600 °C — 1 %, 4000 °C — 59 %, 6000 °C — 99,5 %.
Жидкий кислород (температура кипения −182,98 °C) — это бледно-голубая жидкость.
Твёрдый кислород (температура плавления −218,35°C) — синие кристаллы.
Известны 6 кристаллических фаз, из которых три существуют при давлении в 1 атм.:
- α-О2 — существует при температуре ниже 23,65 К; ярко-синие кристаллы относятся к моноклинной сингонии, параметры ячейкиa=5,403 Å, b=3,429 Å, c=5,086 Å; β=132,53°[4].
- β-О2 — существует в интервале температур от 23,65 до 43,65 К; бледно-синие кристаллы (при повышении давления цвет переходит в розовый) имеют ромбоэдрическую решётку, параметры ячейки a=4,21 Å, α=46,25°[4].
- γ-О2 — существует при температурах от 43,65 до 54,21 К; бледно-синие кристаллы имеют кубическую симметрию, период решётки a=6,83 Å[4].
Ещё три фазы образуются при высоких давлениях:

